WillD
Expert
- Joined
- Jul 19, 2021
- Messages
- 774
- Reaction score
- 1,062
- Points
- 93
Avec Battery acid
Avec l'acide muriatique
Avec l'acide acétique glacial
Isomérisation du CBD avec le pTSA.
A une solution de CBD (1000g) dans 20L de CH2Cl2 anhydre (ou de toluène), le pTSA (500g) a été ajouté à température ambiante, sous atmosphère d'azote. La réaction a été agitée dans les mêmes conditions pendant 48h. Ensuite, le mélange a été dilué avec Et2O et lavé avec une solution saturée de NaHCO3. La couche organique a été collectée, lavée avec de la saumure, séchée sur Na2SO4 anhydre et concentrée. CH2Cl2 : rendement Δ8-THC ~940g ; Toluène : rendement Δ9-THC ~820g, Δ8-THC ~10g.
Isomérisation du CBD avec pTSA et MW.
Dans un récipient ouvert ont été ajoutés du CBD (500g), 1L d'hexane, et 15,22g de pTSA. La réaction a été irradiée dans un four à micro-ondes commercial modifié pendant 5 minutes (1200W). La température des réactions a été contrôlée à l'aide d'un thermomètre à perles à thermocouple tressé en téflon. Le mélange réactionnel a été versé dans une solution saturée de bicarbonate de sodium et extrait avec du dichlorométhane. La couche organique combinée a été lavée avec de la saumure, séchée sur Na2SO4 et évaporée sous vide. Rendement Δ8-THC ~393g ; Δ9-THC ~16g.
Isomérisation du CBD avec pTSA et SN.
Dans un récipient ouvert ont été ajoutés du CBD (500g), 1L de toluène, et 15,22g de pTSA. La réaction a été soniquée à l'aide d'un bain à ultrasons (40KHz) pendant 10 minutes à 60°C. . La température des réactions a été contrôlée à l'aide d'un thermomètre à perles à thermocouple tressé en téflon. Le mélange réactionnel a été versé dans une solution saturée de bicarbonate de sodium et extrait avec du dichlorométhane. La couche organique combinée a été lavée avec de la saumure, séchée sur Na2SO4 et évaporée sous vide. Rendement Δ8-THC ~352g ; Δ9-THC ~72g.
1. 1 g de CBD a été ajouté à 35 ml d'éthanol à 95 % dans un ballon à fond rond (RBF) de 50 ml.
2. Placé dans un bain d'eau chaude à 70°C.
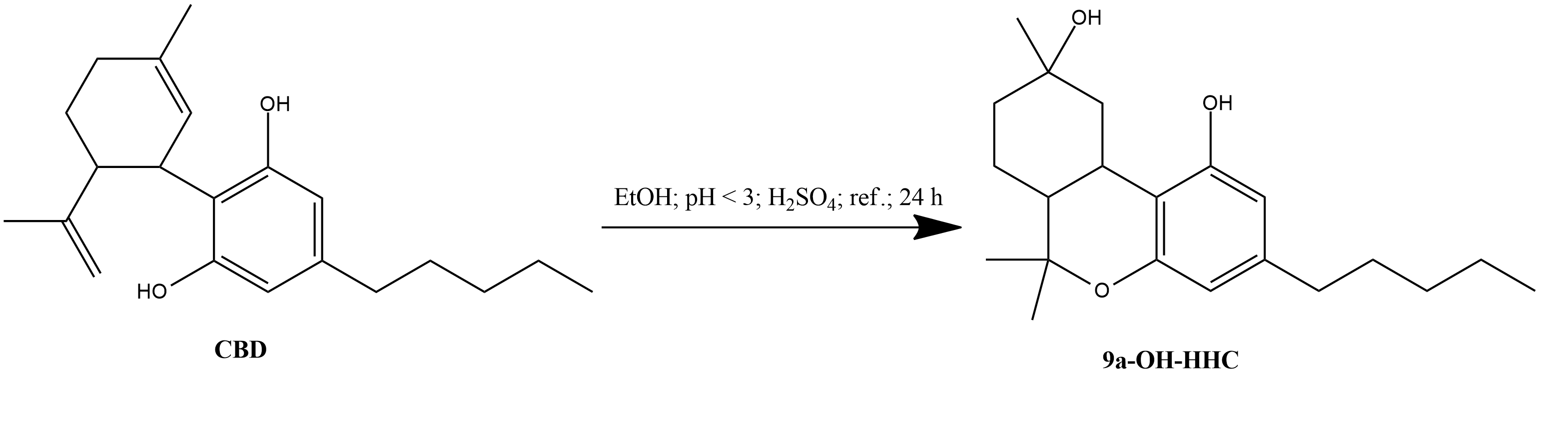
3. Une fois le CBD dissous, 4 gouttes d'acide sulfurique à 35 % ont été ajoutées pour acidifier la solution, pH < 3.
4. Le mélange a été laissé à reflux pendant 24 heures dans le bain-marie à 70°C.
5. Une fois terminé, 5 gouttes de NaOH 10M ont été utilisées pour basifier la solution jusqu'à ce que le pH soit supérieur à 10, ce qui élimine l'acide sulfurique sous forme de sulfate de sodium.
6. La réaction a ensuite été filtrée pour éliminer le sulfate de sodium, ce qui a permis de ne conserver que les cannabinoïdes dans la solution d'éthanol restante.
7. L'extraction de l'échantillon après 0 heure n'a permis de trouver que du CBD à 2,80 minutes, ce qui correspond aux échantillons de référence à 2,80 minutes. Après 1 heure, le pic de CBD a été réduit, mais restait le principal pic présent. Cependant, d'autres impuretés ont commencé à augmenter après 24 h, comme à 2,18 min et 3,40 min, qui se sont avérées être du 8-OH-iso- HHC et du 9α-OH-HHC. En outre, le doublet D 9-THC et D 8-THC a été trouvé à 4,10 min et 4,22 min. Un autre pic à 3,77 min s'est avéré être un pic d'isomérisation du D 9-THC et on pense qu'il s'agit du D 11-THC ou du D 7-THC. Cette méthode n'a pas isomérisé tout le CBD, même après 24 h. Cependant, le pic du CBD n'était plus le pic le plus important de l'échantillon. Le pic le plus important s'est avéré être le pic de 3,38, qui correspondait au 9α-OH-HHC.
2. Placé dans un bain d'eau chaude à 70°C.
3. Une fois le CBD dissous, 4 gouttes d'acide sulfurique à 35 % ont été ajoutées pour acidifier la solution, pH < 3.
4. Le mélange a été laissé à reflux pendant 24 heures dans le bain-marie à 70°C.
5. Une fois terminé, 5 gouttes de NaOH 10M ont été utilisées pour basifier la solution jusqu'à ce que le pH soit supérieur à 10, ce qui élimine l'acide sulfurique sous forme de sulfate de sodium.
6. La réaction a ensuite été filtrée pour éliminer le sulfate de sodium, ce qui a permis de ne conserver que les cannabinoïdes dans la solution d'éthanol restante.
7. L'extraction de l'échantillon après 0 heure n'a permis de trouver que du CBD à 2,80 minutes, ce qui correspond aux échantillons de référence à 2,80 minutes. Après 1 heure, le pic de CBD a été réduit, mais restait le principal pic présent. Cependant, d'autres impuretés ont commencé à augmenter après 24 h, comme à 2,18 min et 3,40 min, qui se sont avérées être du 8-OH-iso- HHC et du 9α-OH-HHC. En outre, le doublet D 9-THC et D 8-THC a été trouvé à 4,10 min et 4,22 min. Un autre pic à 3,77 min s'est avéré être un pic d'isomérisation du D 9-THC et on pense qu'il s'agit du D 11-THC ou du D 7-THC. Cette méthode n'a pas isomérisé tout le CBD, même après 24 h. Cependant, le pic du CBD n'était plus le pic le plus important de l'échantillon. Le pic le plus important s'est avéré être le pic de 3,38, qui correspondait au 9α-OH-HHC.
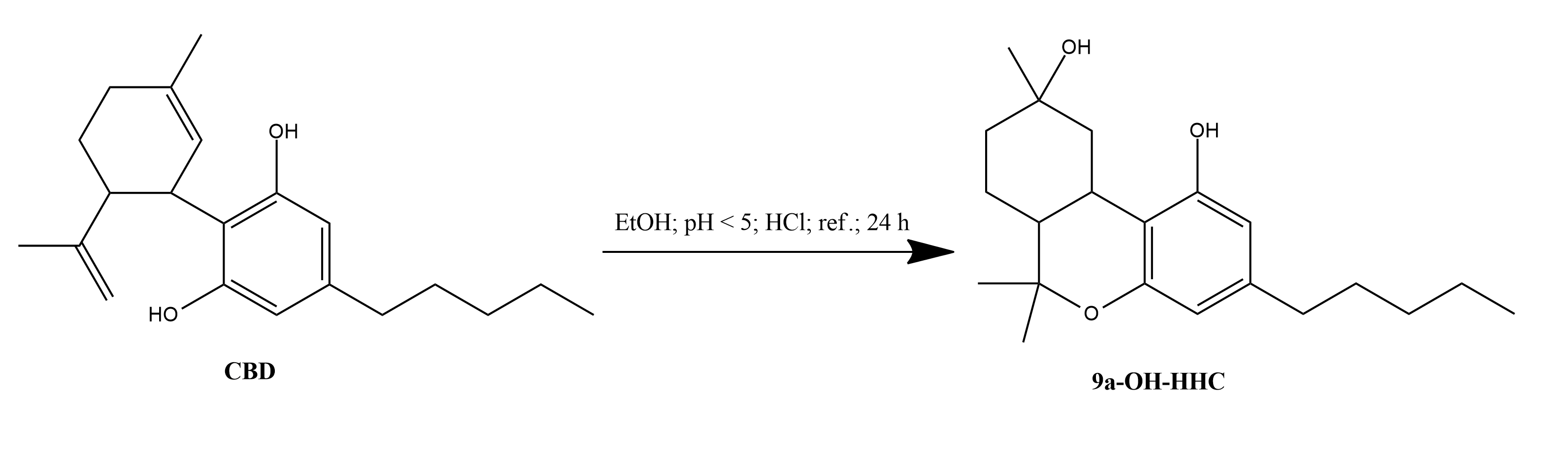
Avec l'acide muriatique
1. 1 g de CBD a été ajouté à 35 ml d'éthanol à 95 % dans un RBF de 50 ml.
2. Placé dans un bain d'eau chaude à 70°C.
3. Une fois le CBD dissous, 47,3 ml d'acide chlorhydrique à 37 % ont été ajoutés à la solution, pour obtenir une concentration finale de 0,05 % de HCl avec un pH inférieur à 5.
4. Le mélange a été laissé à reflux pendant 24 heures au bain-marie à 70°C.
5. L'extraction de l'échantillon pendant 0 h n'a permis de trouver que du CBD à 2,80 min, ce qui correspond aux échantillons de référence à 2,80 min. Après 1 heure, le pic de CBD a été réduit, mais restait le principal pic présent. Cependant, d'autres impuretés ont commencé à augmenter après 24 h, comme à 2,18 min et 3,40 min, qui se sont avérées être du 8-OH-iso- HHC et du 9α-OH-HHC. En outre, le doublet D 9-THC et D 8-THC a été trouvé à 4,10 min et 4,22 min. Un autre pic à 3,77 min s'est avéré être un pic d'isomérisation du D 9-THC et on pense qu'il s'agit du D 11-THC ou du D 7-THC. Une fragmentation a été effectuée et a montré qu'il avait la même fragmentation et les mêmes rapports que le D 9-THC et le D 8-THC, ce qui confirme qu'il s'agit d'un isomère du D 9-THC et du D 8-THC. Cette méthode n'a pas permis d'isomériser tout le CBD, même après 24 h. Cependant, le pic du CBD n'était plus le pic le plus important de l'échantillon. Le pic le plus important s'est avéré être le pic de 3,38, qui correspondait au 9α-OH-HHC.
2. Placé dans un bain d'eau chaude à 70°C.
3. Une fois le CBD dissous, 47,3 ml d'acide chlorhydrique à 37 % ont été ajoutés à la solution, pour obtenir une concentration finale de 0,05 % de HCl avec un pH inférieur à 5.
4. Le mélange a été laissé à reflux pendant 24 heures au bain-marie à 70°C.
5. L'extraction de l'échantillon pendant 0 h n'a permis de trouver que du CBD à 2,80 min, ce qui correspond aux échantillons de référence à 2,80 min. Après 1 heure, le pic de CBD a été réduit, mais restait le principal pic présent. Cependant, d'autres impuretés ont commencé à augmenter après 24 h, comme à 2,18 min et 3,40 min, qui se sont avérées être du 8-OH-iso- HHC et du 9α-OH-HHC. En outre, le doublet D 9-THC et D 8-THC a été trouvé à 4,10 min et 4,22 min. Un autre pic à 3,77 min s'est avéré être un pic d'isomérisation du D 9-THC et on pense qu'il s'agit du D 11-THC ou du D 7-THC. Une fragmentation a été effectuée et a montré qu'il avait la même fragmentation et les mêmes rapports que le D 9-THC et le D 8-THC, ce qui confirme qu'il s'agit d'un isomère du D 9-THC et du D 8-THC. Cette méthode n'a pas permis d'isomériser tout le CBD, même après 24 h. Cependant, le pic du CBD n'était plus le pic le plus important de l'échantillon. Le pic le plus important s'est avéré être le pic de 3,38, qui correspondait au 9α-OH-HHC.
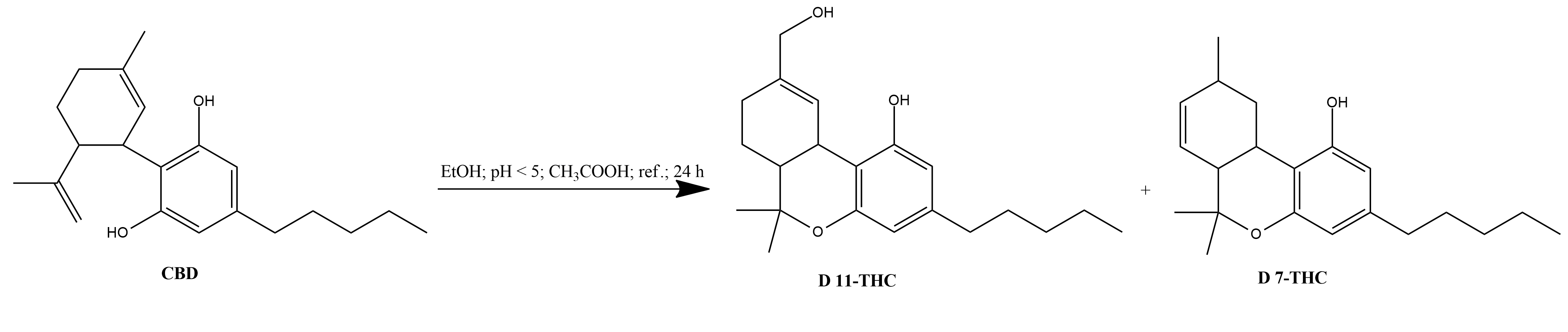
Avec l'acide acétique glacial
1. 1 g de CBD a été ajouté à 35 ml d'éthanol à 95 % dans un RBF de 50 ml.
2. Placé dans un bain d'eau chaude à 70°C.
3. Une fois le CBD dissous, 1,909 ml d'acide acétique glacial à 99 % ont été ajoutés à la solution, ce qui a donné une concentration finale de 5,2 % d'acide acétique.
4. Le mélange a été laissé à reflux pendant 24 heures au bain-marie à 70°C.
5. L'extraction de l'échantillon à 0 h a permis de trouver uniquement du CBD à 2,80 min, ce qui correspond aux échantillons de référence à 2,80. Après 1 h, les changements de l'isomérisation du CBD ont été constatés uniquement sous la forme d'une augmentation du pic à 3,77, que l'on pense être du D 11-THC ou du D 7-THC. Au bout de 4 heures, on a constaté une augmentation notable du pic du D 9-THC. Après 24 heures, la réaction a été analysée et a révélé que le 11-5 00 -dihydroxy-CBD, le 8-OH-iso-HHC, le CBD, le 10-méthoxy-THC et le D 9-THC ont été trouvés à 1,96 min, 2,22 min, 2,80 min, 3,50 min et 4,11 min, respectivement. Le composé à 3,77 min a été trouvé dans ces spectres et était le plus abondant après 24 heures.
2. Placé dans un bain d'eau chaude à 70°C.
3. Une fois le CBD dissous, 1,909 ml d'acide acétique glacial à 99 % ont été ajoutés à la solution, ce qui a donné une concentration finale de 5,2 % d'acide acétique.
4. Le mélange a été laissé à reflux pendant 24 heures au bain-marie à 70°C.
5. L'extraction de l'échantillon à 0 h a permis de trouver uniquement du CBD à 2,80 min, ce qui correspond aux échantillons de référence à 2,80. Après 1 h, les changements de l'isomérisation du CBD ont été constatés uniquement sous la forme d'une augmentation du pic à 3,77, que l'on pense être du D 11-THC ou du D 7-THC. Au bout de 4 heures, on a constaté une augmentation notable du pic du D 9-THC. Après 24 heures, la réaction a été analysée et a révélé que le 11-5 00 -dihydroxy-CBD, le 8-OH-iso-HHC, le CBD, le 10-méthoxy-THC et le D 9-THC ont été trouvés à 1,96 min, 2,22 min, 2,80 min, 3,50 min et 4,11 min, respectivement. Le composé à 3,77 min a été trouvé dans ces spectres et était le plus abondant après 24 heures.
Isomérisation du CBD avec le pTSA.
A une solution de CBD (1000g) dans 20L de CH2Cl2 anhydre (ou de toluène), le pTSA (500g) a été ajouté à température ambiante, sous atmosphère d'azote. La réaction a été agitée dans les mêmes conditions pendant 48h. Ensuite, le mélange a été dilué avec Et2O et lavé avec une solution saturée de NaHCO3. La couche organique a été collectée, lavée avec de la saumure, séchée sur Na2SO4 anhydre et concentrée. CH2Cl2 : rendement Δ8-THC ~940g ; Toluène : rendement Δ9-THC ~820g, Δ8-THC ~10g.
Isomérisation du CBD avec pTSA et MW.
Dans un récipient ouvert ont été ajoutés du CBD (500g), 1L d'hexane, et 15,22g de pTSA. La réaction a été irradiée dans un four à micro-ondes commercial modifié pendant 5 minutes (1200W). La température des réactions a été contrôlée à l'aide d'un thermomètre à perles à thermocouple tressé en téflon. Le mélange réactionnel a été versé dans une solution saturée de bicarbonate de sodium et extrait avec du dichlorométhane. La couche organique combinée a été lavée avec de la saumure, séchée sur Na2SO4 et évaporée sous vide. Rendement Δ8-THC ~393g ; Δ9-THC ~16g.
Isomérisation du CBD avec pTSA et SN.
Dans un récipient ouvert ont été ajoutés du CBD (500g), 1L de toluène, et 15,22g de pTSA. La réaction a été soniquée à l'aide d'un bain à ultrasons (40KHz) pendant 10 minutes à 60°C. . La température des réactions a été contrôlée à l'aide d'un thermomètre à perles à thermocouple tressé en téflon. Le mélange réactionnel a été versé dans une solution saturée de bicarbonate de sodium et extrait avec du dichlorométhane. La couche organique combinée a été lavée avec de la saumure, séchée sur Na2SO4 et évaporée sous vide. Rendement Δ8-THC ~352g ; Δ9-THC ~72g.
Last edited:
