G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,958
- Solutions
- 3
- Reaction score
- 3,327
- Points
- 113
- Deals
- 1
Introdução.
 Como é que a cromatografia em camada fina funciona?
Como é que a cromatografia em camada fina funciona?
 Preparação.
Preparação.
Realização do cromatograma.

Pegar num frasco de plástico ou de vidro, deitar 10-15 ml de água, 4-5 gotas de solução de álcool iodado. Agitar durante 7-10 minutos. Escoar a água. O iodo precipita-se na água nos lados do frasco. Colocar este frasco num recipiente.
Fator de retenção
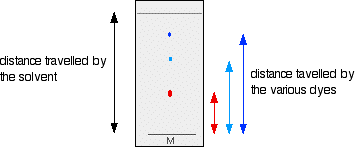
Após uma separação completa, os compostos individuais aparecem como manchas separadas verticalmente. Cada mancha tem um fator de retenção (Rf) que é igual à distância migrada sobre a distância total coberta pelo solvente. A fórmula de Rf é Rf= distância percorrida pela amostra/distância percorrida pelo solvente.
 O valor de Rf pode ser usado para identificar compostos devido à sua singularidade para cada composto. Quando se comparam dois compostos diferentes sob as mesmas condições, o composto com o valor Rf maior é menos polar porque não adere à fase estacionária durante tanto tempo como o composto polar, que teria um valor Rf mais baixo. Os valores Rf e a reprodutibilidade podem ser afectados por uma série de factores diferentes, como a espessura da camada, a humidade na placa TLC, a saturação do recipiente, a temperatura, a profundidade da fase móvel, a natureza da placa TLC, o tamanho da amostra e os parâmetros do solvente. Estes efeitos provocam normalmente um aumento dos valores de Rf. No entanto, no caso da espessura da camada, o valor Rf diminuiria porque a fase móvel se move mais lentamente na placa.
O valor de Rf pode ser usado para identificar compostos devido à sua singularidade para cada composto. Quando se comparam dois compostos diferentes sob as mesmas condições, o composto com o valor Rf maior é menos polar porque não adere à fase estacionária durante tanto tempo como o composto polar, que teria um valor Rf mais baixo. Os valores Rf e a reprodutibilidade podem ser afectados por uma série de factores diferentes, como a espessura da camada, a humidade na placa TLC, a saturação do recipiente, a temperatura, a profundidade da fase móvel, a natureza da placa TLC, o tamanho da amostra e os parâmetros do solvente. Estes efeitos provocam normalmente um aumento dos valores de Rf. No entanto, no caso da espessura da camada, o valor Rf diminuiria porque a fase móvel se move mais lentamente na placa.
Discussão dos resultados
Metanfetamina - 0,55
Mefedrona - 0,65
Conclusão.
A cromatografia é utilizada para separar misturas de substâncias nos seus componentes. Todas as formas de cromatografia funcionam segundo o mesmo princípio. Neste artigo, explicarei este método definindo o Rf da anfetamina, da metanfetamina e da mefedrona.
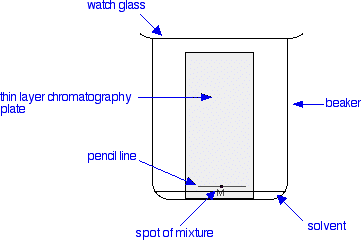
As placas de cromatografia têm uma fase estacionária (um sólido ou um líquido apoiado num sólido) e uma fase móvel (um líquido ou um gás). A fase móvel flui através da fase estacionária e transporta consigo os componentes da mistura. Os diferentes componentes deslocam-se a ritmos diferentes. Veremos as razões para este facto mais abaixo. A cromatografia de camada fina é feita exatamente como diz - utilizando uma camada fina e uniforme de sílica-gel ou alumina revestida num pedaço de vidro, metal ou plástico rígido. O gel de sílica (ou a alumina) é a fase estacionária. A fase estacionária para a cromatografia em camada fina também contém frequentemente uma substância que fluoresce à luz UV ou numa câmara de iodo - por razões que verá mais tarde. A fase móvel é um solvente líquido adequado ou uma mistura de solventes.
As placas de cromatografia têm uma fase estacionária (um sólido ou um líquido apoiado num sólido) e uma fase móvel (um líquido ou um gás). A fase móvel flui através da fase estacionária e transporta consigo os componentes da mistura. Os diferentes componentes deslocam-se a ritmos diferentes. Veremos as razões para este facto mais abaixo. A cromatografia de camada fina é feita exatamente como diz - utilizando uma camada fina e uniforme de sílica-gel ou alumina revestida num pedaço de vidro, metal ou plástico rígido. O gel de sílica (ou a alumina) é a fase estacionária. A fase estacionária para a cromatografia em camada fina também contém frequentemente uma substância que fluoresce à luz UV ou numa câmara de iodo - por razões que verá mais tarde. A fase móvel é um solvente líquido adequado ou uma mistura de solventes.
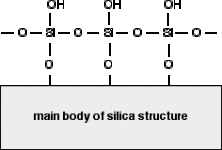
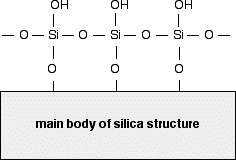
O gel de sílica é uma forma de dióxido de silício (sílica). Os átomos de silício estão unidos através de átomos de oxigénio numa estrutura covalente gigante. No entanto, na superfície do gel de sílica, os átomos de silício estão ligados a grupos -OH. Assim, na superfície do gel de sílica, existem ligações Si-O-H em vez de ligações Si-O-Si. O diagrama mostra uma pequena parte da superfície da sílica. A superfície do gel de sílica é muito polar e, devido aos grupos -OH, pode formar ligações de hidrogénio com compostos adequados à sua volta, bem como forças de dispersão de Van-der-Waals e atracções dipolo-dipolo.
Necessita de:
1. Seringa para 5 ml х 4
2. Frasco de plástico para análise da urina х 4
3. Recipientes de plástico grandes para comida (ou um copo grande e um recipiente de plástico) х 2
4. Placa TLC com camada de gel de sílica 5x10 cm (podes cortar uma grande com uma tesoura)
5. Solventes acetato de etilo, metanol, hexano (pode ser substituído por tetracloreto de carbono), solução aquosa de amoníaco a 10% ou superior, solução alcoólica de iodo
6. Lápis macio, régua e alicate
Não se esqueça das luvas e do respirador, faça a experiência numa sala ventilada.
1. Seringa para 5 ml х 4
2. Frasco de plástico para análise da urina х 4
3. Recipientes de plástico grandes para comida (ou um copo grande e um recipiente de plástico) х 2
4. Placa TLC com camada de gel de sílica 5x10 cm (podes cortar uma grande com uma tesoura)
5. Solventes acetato de etilo, metanol, hexano (pode ser substituído por tetracloreto de carbono), solução aquosa de amoníaco a 10% ou superior, solução alcoólica de iodo
6. Lápis macio, régua e alicate
Não se esqueça das luvas e do respirador, faça a experiência numa sala ventilada.
Realização do cromatograma.
1. Preparar uma solução fluente de acetato de etilo: metanol: amoníaco 85:10:5. Para 10 ml, é necessário tomar 8,5 ml de acetato de etilo, 1 ml de metanol e 0,5 ml de solução de amoníaco e misturar.
 2. Limpar a placa com gel de sílica com esta solução. Colocar a placa na solução, que deve ter 3-4 mm de profundidade num copo grande (como na figura 1). Pode utilizar uma pinça para uma manipulação confortável. Importante: não molhar a placa com água, pois esta estragar-se-á. A placa deve ser mantida na solução até que a parte da frente do solvente atinja o bordo superior da placa.
2. Limpar a placa com gel de sílica com esta solução. Colocar a placa na solução, que deve ter 3-4 mm de profundidade num copo grande (como na figura 1). Pode utilizar uma pinça para uma manipulação confortável. Importante: não molhar a placa com água, pois esta estragar-se-á. A placa deve ser mantida na solução até que a parte da frente do solvente atinja o bordo superior da placa.
3. Vamos começar com um caso simples. Existem quatro substâncias: anfetamina(A), metanfetamina(L), cafeína(K) e mefedrona(M).
Para esta experiência, é necessário obter uma base livre de drogas. Colocar 10-15 mg da amostra (alguns grumos) num frasco de vidro (plástico), purgar duas gotas de solução aquosa de amoníaco. Em seguida, deitar 3-4 gotas de hexano ou tetracloreto de carbono e agitar durante um minuto. A base livre do medicamento é diluída na camada orgânica.4. Agora é preciso colocá-la na placa cromatográfica, que foi preparada anteriormente. Pega numa agulha de uma seringa e corta-a com um alicate, como no exemplo. Tens de obter uma extremidade plana.




 Pega numa placa limpa e seca e desenha uma linha a lápis ~5-6 mm acima do bordo inferior. Qualquer marcação na placa para mostrar a posição original da gota também deve ser feita a lápis. Se tudo isto tiver sido feito com tinta, os corantes da tinta também se deslocarão com a evolução do cromatograma. Marcar quatro pontos a igual distância entre si. Mergulhar a extremidade da agulha cortada na camada orgânica da solução do primeiro narcótico. Tocar na placa com a ponta da agulha e fazer uma pequena mancha com 3-4 mm de diâmetro, esperar que seque e repetir o procedimento 10 vezes. Repetir as etapas 2 e 3 para outras substâncias.
Pega numa placa limpa e seca e desenha uma linha a lápis ~5-6 mm acima do bordo inferior. Qualquer marcação na placa para mostrar a posição original da gota também deve ser feita a lápis. Se tudo isto tiver sido feito com tinta, os corantes da tinta também se deslocarão com a evolução do cromatograma. Marcar quatro pontos a igual distância entre si. Mergulhar a extremidade da agulha cortada na camada orgânica da solução do primeiro narcótico. Tocar na placa com a ponta da agulha e fazer uma pequena mancha com 3-4 mm de diâmetro, esperar que seque e repetir o procedimento 10 vezes. Repetir as etapas 2 e 3 para outras substâncias.
Erro comum: não fazer uma grande mancha de gordura, porque a substância pode sobrepor-se a outras substâncias durante a experiência.
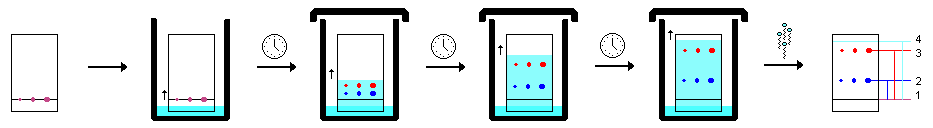
5. Quando as manchas de bases livres estiverem secas, a placa é colocada numa camada pouco profunda de solvente num copo tapado. É importante que o nível do solvente esteja abaixo da linha com a mancha. Esperar até que a linha frontal do solvente atinja 4-5 mm antes do bordo superior da placa e retirá-la. Depois, desenhar uma linha a lápis na linha da frente do solvente. Secar ao ar.

 6. O cromatograma é colocado num recipiente fechado (como outro copo coberto com um vidro de relógio ou grandes recipientes de plástico) juntamente com alguns cristais de iodo. O vapor de iodo contido no recipiente reage com as manchas do cromatograma. As substâncias que lhe interessam podem aparecer como manchas coloridas. Trace-as com um lápis e desenhe pontos no centro de cada mancha.
6. O cromatograma é colocado num recipiente fechado (como outro copo coberto com um vidro de relógio ou grandes recipientes de plástico) juntamente com alguns cristais de iodo. O vapor de iodo contido no recipiente reage com as manchas do cromatograma. As substâncias que lhe interessam podem aparecer como manchas coloridas. Trace-as com um lápis e desenhe pontos no centro de cada mancha.
 Também podes usar uma lâmpada UV com comprimento de onda de 254 e 365 nm.
Também podes usar uma lâmpada UV com comprimento de onda de 254 e 365 nm.

Como preparar a câmara de iodo.Erro comum: não fazer uma grande mancha de gordura, porque a substância pode sobrepor-se a outras substâncias durante a experiência.
5. Quando as manchas de bases livres estiverem secas, a placa é colocada numa camada pouco profunda de solvente num copo tapado. É importante que o nível do solvente esteja abaixo da linha com a mancha. Esperar até que a linha frontal do solvente atinja 4-5 mm antes do bordo superior da placa e retirá-la. Depois, desenhar uma linha a lápis na linha da frente do solvente. Secar ao ar.
Pegar num frasco de plástico ou de vidro, deitar 10-15 ml de água, 4-5 gotas de solução de álcool iodado. Agitar durante 7-10 minutos. Escoar a água. O iodo precipita-se na água nos lados do frasco. Colocar este frasco num recipiente.
Fator de retenção
Após uma separação completa, os compostos individuais aparecem como manchas separadas verticalmente. Cada mancha tem um fator de retenção (Rf) que é igual à distância migrada sobre a distância total coberta pelo solvente. A fórmula de Rf é Rf= distância percorrida pela amostra/distância percorrida pelo solvente.
Na experiência, obtive três manchas em vez das quatro esperadas. A repetição da experiência mostra que a cafeína não é eluída por uma solução de cetato de etilo:metanol:amoníaco 85:10:5. Foi aprovado experimentalmente que esta solução é adequada para eluir drogas como a anfetamina, a metanfetamina e a mefedrona.
 Rf das drogas estudadas.
Rf das drogas estudadas.
Anfetamina - 0,53Metanfetamina - 0,55
Mefedrona - 0,65
Explicação.
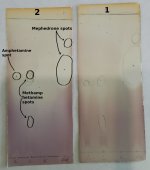
Tenho duas placas com resultados. Duas distâncias medidas entre o ponto inicial e o meio da mancha circundada. Na primeira placa, o ponto da anfetamina estava a 42 mm e, na segunda, a 49 mm da linha de partida, enquanto a linha da frente do solvente estava a 85 e 86 mm, respetivamente. Rf1=42/85=0.49, Rf2=49/86=0.52. Depois calculei a média aritmética 0,53. Os mesmos cálculos foram efectuados para as outras substâncias.
Tenho duas placas com resultados. Duas distâncias medidas entre o ponto inicial e o meio da mancha circundada. Na primeira placa, o ponto da anfetamina estava a 42 mm e, na segunda, a 49 mm da linha de partida, enquanto a linha da frente do solvente estava a 85 e 86 mm, respetivamente. Rf1=42/85=0.49, Rf2=49/86=0.52. Depois calculei a média aritmética 0,53. Os mesmos cálculos foram efectuados para as outras substâncias.
Conclusão.
Como mostra a experiência, pode medir o Rf do seu medicamento e comparar com uma substância conhecida numa mesma placa. Fazer uma mancha da base livre do medicamento e 1-4 manchas de outros medicamentos para verificar o Rf. Se as manchas estiverem à mesma distância da linha de partida, então provavelmente trata-se da mesma substância. Além disso, se obtiver vários pontos da sua droga, provavelmente tem uma mistura de substâncias. Algumas drogas têm várias manchas porque são uma mistura de droga e subprodutos da síntese. No entanto, pode compará-los com outros medicamentos utilizando a cromatografia em camada fina.
Attachments
Last edited by a moderator: