William D.
Expert
- Joined
- Jul 19, 2021
- Messages
- 1,045
- Reaction score
- 1,284
- Points
- 113
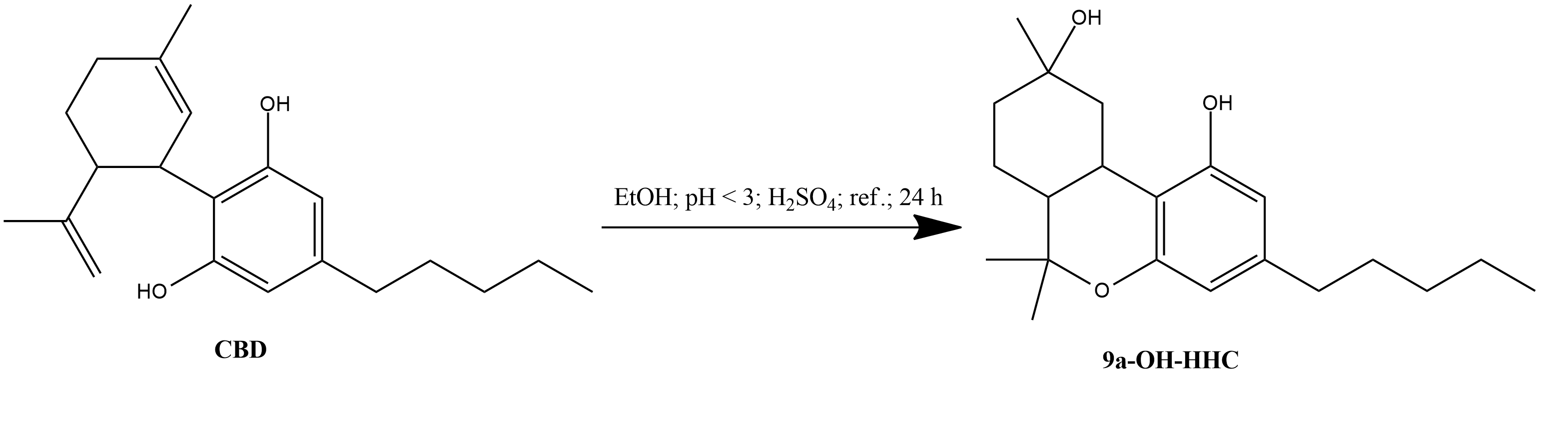
Com Battery acid
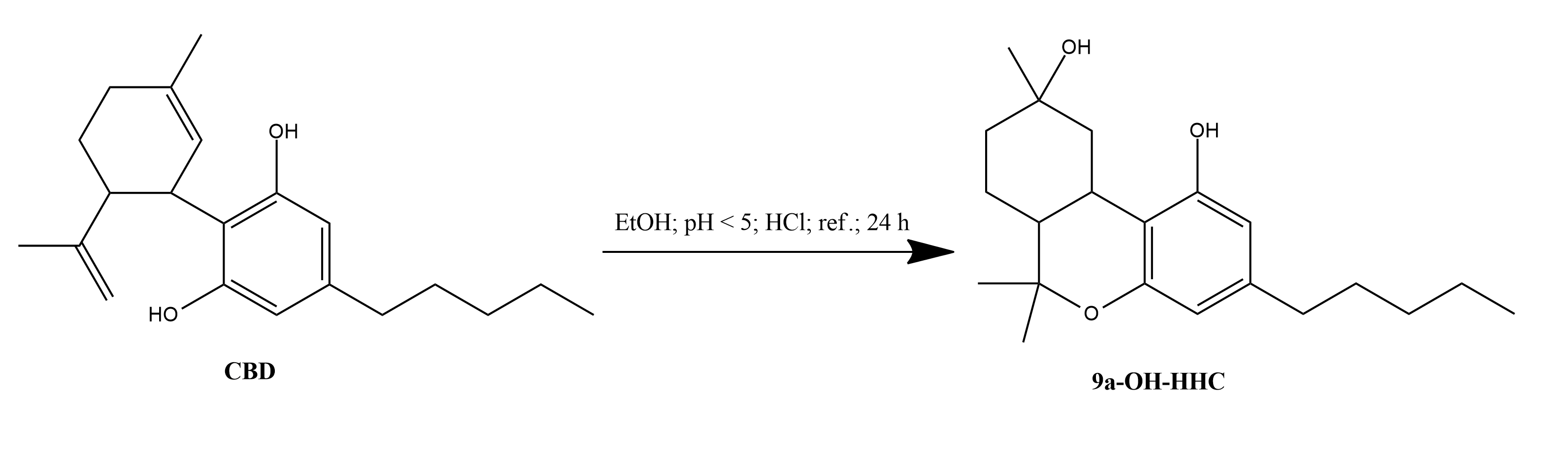
Com ácido muriático
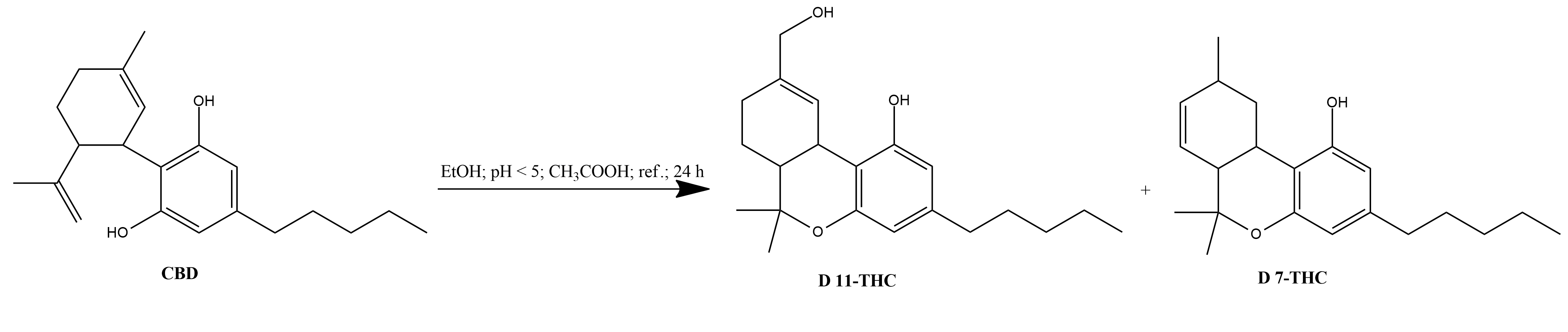
Com ácido acético glacial
Isomerização do CBD com pTSA.
A uma solução de CBD (1000g) em 20L de CH2Cl2 anidro (ou tolueno), adicionou-se pTSA (500g) à temperatura ambiente, sob atmosfera de azoto. A reação foi agitada nas mesmas condições durante 48 horas. Em seguida, a mistura foi diluída com Et2O e lavada com uma solução saturada de NaHCO3. A camada orgânica foi recolhida, lavada com salmoura, seca sobre Na2SO4 anidro e concentrada. CH2Cl2: rendimento de Δ8-THC ~940g; Tolueno: rendimento de Δ9-THC ~820g, Δ8-THC ~10g.
Isomerização do CBD com pTSA e MW.
A um recipiente aberto foi adicionado CBD (500g), 1L de hexano e 15,22g de pTSA. A reação foi irradiada num forno de micro-ondas comercial modificado durante 5 min (1200W). A temperatura das reacções foi monitorizada utilizando um termómetro com termopar entrançado de Teflon. A mistura reacional foi vertida numa solução saturada de bicarbonato de sódio e extraída com diclorometano. A camada orgânica combinada foi lavada com salmoura, seca sobre Na2SO4 e evaporada sob vácuo. Rendimento Δ8-THC ~393g; Δ9-THC ~16g.
Isomerização do CBD com pTSA e SN.
A um recipiente aberto foi adicionado CBD (500g), 1L de tolueno e 15,22g de pTSA. A reação foi sonicada utilizando um banho de ultra-sons (40KHz) durante 10 minutos a 60°C. . A temperatura das reacções foi monitorizada utilizando um termómetro de termopar entrançado em Teflon. A mistura reacional foi vertida para uma solução saturada de bicarbonato de sódio e extraída com diclorometano. A camada orgânica combinada foi lavada com salmoura, seca sobre Na2SO4 e evaporada sob vácuo. Rendimento Δ8-THC ~352g; Δ9-THC ~72g.
1. 1 g de CBD foi adicionado a 35 ml de etanol a 95% num balão de fundo redondo (RBF) de 50 ml.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionadas 4 gotas de ácido sulfúrico a 35% para acidificar a solução, pH < 3.
4. Deixou-se a mistura refluir durante 24 h no banho de água a 70°C.
5. Uma vez terminado, foram utilizadas 5 gotas de NaOH 10M para basificar a solução até que o pH fosse superior a 10, o que remove o ácido sulfúrico como sulfato de sódio.
6. A reação foi então filtrada para remover o sulfato de sódio, o que permitiu que apenas os canabinóides estivessem na solução de etanol restante.
7. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado a 2,80 min, o que está de acordo com as amostras de referência de 2,80 min. Após 1 hora, o pico de CBD foi reduzido, mas ainda era o pico principal presente. No entanto, outras impurezas começaram a aumentar após 24 h, como em 2,18 min e 3,40 min, que se verificou serem 8-OH-iso-HHC e 9α-OH-HHC. Além disso, o dupleto D 9-THC e D 8-THC foi encontrado aos 4,10 min e 4,22 min. Outro pico em 3,77 min foi encontrado como um pico de isomerização de D 9-THC e pensa-se que seja D 11-THC ou D 7-THC. Este método não isomerizou todo o CBD mesmo às 24 h. No entanto, o pico do CBD já não era o pico mais proeminente na amostra. O maior pico encontrado foi o de 3,38 picos, que era 9α-OH-HHC.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionadas 4 gotas de ácido sulfúrico a 35% para acidificar a solução, pH < 3.
4. Deixou-se a mistura refluir durante 24 h no banho de água a 70°C.
5. Uma vez terminado, foram utilizadas 5 gotas de NaOH 10M para basificar a solução até que o pH fosse superior a 10, o que remove o ácido sulfúrico como sulfato de sódio.
6. A reação foi então filtrada para remover o sulfato de sódio, o que permitiu que apenas os canabinóides estivessem na solução de etanol restante.
7. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado a 2,80 min, o que está de acordo com as amostras de referência de 2,80 min. Após 1 hora, o pico de CBD foi reduzido, mas ainda era o pico principal presente. No entanto, outras impurezas começaram a aumentar após 24 h, como em 2,18 min e 3,40 min, que se verificou serem 8-OH-iso-HHC e 9α-OH-HHC. Além disso, o dupleto D 9-THC e D 8-THC foi encontrado aos 4,10 min e 4,22 min. Outro pico em 3,77 min foi encontrado como um pico de isomerização de D 9-THC e pensa-se que seja D 11-THC ou D 7-THC. Este método não isomerizou todo o CBD mesmo às 24 h. No entanto, o pico do CBD já não era o pico mais proeminente na amostra. O maior pico encontrado foi o de 3,38 picos, que era 9α-OH-HHC.
Com ácido muriático
1. 1 g de CBD foi adicionado a 35 ml de etanol a 95% num RBF de 50 ml.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionados 47,3 ml de ácido clorídrico a 37% à solução, obtendo-se uma concentração final de 0,05% de HCl com um pH inferior a 5.
4. A mistura foi deixada em refluxo durante 24 h num banho de água a 70°C.
5. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado a 2,80 min, o que está de acordo com as amostras de referência de 2,80 min. Após 1 hora, o pico do CBD diminuiu, mas ainda era o principal pico presente. No entanto, outras impurezas começaram a aumentar após 24 h, como em 2,18 min e 3,40 min, que se verificou serem 8-OH-iso-HHC e 9α-OH-HHC. Além disso, o dupleto D 9-THC e D 8-THC foi encontrado aos 4,10 min e 4,22 min. Outro pico a 3,77 min foi considerado um pico de isomerização de D 9-THC e pensa-se que seja D 11-THC ou D 7-THC. A fragmentação foi efectuada e verificou-se que apresenta a mesma fragmentação e proporções que o D 9-THC e o D 8-THC, confirmando que se trata de um isómero do D 9-THC e do D 8-THC. Este método não isomerizou todo o CBD mesmo às 24 h. No entanto, o pico do CBD já não era o pico mais proeminente na amostra. O maior pico encontrado foi o de 3,38 picos, que era 9α-OH-HHC.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionados 47,3 ml de ácido clorídrico a 37% à solução, obtendo-se uma concentração final de 0,05% de HCl com um pH inferior a 5.
4. A mistura foi deixada em refluxo durante 24 h num banho de água a 70°C.
5. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado a 2,80 min, o que está de acordo com as amostras de referência de 2,80 min. Após 1 hora, o pico do CBD diminuiu, mas ainda era o principal pico presente. No entanto, outras impurezas começaram a aumentar após 24 h, como em 2,18 min e 3,40 min, que se verificou serem 8-OH-iso-HHC e 9α-OH-HHC. Além disso, o dupleto D 9-THC e D 8-THC foi encontrado aos 4,10 min e 4,22 min. Outro pico a 3,77 min foi considerado um pico de isomerização de D 9-THC e pensa-se que seja D 11-THC ou D 7-THC. A fragmentação foi efectuada e verificou-se que apresenta a mesma fragmentação e proporções que o D 9-THC e o D 8-THC, confirmando que se trata de um isómero do D 9-THC e do D 8-THC. Este método não isomerizou todo o CBD mesmo às 24 h. No entanto, o pico do CBD já não era o pico mais proeminente na amostra. O maior pico encontrado foi o de 3,38 picos, que era 9α-OH-HHC.
Com ácido acético glacial
1. 1 g de CBD foi adicionado a 35 ml de etanol a 95% num RBF de 50 ml.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionados à solução 1,909 ml de ácido acético glacial a 99%, obtendo-se uma concentração final de 5,2% de ácido acético.
4. A mistura foi deixada em refluxo durante 24 h num banho de água a 70°C.
5. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado aos 2,80 min, o que está de acordo com as amostras de referência de 2,80. Após 1 h, as alterações de isomerização do CBD só foram encontradas como um aumento do pico a 3,77, que se pensa ser D 11-THC ou D 7-THC. Após 4 horas, verificou-se um pico notável de aumento de D 9-THC. Às 24 h, a reação foi analisada e verificou-se que 11-5 00 -dihidroxi-CBD, 8-OH-iso-HHC, CBD, 10-metoxi-THC e D 9-THC foram encontrados a 1,96 min, 2,22 min, 2,80 min, 3,50 min e 4,11 min, respetivamente. O composto a 3,77 min foi encontrado nestes espectros e foi o mais abundante após 24 h.
2. Colocado num banho de água quente a 70°C.
3. Uma vez dissolvido o CBD, foram adicionados à solução 1,909 ml de ácido acético glacial a 99%, obtendo-se uma concentração final de 5,2% de ácido acético.
4. A mistura foi deixada em refluxo durante 24 h num banho de água a 70°C.
5. A extração da amostra de 0 h resultou em que apenas o CBD foi encontrado aos 2,80 min, o que está de acordo com as amostras de referência de 2,80. Após 1 h, as alterações de isomerização do CBD só foram encontradas como um aumento do pico a 3,77, que se pensa ser D 11-THC ou D 7-THC. Após 4 horas, verificou-se um pico notável de aumento de D 9-THC. Às 24 h, a reação foi analisada e verificou-se que 11-5 00 -dihidroxi-CBD, 8-OH-iso-HHC, CBD, 10-metoxi-THC e D 9-THC foram encontrados a 1,96 min, 2,22 min, 2,80 min, 3,50 min e 4,11 min, respetivamente. O composto a 3,77 min foi encontrado nestes espectros e foi o mais abundante após 24 h.
Isomerização do CBD com pTSA.
A uma solução de CBD (1000g) em 20L de CH2Cl2 anidro (ou tolueno), adicionou-se pTSA (500g) à temperatura ambiente, sob atmosfera de azoto. A reação foi agitada nas mesmas condições durante 48 horas. Em seguida, a mistura foi diluída com Et2O e lavada com uma solução saturada de NaHCO3. A camada orgânica foi recolhida, lavada com salmoura, seca sobre Na2SO4 anidro e concentrada. CH2Cl2: rendimento de Δ8-THC ~940g; Tolueno: rendimento de Δ9-THC ~820g, Δ8-THC ~10g.
Isomerização do CBD com pTSA e MW.
A um recipiente aberto foi adicionado CBD (500g), 1L de hexano e 15,22g de pTSA. A reação foi irradiada num forno de micro-ondas comercial modificado durante 5 min (1200W). A temperatura das reacções foi monitorizada utilizando um termómetro com termopar entrançado de Teflon. A mistura reacional foi vertida numa solução saturada de bicarbonato de sódio e extraída com diclorometano. A camada orgânica combinada foi lavada com salmoura, seca sobre Na2SO4 e evaporada sob vácuo. Rendimento Δ8-THC ~393g; Δ9-THC ~16g.
Isomerização do CBD com pTSA e SN.
A um recipiente aberto foi adicionado CBD (500g), 1L de tolueno e 15,22g de pTSA. A reação foi sonicada utilizando um banho de ultra-sons (40KHz) durante 10 minutos a 60°C. . A temperatura das reacções foi monitorizada utilizando um termómetro de termopar entrançado em Teflon. A mistura reacional foi vertida para uma solução saturada de bicarbonato de sódio e extraída com diclorometano. A camada orgânica combinada foi lavada com salmoura, seca sobre Na2SO4 e evaporada sob vácuo. Rendimento Δ8-THC ~352g; Δ9-THC ~72g.
Last edited:
