Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 290
- Reaction score
- 327
- Points
- 63
AM-2201 (1-(5-Fluoropentyl)-[1H-indol-3-yl]-(naphthalen-1-yl)-methanone é um canabinóide sintético, que foi inicialmente criado em 2000 como uma ferramenta farmacológica para estudar o sistema endocanabinóide. É um potente agonista completo dos receptores canabinóides (CB1R), que provoca efeitos psicoactivos semelhantes aos do fitocanabinóide Δ9-tetrahidrocanabinol (THC), mas a sua afinidade de ligação é 40 vezes superior à do THC. Do mesmo modo, a afinidade de ligação do АМ-2201 aos receptores canabinóides de tipo 2 (CB2R), responsáveis pelos efeitos periféricos mediados por canabinóides, é 14 vezes superior à do THC. A forma mais comum de administração é fumar, e as doses típicas de AM-2201 variam entre 250 ug e 2 mg. Em regra, o AM-2201 faz parte das seguintes substâncias: "Spice", "K2", "erva legal", "canábis sintética", "incenso de ervas". Além disso, na Alemanha, descobriu-se que era um aditivo de mais de 90 marcas diferentes de "misturas de ervas", que incluíam: Agent Orange", "Atomic Bomb", "Green", "Jamaican Gold Extreme", "Manga Xtreme", "New Bonzai" e "XoXo". A Drug Abuse Warning Network (DAWN) regista cerca de 15 mil visitas aos serviços de urgência associadas ao abuso de canabinóides sintéticos. Os metabolitos do AM-2201 foram identificados em cerca de 60% das amostras de sangue. Durante o aquecimento (por exemplo, enquanto se fuma), o AM-2201 pode ser transformado em JWH-018 em pequena escala. O JWH-018 foi um dos primeiros canabinóides sintéticos, incluído em várias legislações nacionais relativas ao controlo de drogas. No entanto, o AM-2201 não é considerado um precursor direto de qualquer substância controlada internacionalmente. O AM-2201 é um naftoilindole, alquilado no azoto do indol e com um átomo de flúor na posição 5 da cadeia lateral do pentilo. Do ponto de vista da química básica, pode ser considerado relativamente inerte, uma vez que é substituído pelo motivo naftoilindol numa posição recreativa C-3. Devido à aromaticidade do sistema indol, o azoto não conduz a um aumento da "basicidade". Ao contrário dos seus análogos não fluorados, pode transformar-se em JWH-018 e JWH-022 a temperaturas mais elevadas, em pequena escala. O perfil analítico desta substância é descrito em muitos documentos diferentes e os métodos utilizados incluem LC-MS/MS, GC-EI-MS, LC-Q-ToF-MS, AccuTOF-DART, NMR, FTIR ATR e deteção UV-VIS. Pode ser detectado no soro, no sangue total, no cabelo, no fluido oral e, nas amostras de urina, o principal alvo analítico são os seus principais metabolitos.
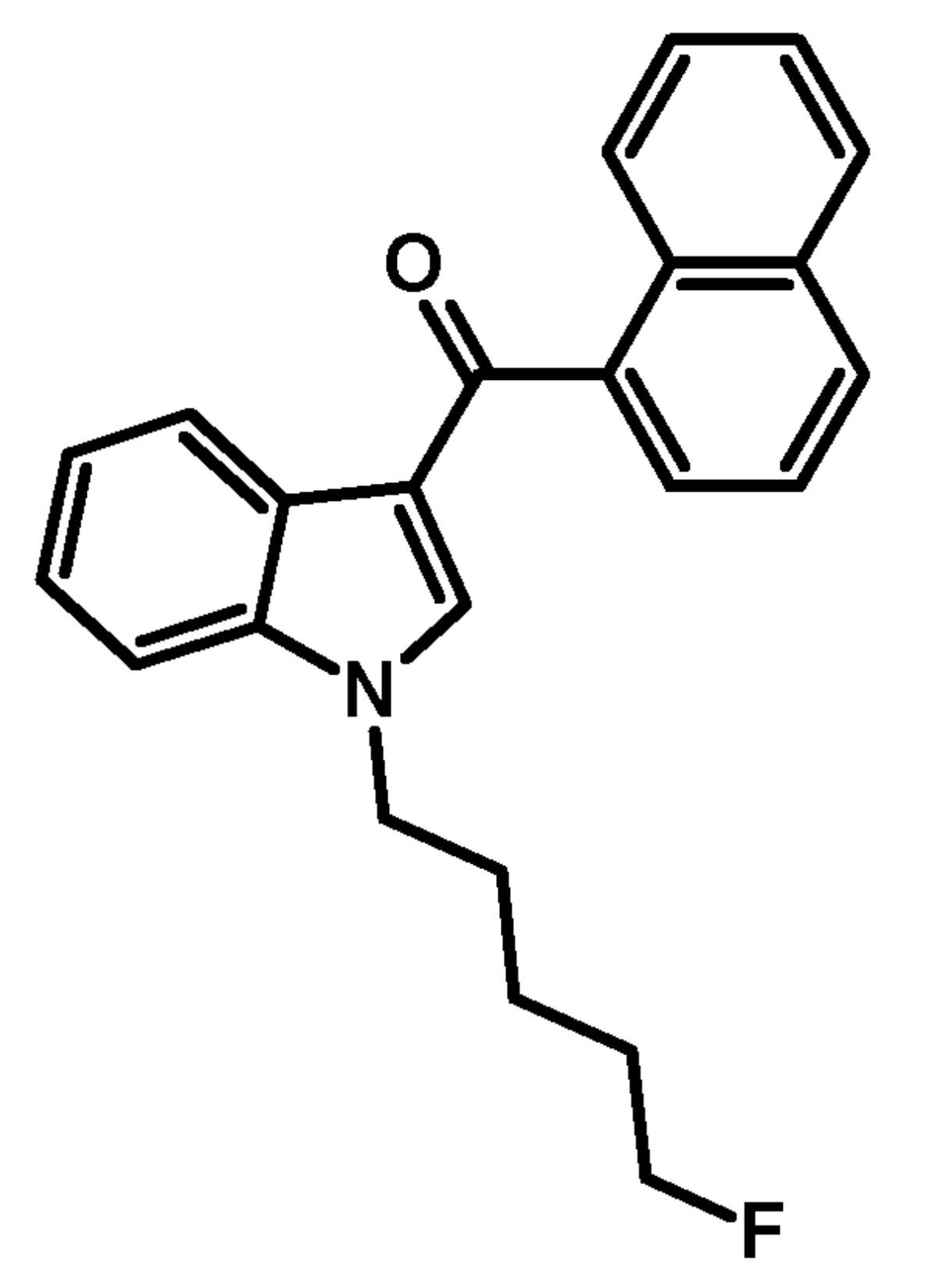
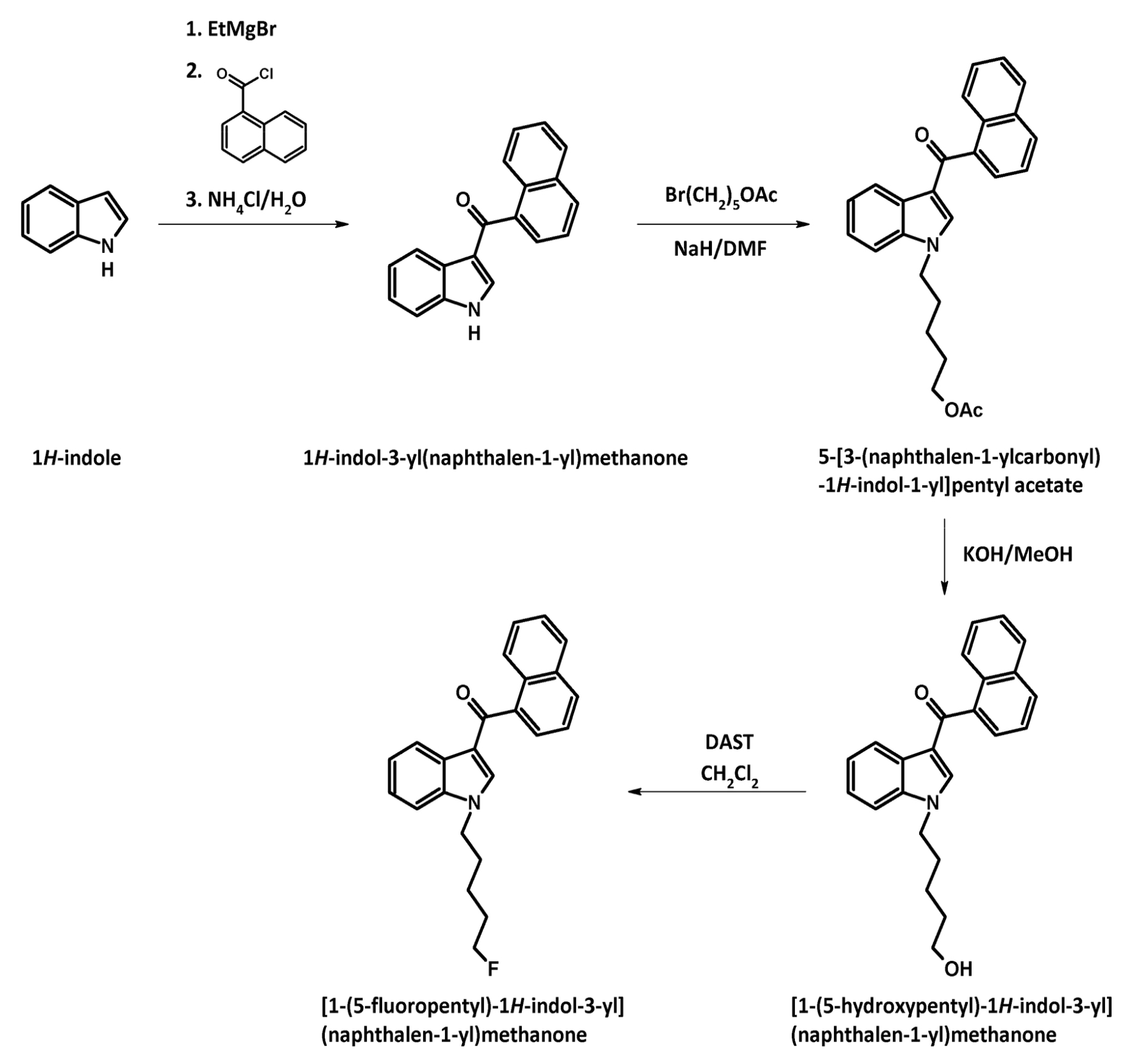
A substância em si tem o aspeto de um sólido cristalino branco (na forma pura), solúvel em etanol (5 mg/ml). Tem uma fórmula molecular C24H22FNO, peso molecular 359,43 g/mol, ponto de fusão 93,7 °C. O ponto de ebulição da substância é indeterminado. A síntese do АМ-2201 foi descrita pela primeira vez em 2001 por Alexandros Makriyannis e Hongfeng Deng. Começa com uma solução de 1-H indole no éter etílico do ácido acético, é adicionada uma solução de brometo de metil magnésio no éter etílico do ácido acético. Em seguida, adiciona-se cloreto de naftaleno-1-carbonilo (preparado a partir de ácido naftaleno-1-carboxílico e cloreto de tionilo) e, finalmente, uma solução aquosa de cloreto de amónio. Em seguida, o filtrado resultante da 1H-indol-3-il(naftaleno-1-il)metanona é lavado e recristalizado. Este produto é adicionado à suspensão de hidreto de sódio em dimetilformamida (DMF) e, em seguida, adiciona-se 5-bromopentilacetato para a N-alquilação. Após a clivagem do acetato por solução de hidróxido de potássio em metanol, procede-se à fluorização da cadeia lateral do pentilo utilizando trifluoreto de dietilaminossulfureto (DAST) e diclorometano.



Farmacocinética e farmacodinâmica do АМ-2201.
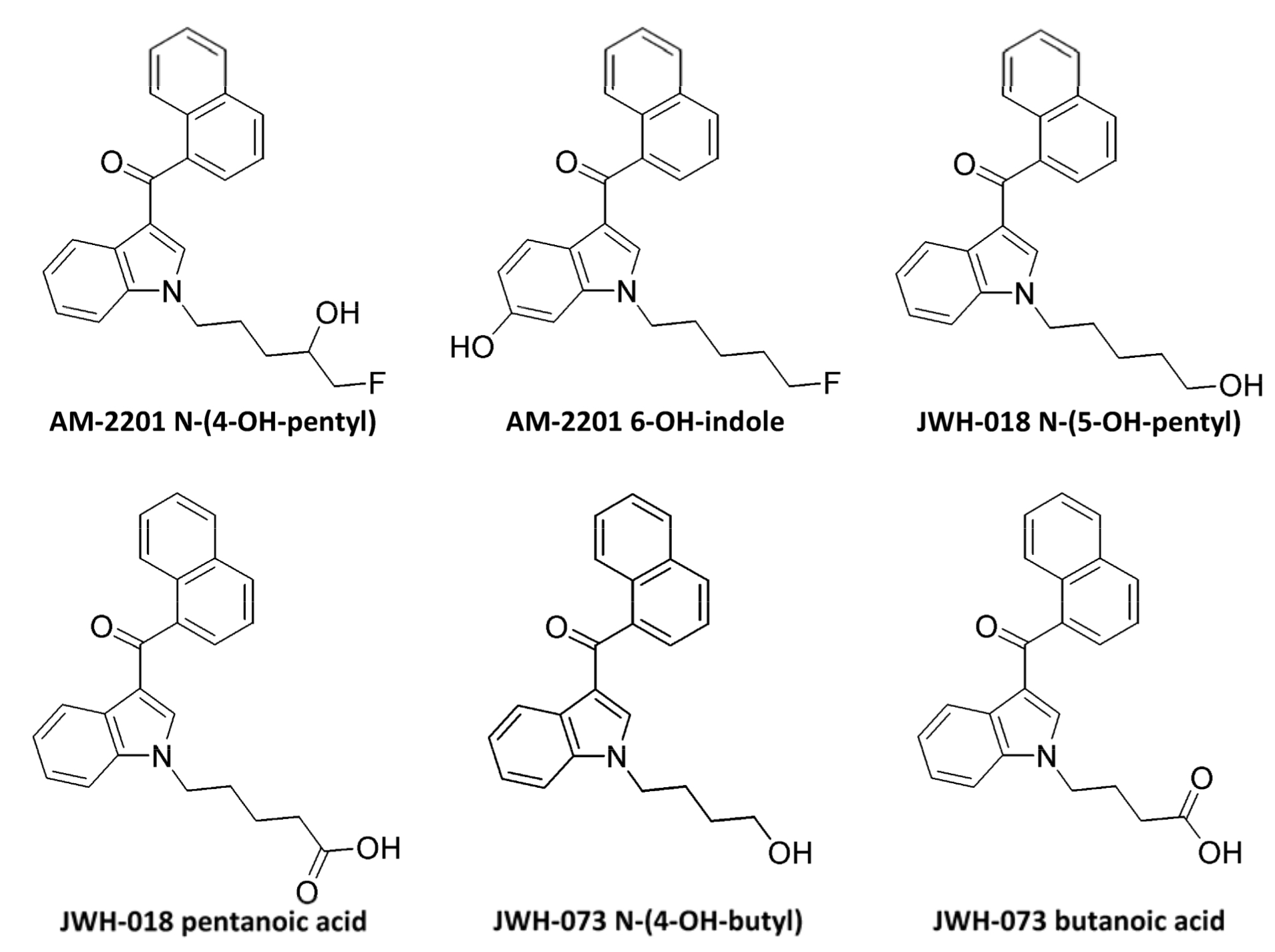
O АМ-2201 é metabolizado por várias enzimas da família CYP450. Em estudos com microssomas hepáticos humanos (HLM) e com proteína humana recombinante, identificou-se que CYP2C9 e CYP1A2 são as principais enzimas envolvidas na oxidação de АМ-2201, enquanto CYP2C19, 2D6, 2E1 e 3A4 têm um papel insignificante nesta fase do metabolismo. Além das reações metabólicas, o AM-2201 sofre defluoração enzimática, que se presume estar na presença do citocromo Р450 2Е1. Foi também revelado que os CYP1A2, 2C9 e 2C19 medeiam a desfluoração oxidativa. Em estudos in vitro e in vivo, a diferença entre JWH-018 e А-2201 foi revelada. Assim, JWH-018 N- (4OH-pentyl) é formado exclusivamente após a absorção de JWH-018, por isso pode ser usado como um marcador de diagnóstico para diferenciar entre a absorção de JWH-018 e AM-2201. Os principais metabolitos incluem: AM-2201 N-(4-OH-pentil), AM-2201 6-OH-indole, JWH-018 N-(5-OH-pentil), ácido pentanóico JWH-018, JWH-073 N-(4- OH-butil) e ácido butanóico JWH-073. A conjugação com o ácido glucurónico é realizada por várias UDP-glucuronosiltranseferases, principalmente hepáticas (UGT1A1, UGT1A9 e UGT2B7) e enzimas, incluindo: JWH-018 N-(5-OH-pentil), JWH-018 ácido pentanóico, JWH-073 N-(4-OH-butil), bem como JWH-073 ácido butanóico.
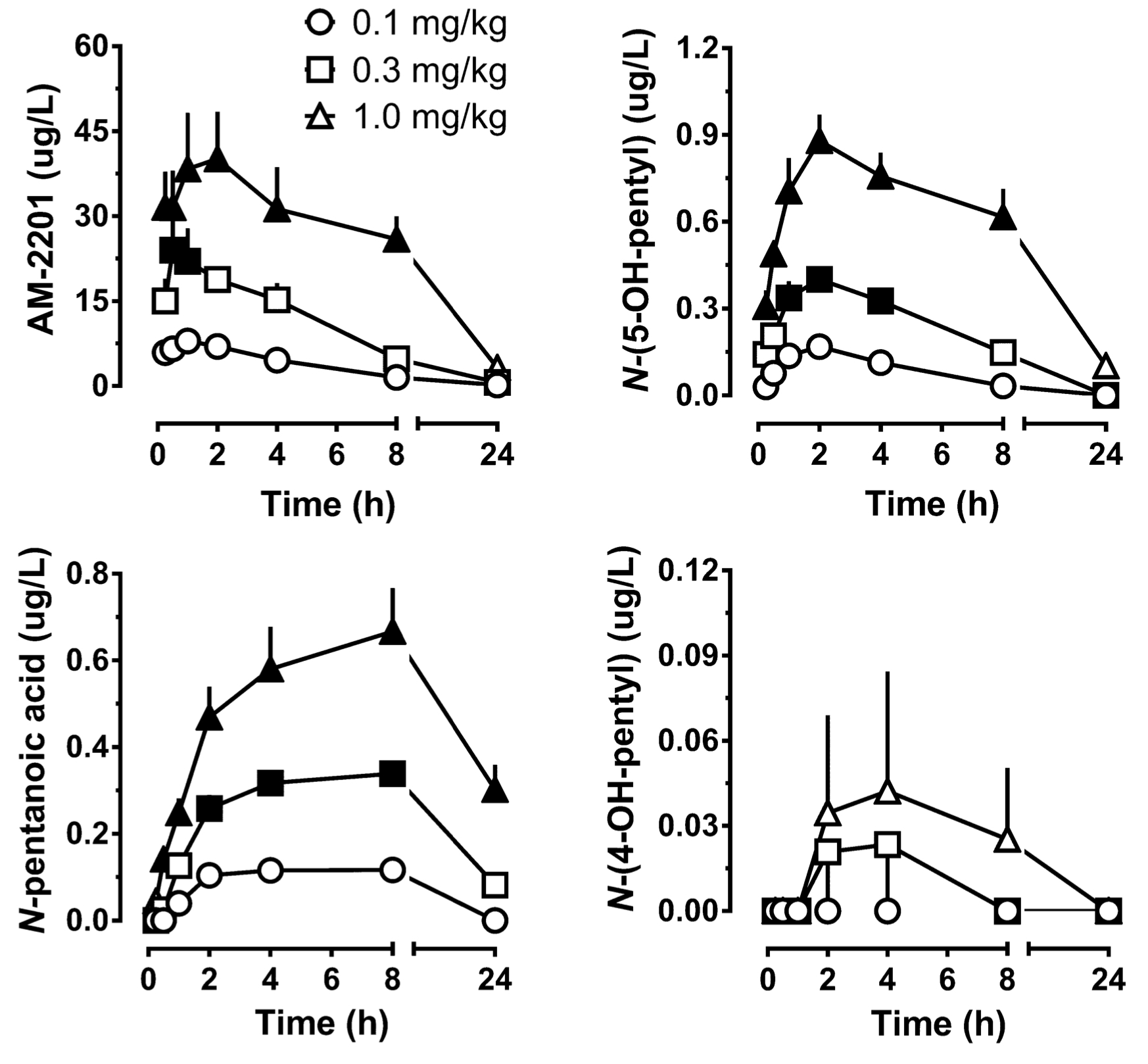
Quanto às constantes farmacológicas, após a administração de 5 mg de АМ-2201, a concentração máxima no soro com um indicador de 0,56 n/ml é detectada após 1 hora e 35 minutos, e continua a ser detetável no soro durante os cinco dias seguintes (com limite de deteção de 0,8 pg/ml). Este facto indica uma semi-vida de vários dias. Nos estudos de Carlier sobre o metabolismo do AM-2201 em ratos, foram determinados perfis de concentração temporal no plasma, que dependiam significativamente da dose e do tempo, enquanto a concentração aumentava linearmente à medida que a dose aumentava. Assim, após a administração de AM-2201 numa dose de 0,3 mg/kg, a concentração foi significativamente mais elevada do que após a administração de 0,1 mg/kg, embora fosse detetável no plasma mesmo após 4 horas com um indicador de 3,22 μg/L. O tempo máximo para a concentração máxima foi de 1,3 horas, e não dependeu da dose administrada. No entanto, a semi-vida de eliminação dependeu da dose administrada. O tempo para a concentração máxima do metabolito WH-018 N-(5-hidroxipentilo) foi de 2 horas, e o metabolito pôde ser detectado mesmo após 24 horas. Em 2013, Hutter relatou o primeiro estudo farmacocinético do AM-2201 em seres humanos, que se baseou na ingestão única da substância numa dose de 0,07 mg/kg. Em seu estudo, a concentração de AM-2201 no plasma caiu para 0,6 a <0,02 μg / L (LOQ) em 1,5-125 horas após a administração. Apenas 4 metabolitos foram identificados no soro: JWH-018 ácido N-pentanóico, JWH-018 N-(5-hidroxipentil), AM-2201 6'-hidroxiindol e AM-2201 N-(4-hidroxipentil). É importante notar que as concentrações séricas do ácido N-pentanóico do JWH-018 excederam as do АМ-2201 em todas as amostras. As concentrações máximas de JWH-018 N-(5-hidroxipentilo) e de ácido JWH-018 N-pentanóico foram registadas após 1,5 e 4,1 horas desde a administração da substância, respetivamente. O ácido N-pentanóico do JWH-018 foi detetável até 57 horas após a ingestão. Os diferentes indicadores nos ratos e nos seres humanos resultam, presumivelmente, de diferenças interespecíficas e de diferenças nas formas de administração. Assim, após a administração oral do AM-2201, o metabolismo gastrointestinal foi mais significativo do que a via sc, que é uma forma de contornar esta via metabólica. A concentração de AM-2201 no sangue em casos humanos não excedeu 5 μg/L.
Ainda não foram revelados dados sobre a farmacodinâmica da substância in vivo. No entanto, sabe-se que tem uma elevada afinidade de ligação aos receptores canabinóides de primeiro tipo, expressa em IC50 (ocupação de 50% dos receptores) - 1,0 nM e aos receptores canabinóides de segundo tipo - 2,6 nM, em comparação com a afinidade do delta-9 tetrahidrocanabinol (THC) - 40,7 nM para os receptores CB1- e 36,4 nM para os receptores CB2. Além disso, em estudos in vitro com análise de ligação de [35S] guanosina-5'-O-(3-thio)-trifosfato ([35S]GTPγS), a concentração efectiva de 50% (EC50) é determinada em 0,24 nM com propriedades agonísticas completas da substância em termos de receptores. Com base nestes dados e em observações clínicas, pode presumir-se que o AM-2201 apresenta efeitos típicos dos agonistas CB1. Estes efeitos podem incluir sedação, disfunção cognitiva, taquicardia, hipotensão postural, boca seca, ataxia, imunossupressão e efeitos psicotrópicos. Uma diferença acentuada em relação ao THC é a formação de metabolitos potencialmente farmacologicamente activos pelo AM-2201. No caso do THC, sabe-se que apenas um dos principais metabolitos tem propriedades psicoactivas e preserva a afinidade de ligação aos receptores canabinóides (11-OH-THC: Ki no recetor CB1: 38,4 ± 0,8 nM). Alguns metabolitos do AM-2201 preservam uma elevada afinidade de ligação ao recetor CB1 com uma classificação relativa de ligação AM-2201 > AM-2201 N-(4-OH-pentyl) = JWH-018 N-(5-OH- pentyl) > THC > JWH-073 N-(4-OH-butyl). O metabolito glucoronidado JWH-018 N-(5-OH-pentyl) preserva a sua afinidade para o recetor CB1 e a sua atividade como antagonista neutro (Ki: 922 nM). Não existem dados sobre se este metabolito é capaz de antagonizar os efeitos farmacológicos do JWH-018 in vivo, ou se são formadas concentrações suficientes no local de ação.
Efeitos clínicos, doses e toxicidade do АМ-2201.
O uso da substância por pessoas com doenças mentais é fortemente proibido. Quanto ao potencial de dependência, a dependência mental da substância ocorre exclusivamente com o uso repetido a longo prazo. Há dados sobre a possibilidade de ocorrência de síndrome de abstinência, que é caracterizada por humor distorcido, tremor nas extremidades, aumento da ansiedade, estado subdepressivo, aumento espontâneo da frequência cardíaca e ataques de pânico, e os sintomas acima são nivelados dentro de 2-3 meses de abstinência sem a terapia farmacológica.A substância em si tem o aspeto de um sólido cristalino branco (na forma pura), solúvel em etanol (5 mg/ml). Tem uma fórmula molecular C24H22FNO, peso molecular 359,43 g/mol, ponto de fusão 93,7 °C. O ponto de ebulição da substância é indeterminado. A síntese do АМ-2201 foi descrita pela primeira vez em 2001 por Alexandros Makriyannis e Hongfeng Deng. Começa com uma solução de 1-H indole no éter etílico do ácido acético, é adicionada uma solução de brometo de metil magnésio no éter etílico do ácido acético. Em seguida, adiciona-se cloreto de naftaleno-1-carbonilo (preparado a partir de ácido naftaleno-1-carboxílico e cloreto de tionilo) e, finalmente, uma solução aquosa de cloreto de amónio. Em seguida, o filtrado resultante da 1H-indol-3-il(naftaleno-1-il)metanona é lavado e recristalizado. Este produto é adicionado à suspensão de hidreto de sódio em dimetilformamida (DMF) e, em seguida, adiciona-se 5-bromopentilacetato para a N-alquilação. Após a clivagem do acetato por solução de hidróxido de potássio em metanol, procede-se à fluorização da cadeia lateral do pentilo utilizando trifluoreto de dietilaminossulfureto (DAST) e diclorometano.
Farmacocinética e farmacodinâmica do АМ-2201.
O АМ-2201 é metabolizado por várias enzimas da família CYP450. Em estudos com microssomas hepáticos humanos (HLM) e com proteína humana recombinante, identificou-se que CYP2C9 e CYP1A2 são as principais enzimas envolvidas na oxidação de АМ-2201, enquanto CYP2C19, 2D6, 2E1 e 3A4 têm um papel insignificante nesta fase do metabolismo. Além das reações metabólicas, o AM-2201 sofre defluoração enzimática, que se presume estar na presença do citocromo Р450 2Е1. Foi também revelado que os CYP1A2, 2C9 e 2C19 medeiam a desfluoração oxidativa. Em estudos in vitro e in vivo, a diferença entre JWH-018 e А-2201 foi revelada. Assim, JWH-018 N- (4OH-pentyl) é formado exclusivamente após a absorção de JWH-018, por isso pode ser usado como um marcador de diagnóstico para diferenciar entre a absorção de JWH-018 e AM-2201. Os principais metabolitos incluem: AM-2201 N-(4-OH-pentil), AM-2201 6-OH-indole, JWH-018 N-(5-OH-pentil), ácido pentanóico JWH-018, JWH-073 N-(4- OH-butil) e ácido butanóico JWH-073. A conjugação com o ácido glucurónico é realizada por várias UDP-glucuronosiltranseferases, principalmente hepáticas (UGT1A1, UGT1A9 e UGT2B7) e enzimas, incluindo: JWH-018 N-(5-OH-pentil), JWH-018 ácido pentanóico, JWH-073 N-(4-OH-butil), bem como JWH-073 ácido butanóico.
Quanto às constantes farmacológicas, após a administração de 5 mg de АМ-2201, a concentração máxima no soro com um indicador de 0,56 n/ml é detectada após 1 hora e 35 minutos, e continua a ser detetável no soro durante os cinco dias seguintes (com limite de deteção de 0,8 pg/ml). Este facto indica uma semi-vida de vários dias. Nos estudos de Carlier sobre o metabolismo do AM-2201 em ratos, foram determinados perfis de concentração temporal no plasma, que dependiam significativamente da dose e do tempo, enquanto a concentração aumentava linearmente à medida que a dose aumentava. Assim, após a administração de AM-2201 numa dose de 0,3 mg/kg, a concentração foi significativamente mais elevada do que após a administração de 0,1 mg/kg, embora fosse detetável no plasma mesmo após 4 horas com um indicador de 3,22 μg/L. O tempo máximo para a concentração máxima foi de 1,3 horas, e não dependeu da dose administrada. No entanto, a semi-vida de eliminação dependeu da dose administrada. O tempo para a concentração máxima do metabolito WH-018 N-(5-hidroxipentilo) foi de 2 horas, e o metabolito pôde ser detectado mesmo após 24 horas. Em 2013, Hutter relatou o primeiro estudo farmacocinético do AM-2201 em seres humanos, que se baseou na ingestão única da substância numa dose de 0,07 mg/kg. Em seu estudo, a concentração de AM-2201 no plasma caiu para 0,6 a <0,02 μg / L (LOQ) em 1,5-125 horas após a administração. Apenas 4 metabolitos foram identificados no soro: JWH-018 ácido N-pentanóico, JWH-018 N-(5-hidroxipentil), AM-2201 6'-hidroxiindol e AM-2201 N-(4-hidroxipentil). É importante notar que as concentrações séricas do ácido N-pentanóico do JWH-018 excederam as do АМ-2201 em todas as amostras. As concentrações máximas de JWH-018 N-(5-hidroxipentilo) e de ácido JWH-018 N-pentanóico foram registadas após 1,5 e 4,1 horas desde a administração da substância, respetivamente. O ácido N-pentanóico do JWH-018 foi detetável até 57 horas após a ingestão. Os diferentes indicadores nos ratos e nos seres humanos resultam, presumivelmente, de diferenças interespecíficas e de diferenças nas formas de administração. Assim, após a administração oral do AM-2201, o metabolismo gastrointestinal foi mais significativo do que a via sc, que é uma forma de contornar esta via metabólica. A concentração de AM-2201 no sangue em casos humanos não excedeu 5 μg/L.
Ainda não foram revelados dados sobre a farmacodinâmica da substância in vivo. No entanto, sabe-se que tem uma elevada afinidade de ligação aos receptores canabinóides de primeiro tipo, expressa em IC50 (ocupação de 50% dos receptores) - 1,0 nM e aos receptores canabinóides de segundo tipo - 2,6 nM, em comparação com a afinidade do delta-9 tetrahidrocanabinol (THC) - 40,7 nM para os receptores CB1- e 36,4 nM para os receptores CB2. Além disso, em estudos in vitro com análise de ligação de [35S] guanosina-5'-O-(3-thio)-trifosfato ([35S]GTPγS), a concentração efectiva de 50% (EC50) é determinada em 0,24 nM com propriedades agonísticas completas da substância em termos de receptores. Com base nestes dados e em observações clínicas, pode presumir-se que o AM-2201 apresenta efeitos típicos dos agonistas CB1. Estes efeitos podem incluir sedação, disfunção cognitiva, taquicardia, hipotensão postural, boca seca, ataxia, imunossupressão e efeitos psicotrópicos. Uma diferença acentuada em relação ao THC é a formação de metabolitos potencialmente farmacologicamente activos pelo AM-2201. No caso do THC, sabe-se que apenas um dos principais metabolitos tem propriedades psicoactivas e preserva a afinidade de ligação aos receptores canabinóides (11-OH-THC: Ki no recetor CB1: 38,4 ± 0,8 nM). Alguns metabolitos do AM-2201 preservam uma elevada afinidade de ligação ao recetor CB1 com uma classificação relativa de ligação AM-2201 > AM-2201 N-(4-OH-pentyl) = JWH-018 N-(5-OH- pentyl) > THC > JWH-073 N-(4-OH-butyl). O metabolito glucoronidado JWH-018 N-(5-OH-pentyl) preserva a sua afinidade para o recetor CB1 e a sua atividade como antagonista neutro (Ki: 922 nM). Não existem dados sobre se este metabolito é capaz de antagonizar os efeitos farmacológicos do JWH-018 in vivo, ou se são formadas concentrações suficientes no local de ação.
Efeitos clínicos, doses e toxicidade do АМ-2201.
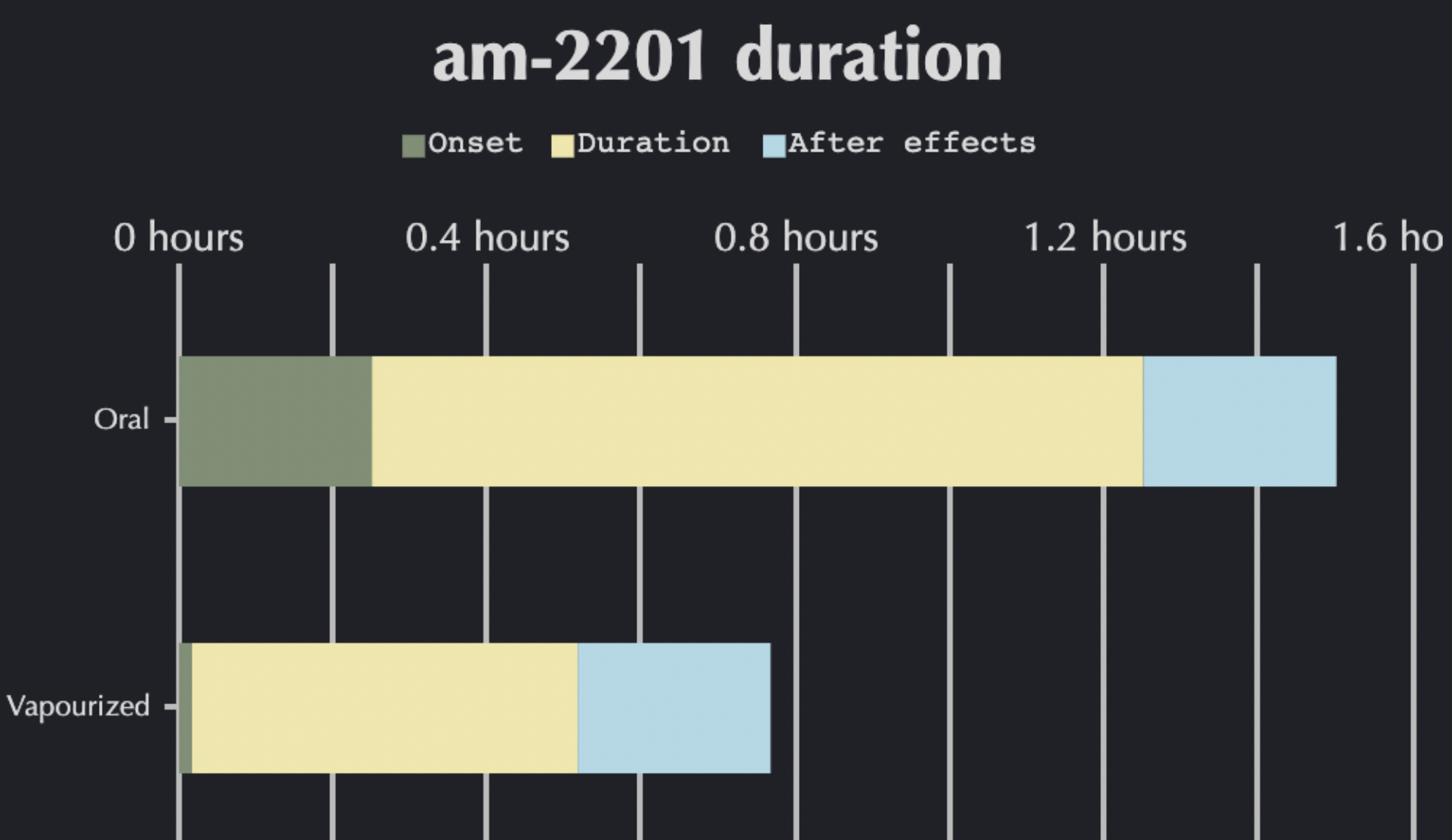
A percentagem de АМ-2201 em várias "misturas de ervas" é heterogénea e pode variar (de acordo com diferentes fontes) de 1 a 300 mg/g. O indicador médio varia entre 30 mg/g. Considerando o facto de que o método mais comum de administração do AM-2201 é fumar, a identificação de doses exactas numa mistura é impossível. No entanto, ao analisar os dados da investigação, pode ser feita uma gradação da dose da substância pura em termos da percentagem de THC e CBD na substância. Assim, a dose mínima inicial (incluindo os dados do EMCDDA) de АМ-2201, que está associada a efeitos clínicos significativos e percetíveis, é de 3-4 μg/kg. As doses médias variam entre 8 e 17 μg/kg. Qualquer dose superior a 20 μg/kg é elevada e considera-se que implica o risco mais elevado de desenvolvimento de efeitos secundários pronunciados. Considerando um risco potencialmente elevado de desenvolvimento de efeitos secundários, não se recomenda a utilização do AM-2201 em doses elevadas devido à perda de controlo sobre o estado físico e mental. Quando administrado por inalação, o início dos efeitos dá-se em 5 minutos e o pico dos efeitos em 30-50 minutos. Os efeitos podem durar 60-180 minutos, e o período pós-efeitos dura até 5 horas, dependendo da dose.
Os efeitos positivos desejáveis da substância incluem os mesmos efeitos que ocorrem devido à utilização de THC: euforia, relaxamento moderado, comportamento alegre, algumas ilusões, etc. No entanto, tendo em conta o facto de o AM-2201 ser um canabinóide sintético (e devido à sua especificidade farmacodinâmica), tem efeitos secundários mais pronunciados, que incluem oscilação (marcha trémula), coordenação prejudicada, aumento da pressão arterial (ou uma diminuição pronunciada) e do pulso, afasia, convulsões, comportamento agressivo, movimentos lentos, vermelhidão da conjuntiva, alucinações, sonolência, sopor ou coma, tremor das pálpebras, sangramento das gengivas, midríase, desorientação, ansiedade e paranoia, depressão (em pós-efeitos), síndrome de despersonalização / desrealização ocorre raramente. Além disso, os efeitos negativos incluem taquicardia, agitação, alucinações, hipertensão, um ligeiro aumento da glucose no sangue, hipocalemia, vómitos, dores no peito, convulsões, mioclonia, ansiedade grave que conduz a ataques de pânico e psicose aguda.
A toxicidade do AM-2201 foi estudada apenas em células neurais primárias do prosencéfalo e mostrou indução de citotoxicidade em função da concentração. Durante a pré-incubação com um antagonista seletivo de CB1, a citotoxicidade de АМ-2201 (30 μM) foi deprimida, o que indica um papel importante dos receptores CB1 na indução de citotoxicidade desta linha de células, não em outros mecanismos. Além disso, a citotoxicidade de АМ-2201 ocorre por apoptose e é mediada por caspases, o que indica um forte efeito neurotóxico. Devido à natureza lipofílica desta substância, não se pode excluir que ocorram concentrações mais elevadas nas secções profundas (através do efeito de acumulação) ou nas células epiteliais do trato digestivo (que são diretamente expostas ao fumo ou à substância pura). A neurotoxicidade do AM-2201 é comprovada pelo facto de o sistema endocanabinóide já estar formado no sistema nervoso central em desenvolvimento desde o momento da conceção e também pelo facto de o canabimimético -55,212-2, que interfere no sistema endocanabinóide, causar anencefalia e perturbações neurocomportamentais na descendência. Também se pode supor que, tendo em conta as propriedades físico-químicas da substância, esta pode passar para os tecidos fetais através da placenta. Os sintomas clínicos de abstinência mais comuns são: ansiedade, humor instável, explosões de choro, sensação de vazio interior, falta de ar, hiperacusia, dores somáticas, hiperventilação, sudação intensa, ansiedade motora e interna, insónia, tosse, dificuldade de concentração.
Os efeitos positivos desejáveis da substância incluem os mesmos efeitos que ocorrem devido à utilização de THC: euforia, relaxamento moderado, comportamento alegre, algumas ilusões, etc. No entanto, tendo em conta o facto de o AM-2201 ser um canabinóide sintético (e devido à sua especificidade farmacodinâmica), tem efeitos secundários mais pronunciados, que incluem oscilação (marcha trémula), coordenação prejudicada, aumento da pressão arterial (ou uma diminuição pronunciada) e do pulso, afasia, convulsões, comportamento agressivo, movimentos lentos, vermelhidão da conjuntiva, alucinações, sonolência, sopor ou coma, tremor das pálpebras, sangramento das gengivas, midríase, desorientação, ansiedade e paranoia, depressão (em pós-efeitos), síndrome de despersonalização / desrealização ocorre raramente. Além disso, os efeitos negativos incluem taquicardia, agitação, alucinações, hipertensão, um ligeiro aumento da glucose no sangue, hipocalemia, vómitos, dores no peito, convulsões, mioclonia, ansiedade grave que conduz a ataques de pânico e psicose aguda.
A toxicidade do AM-2201 foi estudada apenas em células neurais primárias do prosencéfalo e mostrou indução de citotoxicidade em função da concentração. Durante a pré-incubação com um antagonista seletivo de CB1, a citotoxicidade de АМ-2201 (30 μM) foi deprimida, o que indica um papel importante dos receptores CB1 na indução de citotoxicidade desta linha de células, não em outros mecanismos. Além disso, a citotoxicidade de АМ-2201 ocorre por apoptose e é mediada por caspases, o que indica um forte efeito neurotóxico. Devido à natureza lipofílica desta substância, não se pode excluir que ocorram concentrações mais elevadas nas secções profundas (através do efeito de acumulação) ou nas células epiteliais do trato digestivo (que são diretamente expostas ao fumo ou à substância pura). A neurotoxicidade do AM-2201 é comprovada pelo facto de o sistema endocanabinóide já estar formado no sistema nervoso central em desenvolvimento desde o momento da conceção e também pelo facto de o canabimimético -55,212-2, que interfere no sistema endocanabinóide, causar anencefalia e perturbações neurocomportamentais na descendência. Também se pode supor que, tendo em conta as propriedades físico-químicas da substância, esta pode passar para os tecidos fetais através da placenta. Os sintomas clínicos de abstinência mais comuns são: ansiedade, humor instável, explosões de choro, sensação de vazio interior, falta de ar, hiperacusia, dores somáticas, hiperventilação, sudação intensa, ansiedade motora e interna, insónia, tosse, dificuldade de concentração.
Last edited by a moderator:
