Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 328
- Reaction score
- 332
- Points
- 63
A dextroanfetamina (D-AMP) pertence a uma classe de estimulantes do sistema nervoso central. A Food and Drug Administration dos EUA a classifica como uma substância de cronograma II com alto potencial de abuso. Os medicamentos com liberação imediata e retardada de anfetamina são aprovados pela FDA para o tratamento de TDAH e narcolepsia em adultos e crianças. A dextroanfetamina é diferente de seu reflexo - a levoanfetamina - porque tem uma estimulação mais pronunciada do sistema nervoso devido à dopamina, e menos devido à norepinefrina.
Síntese da dextroanfetamina a partir do P2P
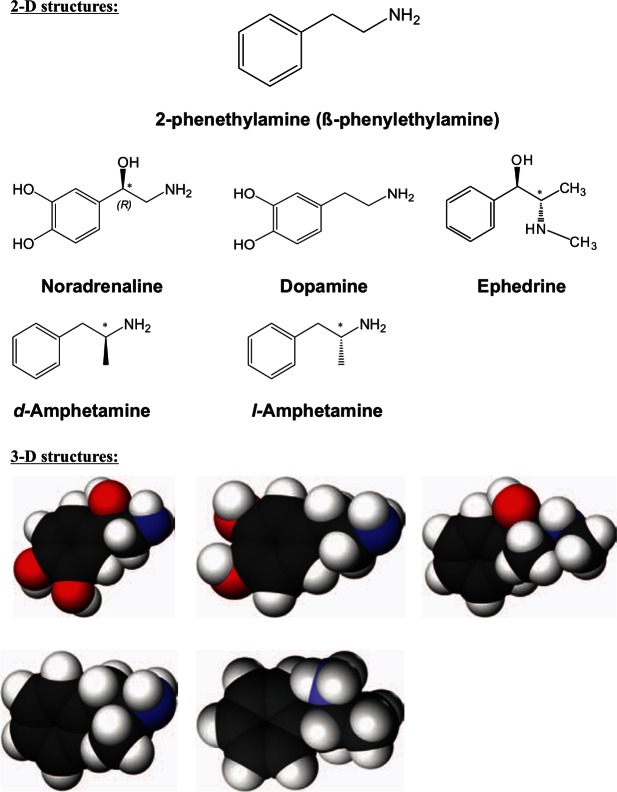
Propriedades físico-químicas e formas da substância.
Fundamentalmente, a dextroanfetamina, assim como o racemato de anfetamina, tem a aparência de um líquido oleoso volátil incolor com um odor característico de "peixe" e é bem solúvel em solventes orgânicos. Seu ponto de ebulição é de 200-203 °C. O enantiômero pode ter uma aparência pulverulenta com a formação de pequenas "pedras" de cor branca ou amarelo-claro/creme, com um odor fraco, fracamente higroscópico, parcialmente solúvel em água quando está na forma de comprimido. É mais frequentemente encontrado na forma de sulfato, cloridrato, sucrato e, muito raramente, na forma de fosfato. Em geral, a dextroanfetamina faz parte de vários medicamentos, como "Aderral" e "Dexedrine", onde é encontrada na forma de sucrato e sulfato em concentrações de 25% do volume total. Também faz parte do "Vyvanse", "Elvanse", "Tyvense", onde se encontra no estado proativo de dimesilato de lisdexanfetamina; a fermentação com l-lisina a metaboliza na forma ativa de d-anfetamina; "Dexedrine". Outros nomes comerciais de medicamentos incluem: Sulfato de dexedrina, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedrina, Diocurb, Dextrostat.
Farmacocinética.
Quando administrada, a anfetamina é metabolizada por hidroxilação, onde o principal citocromo é o CYP2D6, beta-hidroxilação (DBH) e desaminação oxidativa (FMO3); há outras enzimas que estão menos envolvidas no metabolismo da anfetamina, como a butirato-CoA ligase e a glicina-N-aciltransferase. A biodisponibilidade (com pH gastrointestinal inalterado) chega a 70-75% para o racemato e até 80-83% para a dextroanfetamina. A ligação com as proteínas plasmáticas chega a 15-30% de acordo com várias fontes em pessoas saudáveis, o volume de distribuição é moderado, a substância passa ativamente pela barreira hematoencefálica com um coeficiente variável de 17p. T1/2 é de cerca de 7 a 15 horas, dependendo de muitos fatores, incluindo o pH da urina (com uma aceleração da meia-vida em valores mais baixos). Imax - 15-70 minutos. A dosagem letal do isômero d da anfetamina não foi estudada; entretanto, há conclusões teóricas sobre grandes valores de DL 50 de 5-10% a partir dos dados extrapolados disponíveis do racemato padrão do sulfato de anfetamina (98-130 mg/kg). A anfetamina é eliminada quase nos mesmos indicadores qualitativos dos metabólitos conhecidos; no entanto, o volume de ácido hipúrico, glicuronídeo de benzoíla e norefedrina é significativamente menor (60% do total de dados), o que se deve à especificidade desse racemato no contexto do metabolismo em nível de desaminação. Em estudos com roedores, foi comprovada uma diminuição acentuada da genotoxicidade em contraste com o racemato de anfetamina padrão na dose de 4600 mg/ml.
Mecanismo de ação.
O mecanismo de ação farmacodinâmico quase não difere da forma fundamental da anfetamina. Por meio da inibição e reversão dos transportadores de serotonina, norepinefrina e dopamina, interação com TAAR1, o que, em última análise, leva a um aumento na concentração de monoaminas e catecolaminas simultaneamente na fenda sináptica (o espaço é de 10-50 nm de largura entre as membranas, as bordas são reforçadas por contatos intercelulares). Uma característica importante da dextroanfetamina, especificamente, é o fato de que a afinidade do enantiômero do lado direito com o TAAR1 é muito maior (de 15 a 30%, de acordo com várias fontes), e o VMAT2 capta uma quantidade menor desse enantiômero, e a afinidade mínima para o transportador de serotonina, em contraste com o do lado esquerdo, e a carga de sistemas como CDK5R1, DLG1 e CAMKIIAA é significativamente menor com efeitos clínicos equivalentes.
Não menos importante é o fato científico identificado pela Novascreen BioSciences Corporation de que, devido à menor afinidade por vários receptores (a1, a2, b-adrenoreceptores, mu-opioide, histamina, CCK, NK, GABA, ETeA e outros), a gravidade dos efeitos clínicos colaterais indesejáveis e outras consequências negativas no nível molecular são significativamente menores, o que determina a prioridade dessa forma específica da substância com a preservação dos efeitos clínicos desejados correspondentes. O efeito líquido dessas propriedades de ação múltipla é que a d-anfetamina aumenta a "disponibilidade" ou a capacidade de concentração de catecolaminas no espaço extracelular, revertendo o transporte de catecolaminas da extremidade terminal do neurônio, o que também é uma das características do enantiômero de rotação direita. Os indicadores de inibição da captação de [3 H] por sinaptossomas de cérebro de rato pelo d-enantiômero variam e diferem significativamente do racemato de anfetamina. Para norepinefrina, Ki = nM em um valor de 45-50, para dopamina 82-200, para 5-HT, os indicadores variam de 1840 a 3830 em modelos de cérebro de ratos. Um efeito mais "suave" do ciclo de dependência dessa forma de anfetamina é consequência de uma superexpressão relativamente menor de FosB no núcleo accumbens, da presença de efeitos positivos e da ausência de inibição de CREB por proteínas e serina fosfotases, precisamente devido à menor afinidade e influência nos sistemas glutamatérgicos e serotoninérgicos. Os efeitos neuroquímicos em comparação também têm uma capacidade distinta; nos estudos de Heal e Wickens, foram detectadas alterações na atividade motora, em que seu valor máximo foi de 3 a 4 vezes menor do que com a ingestão de cloridrato ou sulfato de anfetamina, o que está diretamente relacionado à taxa e à correção molecular do fluxo de saída da dopamina no estriado do cérebro.
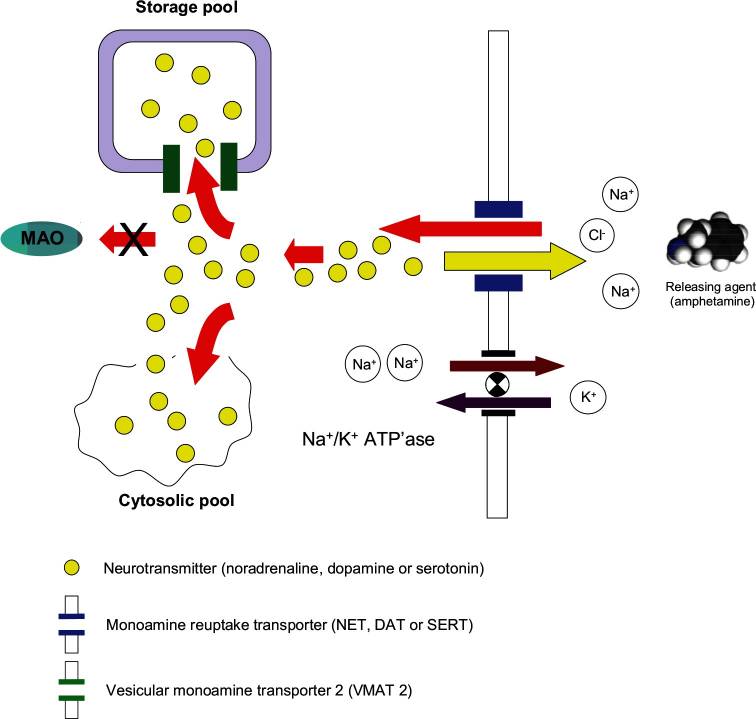
Embora os experimentos in vitro forneçam uma boa visão dos mecanismos individuais, a eficácia da anfetamina em relação a outros agonistas indiretos de monoamina, por exemplo, os inibidores clássicos da recaptação, só pode ser estimada a partir de experimentos in vivo. Usamos a microdiálise intracerebral de sonda dupla para explorar os efeitos in vivo da d- e l-anfetamina no rato espontaneamente hipertenso (SHR), que foi proposto como modelo roedor de TDAH. Ambos os isômeros da anfetamina aumentaram de forma dependente da dose as concentrações extracelulares de noradrenalina no córtex pré-frontal (PFC) e de dopamina no estriado. A farmacodinâmica de seus efeitos é típica daquelas relatadas para agentes liberadores de monoamina, ou seja, um rápido início de ação com aumentos de pico de noradrenalina e efluxo de dopamina ocorrendo em 30-45 minutos, grandes efeitos (400-450% da linha de base para noradrenalina e 700-1500% da linha de base para dopamina), com um declínio relativamente rápido após o máximo. Embora nenhum resultado comparativo tenha sido incluído nesta revisão, a magnitude dos aumentos produzidos pelos isômeros da anfetamina é maior do que a relatada para os inibidores clássicos da recaptação, como a atomoxetina ou a bupropiona, e não há limite de dose-efeito para as ações da anfetamina.
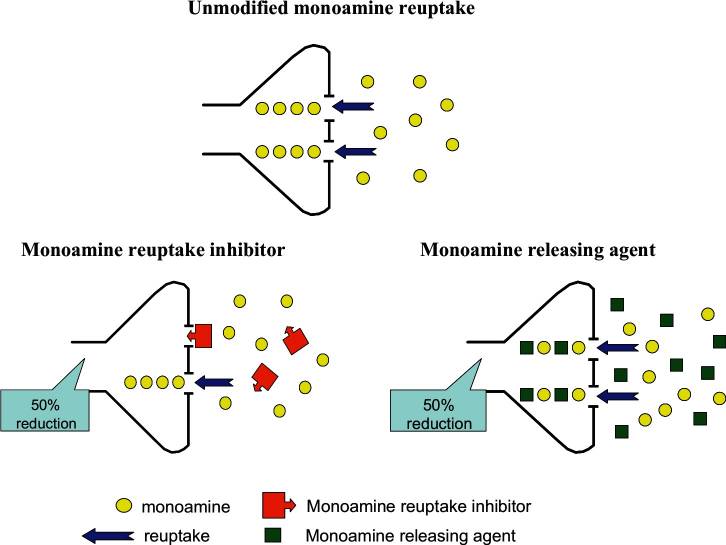
Ao comparar os efeitos dos medicamentos sobre o efluxo de catecolaminas no CPF, é importante considerar a neuroanatomia altamente incomum dessa região cerebral. A densidade dos sítios DAT nos neurônios dopaminérgicos do CPF é muito baixa e, como consequência, a maior parte da dopamina liberada é sequestrada via NET nos neurônios noradrenérgicos. Embora existam poucos sítios DAT nos neurônios dopaminérgicos do CPF, sua capacidade de recaptação é suficiente para que a anfetamina provoque uma liberação substancial de dopamina, embora tenha sido sugerido que grande parte da liberação de dopamina no CPF provém de neurônios noradrenérgicos. Nos estudos de desenvolvimento da Shire em modelos in vivo, foi comprovada uma diferença estatisticamente significativa. O D-AMP influenciou os componentes cognitivos do controle impulsivo de forma diferente: a proporção de escolha impulsiva diminuiu com o mesmo nível de recompensa, o que também confirma a eficácia desse enantiômero.
Métodos de uso e doses.
A dosagem recreativa do d-enantiômero de anfetamina começa com 40-60 mg por via oral; em casos de tolerância presente, a dosagem inicial pode ser aumentada para 120-160 mg em uma única aplicação oral. Quando administrada por via intranasal, recomenda-se usar uma dose inicial de 30-50 mg. A administração parenteral dessa forma é permitida somente no caso de se obter uma solução pura. Quaisquer comprimidos ou pós são recomendados para uso apenas por administração oral e intranasal. Na administração parenteral, a dose inicial é de 0,15-0,24 mg/kg.
Apresentação clínica da intoxicação por anfetamina.
Os sintomas acima são "leves", sua gravidade é até 40% menor do que a da forma combinada. Portanto, efeitos negativos indesejáveis como dificuldade para urinar, distúrbios do ritmo cardíaco, aumento da frequência cardíaca, aumento da pressão arterial, aumento da sudorese, temperatura corporal elevada, náusea, dilatação da pupila ocorrem exclusivamente em altas doses e são proporcionalmente diferentes em comparação com o racemato.
1. Euforia e sensação de aumento de energia;
2. Vigília prolongada;
3. Ideias ou ações grandiosas;
4. Comportamento violento ou agressivo;
5. Viés de confirmação;
6. Labilidade do humor;
7. Comportamento caracterizado por estereótipos repetidos;
8. Ilusões auditivas, visuais ou táteis;
9. Distorção da personalidade;
10. Supressão do apetite.
Além disso, as pessoas que usam D-AMP devem apresentar pelo menos dois dos seguintes sinais para serem diagnosticadas:
1. Taquicardia;
2. Hipertensão arterial;
3. Sudorese e calafrios febris;
4. Náusea ou vômito;
5. Fraqueza muscular;
6. Dor ou desconforto atrás do esterno;
7. Agitação psicomotora;
8. Dilatação da pupila.
Os sintomas da intoxicação por D-AMP incluem principalmente sinais de complicações cardiovasculares e do sistema nervoso. Os distúrbios respiratórios ocorrem com menos frequência.
Distúrbios cardíacos: hipertensão e taquicardia são os mais comuns, quando se tomam doses baixas. A bradicardia inicial também é possível devido a um aumento no tônus parassimpático. As arritmias (supraventriculares são frequentes) podem ser causadas por uma crise simpática ou por um bloqueio dos canais rápidos de sódio. A isquemia e o infarto do miocárdio são causados por espasmo coronariano, que atinge o máximo 30 minutos após o uso de D-AMP intranasal e coincide com o pico de concentração da droga no sangue. Mais espasmos coronarianos podem se desenvolver após 90 minutos, o que está associado ao acúmulo de metabólitos de D-AMP. Um aumento na agregação plaquetária leva à formação de coágulos sanguíneos nos vasos coronários. Além disso, a demanda de oxigênio do miocárdio aumenta. Uma complicação rara é a ruptura da aorta.
Instruções especiais, interações com outras substâncias.
As contraindicações absolutas do uso de qualquer forma de anfetamina são: aterosclerose vascular grave, quaisquer doenças cardiovasculares sintomáticas, ingestão de MAO (e 14 dias após o último ato de uso de medicamento desse grupo), glaucoma, hipertireoidismo.
A regra "não-ADIOS":
Não alcoólicos - não é recomendado o uso com álcool.
Não dissociativos - não é recomendado o uso com drogas dissociativas.
Não-iMAO - não é recomendado o uso com inibidores da monoamina oxidase.
Não opiáceos - não é recomendado o uso com agonistas de receptores opiáceos.
Não estimulantes - não é recomendado o uso com estimulantes.
1. Ao usar o D-AMP junto com medicamentos do grupo dos inibidores da PDE-5, o risco de desenvolver efeitos colaterais de ambas as substâncias aumenta. Efeitos colaterais mais comuns: dor de cabeça intensa de natureza espástica, náusea. A incidência de desenvolvimento de condições críticas graves é baixa.
2. Ao usar o D-AMP junto com a maconha, há risco de aumento da pressão arterial, dor de cabeça, tremores finos e secura na boca. A probabilidade de desenvolvimento de condições críticas graves é baixa.
3. Ao usar o D-AMP com neurolépticos/tranquilizantes, há um alto risco de nivelamento dos principais efeitos do D-AMP. A probabilidade de desenvolvimento de condições críticas graves é baixa (nos casos em que não há contraindicações para o uso de neurolépticos).
4. Não é recomendado o uso de D-AMP durante o tratamento com medicamentos antibacterianos, antivirais e antifúngicos, hormônios e anticoagulantes.
5. Não é recomendado o uso do D-AMP durante qualquer manipulação cirúrgica e antes e depois disso por um determinado período (o período é identificado individualmente).
6. Não é recomendável usar D-AMP se for diagnosticado com qualquer distúrbio do sistema cardiovascular, dos rins, do fígado, dos pulmões e do sistema nervoso central.
7. Não é recomendado o uso de D-AMP durante a gravidez e a lactação.
Em dois estudos publicados anteriormente, Jasinski e Krishnan compararam os efeitos subjetivos da d-anfetamina IR em voluntários humanos com experiência com drogas quando esses compostos foram administrados por via intravenosa e oral. No estudo em que eles compararam esses compostos após a administração oral, a d-anfetamina IV (40 mg (29,6 mg de base de d-anfetamina)) evocou um aumento estatisticamente significativo em relação ao placebo em "Gosto pela droga" na escala do Questionário de Avaliação de Drogas - Sujeito (DQRS), enquanto a dose equivalente de d-anfetamina (100 mg, oral) não o fez. Além disso, o tempo do pico do efeito farmacológico da d-anfetamina foi substancialmente atrasado em comparação com a d-anfetamina IR, em 3,0 h versus 1,5-2,0 h. Quando a d-anfetamina foi administrada em uma dose maior de 150 mg, ela aumentou significativamente a pontuação do DQRS "Gosto pela droga" em uma extensão equivalente à d-anfetamina IR (40 mg oral). No entanto, o efeito de pico da dose mais alta de d-amfetamina foi ainda mais tardio, em 4,0 h. Quando a via intravenosa foi explorada, a d-anfetamina IV (20 mg intravenosa) produziu um pico de pontuação de "gosto pela droga" 20 minutos após a dosagem, que coincidiu com a Cmax plasmática. Em contraste, a dose equivalente de d-anfetamina (50 mg intravenosa) não aumentou significativamente o "gosto pela droga" em relação ao placebo, e a Cmax da d-anfetamina plasmática ocorreu consideravelmente mais tarde, às 2,0 h. Ambos os compostos produziram valores equivalentes de AUC0-24h, mas em comparação com a dose equivalente de d-anfetamina IR, a Cmax da d-anfetamina plasmática foi três vezes menor para a lisdexamfetamina e o tmax foi três vezes maior.
Primeiros socorros em caso de superdosagem.
O mecanismo de toxicidade está relacionado principalmente ao excesso de dopamina extracelular, norepinefrina e serotonina. A síndrome clínica primária envolve efeitos neurológicos e cardiovasculares proeminentes, mas as complicações secundárias podem envolver efeitos renais, musculares, pulmonares e gastrointestinais. Hiperatividade, hipertermia, taquicardia, taquipneia, midríase, tremores, convulsões e estado mental alterado são alguns dos sinais e sintomas mais comuns da intoxicação por anfetamina. O diagnóstico pode ser confirmado pela detecção de anfetamina no conteúdo estomacal ou no vômito, ou por exame toxicológico de urina positivo para drogas ilícitas. Uma triagem de anfetamina falso-positiva pode ocorrer após uma overdose de trazodona ou de bupropiona. Não há antídoto para a toxicidade da anfetamina; entretanto, o carvão ativado é um tratamento de emergência. Em pacientes que podem beber com segurança, a recomendação é administrar carvão ativado de 1 a 2 g/kg até 100 g por via oral se a ingestão tiver ocorrido na última hora. A toxicidade relacionada à anfetamina requer tratamento por meio do controle dos sinais cardiovasculares e do sistema nervoso central que ameaçam a vida em um ambiente tranquilo.
Indicações para ir ao hospital ou chamar uma ambulância: consciência prejudicada ou ausente, fala prejudicada, atividade motora, falta de orientação no espaço e no tempo, dor intensa atrás do esterno que dure mais de meia hora, aumento da temperatura corporal de mais de 38,0 C ou hipertermia que dure mais de meia hora, aumento da pressão arterial de mais de 180/110 mmHg sem efeito de terapia hipotensiva.
1. O tratamento de pacientes com pressão arterial superior a 140/95 mm Hg inclui um comprimido de betabloqueador sem atividade simpaticomimética intrínseca, um comprimido de inibidor da ECA e, após 30 minutos, um comprimido de tranquilizante (0,25 mg de alprazolam).
2. Em pacientes com ansiedade intensa, ataque de pânico, psicose: um comprimido de um tranquilizante e um comprimido de um neuroléptico com efeito sedativo, ajuda psicológica, psicoterapia de emergência.
3. Em pacientes com dor no esterno, desconforto no peito: um comprimido de bloqueadores lentos dos canais de cálcio da terceira geração, reduzindo reflexivamente a frequência cardíaca, um comprimido de um inibidor da ECA da terceira geração OU um comprimido de um agonista dos efeitos da imidazolina OU um comprimido; se a síndrome da dor não se tornar menos intensa em 20 minutos, recomenda-se ir ao hospital.
4. Quando houver um aumento na temperatura corporal não superior a 37,5 °C, recomenda-se a observação dinâmica por meia hora. Não é necessário tratamento farmacológico. Se a hipertermia persistir por mais de meia hora (na ausência de causas externas), recomenda-se ir ao hospital.
5. Em pacientes com dores de cabeça intensas, recomenda-se o uso de antiespasmódicos em combinação com remédios fitoterápicos sedativos ou tranquilizantes em doses baixas. Se a cefaleia estiver associada a vômitos, recomenda-se uma injeção intramuscular de metoclopramida 2,0 ml. A náusea isolada e a dispepsia funcional não requerem tratamento farmacológico.
6. Para tremores, convulsões moderadas ou agitação psicomotora leve, recomenda-se o uso de tranquilizantes. É altamente recomendável não usar neurolépticos nesses casos.
Um betabloqueador, como o propranolol, pode ajudar a controlar as taquiarritmias cardíacas. Considere o uso de nitroprussiato intravenoso (comece com 0,5 a 1 mcg/kg por minuto e aumente conforme necessário) para hipertensão grave. Deve-se administrar fluido intravenoso, pois ele combate a hipertermia, auxilia na manutenção da função renal e ajuda a promover a eliminação da anfetamina e seus análogos. Em casos de agitação grave, os médicos devem considerar um tratamento agressivo para evitar hipertensão maligna, rabdomiólise, hipertermia e convulsões. As evidências apóiam o uso de grandes doses de benzodiazepínicos para tratar a psicose e a agitação relacionadas à overdose de anfetaminas. Nos casos em que a agitação, o delírio e os distúrbios de movimento não respondem aos benzodiazepínicos, as terapias de segunda linha incluem antipsicóticos, como ziprasidona ou haloperidol, agonistas centrais de alfa-adrenorreceptores, como dexmedetomidina, ou propofol. A paralisia neuromuscular, a intubação e as medidas de resfriamento ativo podem ser necessárias em casos graves. Em pacientes com taquicardia, faça um ECG e considere a possibilidade de telemetria. Use fluidos intravenosos e sedação para controlar os sintomas cardíacos. Em casos de hipertensão grave, considere nitroprussiato intravenoso. Iniciar solução salina normal a 0,9% e monitorar a creatina quinase (CK), os eletrólitos e a creatinina é a melhor maneira de controlar a rabdomiólise.
Há relatos de casos sobre a cardiomiopatia de Takotsubo (TTC), também conhecida como cardiomiopatia induzida por estresse, que é desencadeada por overdose de anfetaminas. Em um caso, um paciente foi ao departamento de emergência após ingerir 30 comprimidos de sal de anfetamina com sintomas de dor no peito e falta de ar. No momento da apresentação, as enzimas cardíacas estavam elevadas, o eletrocardiograma não apresentava alterações e a fração de ejeção (FE) era de 25% a 30% com hipocinesia grave. No entanto, 24 horas depois, os sintomas foram resolvidos e um ecocardiograma repetido, realizado três dias depois, mostrou uma FE de 60%, sem anormalidades regionais de movimento da parede.
Termos de detecção e regras de armazenamento.
Como regra geral, o armazenamento do racemato de anfetamina, bem como do d-enantiômero, deve ser feito em local protegido da luz e da umidade, de preferência em temperatura ambiente ou a uma temperatura de pelo menos 5 °C e não mais de 40 °C. Pode ser armazenado em papel alimentício ou em embalagens de polietileno tereftalato sem conteúdo metálico.
Após um único uso intranasal de dextroanfetamina, o período de detecção na urina, quando se usam métodos expressos de pesquisa, é de aproximadamente 46 a 72 horas, com uso oral de até 120 a 220 horas. O uso sistemático prolongado de dextroanfetamina não foi estudado no contexto da identificação de metabólitos, embora, teoricamente, se saiba que há uma grande chance de detectar os principais metabólitos por PFIA ou cromatografia-espectrometria de massa durante 1,5 a 2 meses após o último uso de anfetamina (que é menor do que o racemato de anfetamina). O período de detecção dos metabólitos da dextroanfetamina no cabelo é de até 2,5 a 3 meses.
Síntese da dextroanfetamina a partir do P2P
Propriedades físico-químicas e formas da substância.
Fundamentalmente, a dextroanfetamina, assim como o racemato de anfetamina, tem a aparência de um líquido oleoso volátil incolor com um odor característico de "peixe" e é bem solúvel em solventes orgânicos. Seu ponto de ebulição é de 200-203 °C. O enantiômero pode ter uma aparência pulverulenta com a formação de pequenas "pedras" de cor branca ou amarelo-claro/creme, com um odor fraco, fracamente higroscópico, parcialmente solúvel em água quando está na forma de comprimido. É mais frequentemente encontrado na forma de sulfato, cloridrato, sucrato e, muito raramente, na forma de fosfato. Em geral, a dextroanfetamina faz parte de vários medicamentos, como "Aderral" e "Dexedrine", onde é encontrada na forma de sucrato e sulfato em concentrações de 25% do volume total. Também faz parte do "Vyvanse", "Elvanse", "Tyvense", onde se encontra no estado proativo de dimesilato de lisdexanfetamina; a fermentação com l-lisina a metaboliza na forma ativa de d-anfetamina; "Dexedrine". Outros nomes comerciais de medicamentos incluem: Sulfato de dexedrina, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betafedrina, Diocurb, Dextrostat.
Farmacocinética.
Quando administrada, a anfetamina é metabolizada por hidroxilação, onde o principal citocromo é o CYP2D6, beta-hidroxilação (DBH) e desaminação oxidativa (FMO3); há outras enzimas que estão menos envolvidas no metabolismo da anfetamina, como a butirato-CoA ligase e a glicina-N-aciltransferase. A biodisponibilidade (com pH gastrointestinal inalterado) chega a 70-75% para o racemato e até 80-83% para a dextroanfetamina. A ligação com as proteínas plasmáticas chega a 15-30% de acordo com várias fontes em pessoas saudáveis, o volume de distribuição é moderado, a substância passa ativamente pela barreira hematoencefálica com um coeficiente variável de 17p. T1/2 é de cerca de 7 a 15 horas, dependendo de muitos fatores, incluindo o pH da urina (com uma aceleração da meia-vida em valores mais baixos). Imax - 15-70 minutos. A dosagem letal do isômero d da anfetamina não foi estudada; entretanto, há conclusões teóricas sobre grandes valores de DL 50 de 5-10% a partir dos dados extrapolados disponíveis do racemato padrão do sulfato de anfetamina (98-130 mg/kg). A anfetamina é eliminada quase nos mesmos indicadores qualitativos dos metabólitos conhecidos; no entanto, o volume de ácido hipúrico, glicuronídeo de benzoíla e norefedrina é significativamente menor (60% do total de dados), o que se deve à especificidade desse racemato no contexto do metabolismo em nível de desaminação. Em estudos com roedores, foi comprovada uma diminuição acentuada da genotoxicidade em contraste com o racemato de anfetamina padrão na dose de 4600 mg/ml.
Mecanismo de ação.
O mecanismo de ação farmacodinâmico quase não difere da forma fundamental da anfetamina. Por meio da inibição e reversão dos transportadores de serotonina, norepinefrina e dopamina, interação com TAAR1, o que, em última análise, leva a um aumento na concentração de monoaminas e catecolaminas simultaneamente na fenda sináptica (o espaço é de 10-50 nm de largura entre as membranas, as bordas são reforçadas por contatos intercelulares). Uma característica importante da dextroanfetamina, especificamente, é o fato de que a afinidade do enantiômero do lado direito com o TAAR1 é muito maior (de 15 a 30%, de acordo com várias fontes), e o VMAT2 capta uma quantidade menor desse enantiômero, e a afinidade mínima para o transportador de serotonina, em contraste com o do lado esquerdo, e a carga de sistemas como CDK5R1, DLG1 e CAMKIIAA é significativamente menor com efeitos clínicos equivalentes.
Não menos importante é o fato científico identificado pela Novascreen BioSciences Corporation de que, devido à menor afinidade por vários receptores (a1, a2, b-adrenoreceptores, mu-opioide, histamina, CCK, NK, GABA, ETeA e outros), a gravidade dos efeitos clínicos colaterais indesejáveis e outras consequências negativas no nível molecular são significativamente menores, o que determina a prioridade dessa forma específica da substância com a preservação dos efeitos clínicos desejados correspondentes. O efeito líquido dessas propriedades de ação múltipla é que a d-anfetamina aumenta a "disponibilidade" ou a capacidade de concentração de catecolaminas no espaço extracelular, revertendo o transporte de catecolaminas da extremidade terminal do neurônio, o que também é uma das características do enantiômero de rotação direita. Os indicadores de inibição da captação de [3 H] por sinaptossomas de cérebro de rato pelo d-enantiômero variam e diferem significativamente do racemato de anfetamina. Para norepinefrina, Ki = nM em um valor de 45-50, para dopamina 82-200, para 5-HT, os indicadores variam de 1840 a 3830 em modelos de cérebro de ratos. Um efeito mais "suave" do ciclo de dependência dessa forma de anfetamina é consequência de uma superexpressão relativamente menor de FosB no núcleo accumbens, da presença de efeitos positivos e da ausência de inibição de CREB por proteínas e serina fosfotases, precisamente devido à menor afinidade e influência nos sistemas glutamatérgicos e serotoninérgicos. Os efeitos neuroquímicos em comparação também têm uma capacidade distinta; nos estudos de Heal e Wickens, foram detectadas alterações na atividade motora, em que seu valor máximo foi de 3 a 4 vezes menor do que com a ingestão de cloridrato ou sulfato de anfetamina, o que está diretamente relacionado à taxa e à correção molecular do fluxo de saída da dopamina no estriado do cérebro.
Embora os experimentos in vitro forneçam uma boa visão dos mecanismos individuais, a eficácia da anfetamina em relação a outros agonistas indiretos de monoamina, por exemplo, os inibidores clássicos da recaptação, só pode ser estimada a partir de experimentos in vivo. Usamos a microdiálise intracerebral de sonda dupla para explorar os efeitos in vivo da d- e l-anfetamina no rato espontaneamente hipertenso (SHR), que foi proposto como modelo roedor de TDAH. Ambos os isômeros da anfetamina aumentaram de forma dependente da dose as concentrações extracelulares de noradrenalina no córtex pré-frontal (PFC) e de dopamina no estriado. A farmacodinâmica de seus efeitos é típica daquelas relatadas para agentes liberadores de monoamina, ou seja, um rápido início de ação com aumentos de pico de noradrenalina e efluxo de dopamina ocorrendo em 30-45 minutos, grandes efeitos (400-450% da linha de base para noradrenalina e 700-1500% da linha de base para dopamina), com um declínio relativamente rápido após o máximo. Embora nenhum resultado comparativo tenha sido incluído nesta revisão, a magnitude dos aumentos produzidos pelos isômeros da anfetamina é maior do que a relatada para os inibidores clássicos da recaptação, como a atomoxetina ou a bupropiona, e não há limite de dose-efeito para as ações da anfetamina.
Ao comparar os efeitos dos medicamentos sobre o efluxo de catecolaminas no CPF, é importante considerar a neuroanatomia altamente incomum dessa região cerebral. A densidade dos sítios DAT nos neurônios dopaminérgicos do CPF é muito baixa e, como consequência, a maior parte da dopamina liberada é sequestrada via NET nos neurônios noradrenérgicos. Embora existam poucos sítios DAT nos neurônios dopaminérgicos do CPF, sua capacidade de recaptação é suficiente para que a anfetamina provoque uma liberação substancial de dopamina, embora tenha sido sugerido que grande parte da liberação de dopamina no CPF provém de neurônios noradrenérgicos. Nos estudos de desenvolvimento da Shire em modelos in vivo, foi comprovada uma diferença estatisticamente significativa. O D-AMP influenciou os componentes cognitivos do controle impulsivo de forma diferente: a proporção de escolha impulsiva diminuiu com o mesmo nível de recompensa, o que também confirma a eficácia desse enantiômero.
Métodos de uso e doses.
A dosagem recreativa do d-enantiômero de anfetamina começa com 40-60 mg por via oral; em casos de tolerância presente, a dosagem inicial pode ser aumentada para 120-160 mg em uma única aplicação oral. Quando administrada por via intranasal, recomenda-se usar uma dose inicial de 30-50 mg. A administração parenteral dessa forma é permitida somente no caso de se obter uma solução pura. Quaisquer comprimidos ou pós são recomendados para uso apenas por administração oral e intranasal. Na administração parenteral, a dose inicial é de 0,15-0,24 mg/kg.
Apresentação clínica da intoxicação por anfetamina.
Os sintomas acima são "leves", sua gravidade é até 40% menor do que a da forma combinada. Portanto, efeitos negativos indesejáveis como dificuldade para urinar, distúrbios do ritmo cardíaco, aumento da frequência cardíaca, aumento da pressão arterial, aumento da sudorese, temperatura corporal elevada, náusea, dilatação da pupila ocorrem exclusivamente em altas doses e são proporcionalmente diferentes em comparação com o racemato.
1. Euforia e sensação de aumento de energia;
2. Vigília prolongada;
3. Ideias ou ações grandiosas;
4. Comportamento violento ou agressivo;
5. Viés de confirmação;
6. Labilidade do humor;
7. Comportamento caracterizado por estereótipos repetidos;
8. Ilusões auditivas, visuais ou táteis;
9. Distorção da personalidade;
10. Supressão do apetite.
Além disso, as pessoas que usam D-AMP devem apresentar pelo menos dois dos seguintes sinais para serem diagnosticadas:
1. Taquicardia;
2. Hipertensão arterial;
3. Sudorese e calafrios febris;
4. Náusea ou vômito;
5. Fraqueza muscular;
6. Dor ou desconforto atrás do esterno;
7. Agitação psicomotora;
8. Dilatação da pupila.
Os sintomas da intoxicação por D-AMP incluem principalmente sinais de complicações cardiovasculares e do sistema nervoso. Os distúrbios respiratórios ocorrem com menos frequência.
Distúrbios cardíacos: hipertensão e taquicardia são os mais comuns, quando se tomam doses baixas. A bradicardia inicial também é possível devido a um aumento no tônus parassimpático. As arritmias (supraventriculares são frequentes) podem ser causadas por uma crise simpática ou por um bloqueio dos canais rápidos de sódio. A isquemia e o infarto do miocárdio são causados por espasmo coronariano, que atinge o máximo 30 minutos após o uso de D-AMP intranasal e coincide com o pico de concentração da droga no sangue. Mais espasmos coronarianos podem se desenvolver após 90 minutos, o que está associado ao acúmulo de metabólitos de D-AMP. Um aumento na agregação plaquetária leva à formação de coágulos sanguíneos nos vasos coronários. Além disso, a demanda de oxigênio do miocárdio aumenta. Uma complicação rara é a ruptura da aorta.
Instruções especiais, interações com outras substâncias.
As contraindicações absolutas do uso de qualquer forma de anfetamina são: aterosclerose vascular grave, quaisquer doenças cardiovasculares sintomáticas, ingestão de MAO (e 14 dias após o último ato de uso de medicamento desse grupo), glaucoma, hipertireoidismo.
A regra "não-ADIOS":
Não alcoólicos - não é recomendado o uso com álcool.
Não dissociativos - não é recomendado o uso com drogas dissociativas.
Não-iMAO - não é recomendado o uso com inibidores da monoamina oxidase.
Não opiáceos - não é recomendado o uso com agonistas de receptores opiáceos.
Não estimulantes - não é recomendado o uso com estimulantes.
1. Ao usar o D-AMP junto com medicamentos do grupo dos inibidores da PDE-5, o risco de desenvolver efeitos colaterais de ambas as substâncias aumenta. Efeitos colaterais mais comuns: dor de cabeça intensa de natureza espástica, náusea. A incidência de desenvolvimento de condições críticas graves é baixa.
2. Ao usar o D-AMP junto com a maconha, há risco de aumento da pressão arterial, dor de cabeça, tremores finos e secura na boca. A probabilidade de desenvolvimento de condições críticas graves é baixa.
3. Ao usar o D-AMP com neurolépticos/tranquilizantes, há um alto risco de nivelamento dos principais efeitos do D-AMP. A probabilidade de desenvolvimento de condições críticas graves é baixa (nos casos em que não há contraindicações para o uso de neurolépticos).
4. Não é recomendado o uso de D-AMP durante o tratamento com medicamentos antibacterianos, antivirais e antifúngicos, hormônios e anticoagulantes.
5. Não é recomendado o uso do D-AMP durante qualquer manipulação cirúrgica e antes e depois disso por um determinado período (o período é identificado individualmente).
6. Não é recomendável usar D-AMP se for diagnosticado com qualquer distúrbio do sistema cardiovascular, dos rins, do fígado, dos pulmões e do sistema nervoso central.
7. Não é recomendado o uso de D-AMP durante a gravidez e a lactação.
Em dois estudos publicados anteriormente, Jasinski e Krishnan compararam os efeitos subjetivos da d-anfetamina IR em voluntários humanos com experiência com drogas quando esses compostos foram administrados por via intravenosa e oral. No estudo em que eles compararam esses compostos após a administração oral, a d-anfetamina IV (40 mg (29,6 mg de base de d-anfetamina)) evocou um aumento estatisticamente significativo em relação ao placebo em "Gosto pela droga" na escala do Questionário de Avaliação de Drogas - Sujeito (DQRS), enquanto a dose equivalente de d-anfetamina (100 mg, oral) não o fez. Além disso, o tempo do pico do efeito farmacológico da d-anfetamina foi substancialmente atrasado em comparação com a d-anfetamina IR, em 3,0 h versus 1,5-2,0 h. Quando a d-anfetamina foi administrada em uma dose maior de 150 mg, ela aumentou significativamente a pontuação do DQRS "Gosto pela droga" em uma extensão equivalente à d-anfetamina IR (40 mg oral). No entanto, o efeito de pico da dose mais alta de d-amfetamina foi ainda mais tardio, em 4,0 h. Quando a via intravenosa foi explorada, a d-anfetamina IV (20 mg intravenosa) produziu um pico de pontuação de "gosto pela droga" 20 minutos após a dosagem, que coincidiu com a Cmax plasmática. Em contraste, a dose equivalente de d-anfetamina (50 mg intravenosa) não aumentou significativamente o "gosto pela droga" em relação ao placebo, e a Cmax da d-anfetamina plasmática ocorreu consideravelmente mais tarde, às 2,0 h. Ambos os compostos produziram valores equivalentes de AUC0-24h, mas em comparação com a dose equivalente de d-anfetamina IR, a Cmax da d-anfetamina plasmática foi três vezes menor para a lisdexamfetamina e o tmax foi três vezes maior.
Primeiros socorros em caso de superdosagem.
O mecanismo de toxicidade está relacionado principalmente ao excesso de dopamina extracelular, norepinefrina e serotonina. A síndrome clínica primária envolve efeitos neurológicos e cardiovasculares proeminentes, mas as complicações secundárias podem envolver efeitos renais, musculares, pulmonares e gastrointestinais. Hiperatividade, hipertermia, taquicardia, taquipneia, midríase, tremores, convulsões e estado mental alterado são alguns dos sinais e sintomas mais comuns da intoxicação por anfetamina. O diagnóstico pode ser confirmado pela detecção de anfetamina no conteúdo estomacal ou no vômito, ou por exame toxicológico de urina positivo para drogas ilícitas. Uma triagem de anfetamina falso-positiva pode ocorrer após uma overdose de trazodona ou de bupropiona. Não há antídoto para a toxicidade da anfetamina; entretanto, o carvão ativado é um tratamento de emergência. Em pacientes que podem beber com segurança, a recomendação é administrar carvão ativado de 1 a 2 g/kg até 100 g por via oral se a ingestão tiver ocorrido na última hora. A toxicidade relacionada à anfetamina requer tratamento por meio do controle dos sinais cardiovasculares e do sistema nervoso central que ameaçam a vida em um ambiente tranquilo.
Indicações para ir ao hospital ou chamar uma ambulância: consciência prejudicada ou ausente, fala prejudicada, atividade motora, falta de orientação no espaço e no tempo, dor intensa atrás do esterno que dure mais de meia hora, aumento da temperatura corporal de mais de 38,0 C ou hipertermia que dure mais de meia hora, aumento da pressão arterial de mais de 180/110 mmHg sem efeito de terapia hipotensiva.
1. O tratamento de pacientes com pressão arterial superior a 140/95 mm Hg inclui um comprimido de betabloqueador sem atividade simpaticomimética intrínseca, um comprimido de inibidor da ECA e, após 30 minutos, um comprimido de tranquilizante (0,25 mg de alprazolam).
2. Em pacientes com ansiedade intensa, ataque de pânico, psicose: um comprimido de um tranquilizante e um comprimido de um neuroléptico com efeito sedativo, ajuda psicológica, psicoterapia de emergência.
3. Em pacientes com dor no esterno, desconforto no peito: um comprimido de bloqueadores lentos dos canais de cálcio da terceira geração, reduzindo reflexivamente a frequência cardíaca, um comprimido de um inibidor da ECA da terceira geração OU um comprimido de um agonista dos efeitos da imidazolina OU um comprimido; se a síndrome da dor não se tornar menos intensa em 20 minutos, recomenda-se ir ao hospital.
4. Quando houver um aumento na temperatura corporal não superior a 37,5 °C, recomenda-se a observação dinâmica por meia hora. Não é necessário tratamento farmacológico. Se a hipertermia persistir por mais de meia hora (na ausência de causas externas), recomenda-se ir ao hospital.
5. Em pacientes com dores de cabeça intensas, recomenda-se o uso de antiespasmódicos em combinação com remédios fitoterápicos sedativos ou tranquilizantes em doses baixas. Se a cefaleia estiver associada a vômitos, recomenda-se uma injeção intramuscular de metoclopramida 2,0 ml. A náusea isolada e a dispepsia funcional não requerem tratamento farmacológico.
6. Para tremores, convulsões moderadas ou agitação psicomotora leve, recomenda-se o uso de tranquilizantes. É altamente recomendável não usar neurolépticos nesses casos.
Um betabloqueador, como o propranolol, pode ajudar a controlar as taquiarritmias cardíacas. Considere o uso de nitroprussiato intravenoso (comece com 0,5 a 1 mcg/kg por minuto e aumente conforme necessário) para hipertensão grave. Deve-se administrar fluido intravenoso, pois ele combate a hipertermia, auxilia na manutenção da função renal e ajuda a promover a eliminação da anfetamina e seus análogos. Em casos de agitação grave, os médicos devem considerar um tratamento agressivo para evitar hipertensão maligna, rabdomiólise, hipertermia e convulsões. As evidências apóiam o uso de grandes doses de benzodiazepínicos para tratar a psicose e a agitação relacionadas à overdose de anfetaminas. Nos casos em que a agitação, o delírio e os distúrbios de movimento não respondem aos benzodiazepínicos, as terapias de segunda linha incluem antipsicóticos, como ziprasidona ou haloperidol, agonistas centrais de alfa-adrenorreceptores, como dexmedetomidina, ou propofol. A paralisia neuromuscular, a intubação e as medidas de resfriamento ativo podem ser necessárias em casos graves. Em pacientes com taquicardia, faça um ECG e considere a possibilidade de telemetria. Use fluidos intravenosos e sedação para controlar os sintomas cardíacos. Em casos de hipertensão grave, considere nitroprussiato intravenoso. Iniciar solução salina normal a 0,9% e monitorar a creatina quinase (CK), os eletrólitos e a creatinina é a melhor maneira de controlar a rabdomiólise.
Há relatos de casos sobre a cardiomiopatia de Takotsubo (TTC), também conhecida como cardiomiopatia induzida por estresse, que é desencadeada por overdose de anfetaminas. Em um caso, um paciente foi ao departamento de emergência após ingerir 30 comprimidos de sal de anfetamina com sintomas de dor no peito e falta de ar. No momento da apresentação, as enzimas cardíacas estavam elevadas, o eletrocardiograma não apresentava alterações e a fração de ejeção (FE) era de 25% a 30% com hipocinesia grave. No entanto, 24 horas depois, os sintomas foram resolvidos e um ecocardiograma repetido, realizado três dias depois, mostrou uma FE de 60%, sem anormalidades regionais de movimento da parede.
Termos de detecção e regras de armazenamento.
Como regra geral, o armazenamento do racemato de anfetamina, bem como do d-enantiômero, deve ser feito em local protegido da luz e da umidade, de preferência em temperatura ambiente ou a uma temperatura de pelo menos 5 °C e não mais de 40 °C. Pode ser armazenado em papel alimentício ou em embalagens de polietileno tereftalato sem conteúdo metálico.
Após um único uso intranasal de dextroanfetamina, o período de detecção na urina, quando se usam métodos expressos de pesquisa, é de aproximadamente 46 a 72 horas, com uso oral de até 120 a 220 horas. O uso sistemático prolongado de dextroanfetamina não foi estudado no contexto da identificação de metabólitos, embora, teoricamente, se saiba que há uma grande chance de detectar os principais metabólitos por PFIA ou cromatografia-espectrometria de massa durante 1,5 a 2 meses após o último uso de anfetamina (que é menor do que o racemato de anfetamina). O período de detecção dos metabólitos da dextroanfetamina no cabelo é de até 2,5 a 3 meses.
Last edited:
