G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,793
- Solutions
- 3
- Reaction score
- 3,057
- Points
- 113
- Deals
- 1
Bevezetés
A lizergsavat, az anyarozs-alkaloidokból származó alapfragmentumot tizennégyszeres sorrendben szintetizálták, kezdve a 3-béta-karboxi-etilindollal. A kiindulási anyagot az 1-benzoil-5-keto-1,2,2a-3,4,5-hexahidrobenz-[cd]-indol (3) intermedierré alakították át, amely a lizergsavban található négy gyűrűből hármat tartalmaz. Ez a keton viszont átalakult a tetraciklusos vegyület, a 9-keto-7-metil-4,5,5,5a,6,6a,7,8,9-oktahidroindolo-[4.3-fe]-kinolin (8), és onnan a lizergsav (14). Ez a szintézis nem egyszerű, és nagy laboratóriumi tapasztalatot és kémiai ismereteket igényel. Ráadásul számos veszélyes anyaggal való manipuláció is előfordul, amelyeket szigorú biztonsági intézkedések mellett kell elvégezni.
forráspont: 536,2 ± 50,0 °C 760 mm Hg nyomáson;
olvadáspont: 240 °C;
molekulatömeg: 268,31 g/mol;
sűrűség: 1,4 ± 0,1 g/ml;
CAS-szám: 82-58-6.
Berendezések és üvegeszközök:
- Acél hidrogénezési reaktor 2-3 L;
- Acél autokláv 500 ml;
- Laboratóriumi mérleg (0,01 - 500 g alkalmas);
- 100, 200, 500 ml-es, 5 és 10 l-es kerekfenekű lombikok;
- Hidrogén (H2) kompresszor és eredet;
- Buchner-lombik és tölcsér (nagy) 5 L [kis mennyiségekhez Schott-szűrő használható];
- Rotovap gép (nagy);
- Vákuumforrás;
- 500 ml-es és 2 l-es elválasztótölcsérek;
- Nitrogénballon ~50-70 L (1 bar);
- Szeptumkupakok a lombikokhoz;
- Sós jeges vízfürdő;
- 5 L x2, 2 L x2; 1 L x2; 500 ml x2; 100 ml x3; 50 ml x2 főzőpoharak;
- Üvegfecskendő vagy Pasteur-pipetta;
- Mágneses keverő vagy felső keverő;
- Vákuumdesztillációs berendezés;
- Reflux kondenzátor;
- Retortaállvány és bilincs a készülék rögzítéséhez;
- Laboratóriumi hőmérő (-20 °C-tól 200 °C-ig) lombikadapterrel;
- pH-indikátor papír;
- Üvegrúd és spatula;
- 250 wattos izzó.
Reagensek.
- 3-Indolepropionsav (1), 94,6 g (0,5 mol);
- 9,5 l desztillált víz (H2O);
- ~400 g nátrium-hidroxid (NaOH);
- 116 g Raney-nikkel (Ni);
- 1050 ml sósav (HCl) koncentrált;
- 2 mL kénsav (H2SO4 koncentrált);
- 210 ml 12N nátrium-hidroxid (NaOH) aq oldat;
- 180 mL benzoil-klorid;
- ~1,5 L metanol (MeOH);
- ~1,6 L etanol (EtOH);
- 201,2 mL tionil-klorid (SOCl2);
- 1950 mL Szén-diszulfid (CS2);
- 240 g alumínium-klorid (AlCl3);
- 2,5 L benzol;
- 500 ml 2N nátrium-hidroxid (NaOH);
- ~3,2 L Dietil-éter (Et2O);
- 3,3 L jégecetsav (AcOH);
- 352 g (1,1 mol) piridin-hidrobromid perbromid;
- 5 L kloroform (CHCl3);
- ~1000 g magnézium-szulfát (MgSO4);
- 307 g (2,35 mol) Metil-aminoaceton-etilén-ketál (5);
- 4,5 L benzol;
- ~500 g Aktív szén (C);
- ~1 L aceton;
- ~500 g nátrium-hidrogénkarbonát (NaHCO3);
- 80 ml Hideg ecetsav-anhidrid (Ac2O);
- 1,5 g nátrium-borohidrid (NaBH4);
- 75 ml Kén-dioxid (SO2 folyadék);
- 40 g nátrium-cianid (NaCN por);
- 300 ml hidrogén-cianid (HCN folyadék);
- 78 mL 1,5%-os kálium-hidroxid (KOH) vizes oldat;
- 8,5 g Hidratált nátrium-arzenát;
- ~ 50 mL xilol;
- 100 mL Ammónium-hidroxid (NH4OH) híg oldat;
- 16,9 g nátrium-metoxid (MeONa).
Eljárás
1-Benzoil-3-(béta-karboxietil)-2,3-dihidroindol (2)A 94,6 g (0,5 mol) 3-Indolpropionsavat (1) 600 ml vízben oldottuk, amely 20 g nátrium-hidroxidot tartalmazott. Az oldatot kb. 100 g Raney-nikkel katalizátorral kevertük, és RT-nél 2-3 literes acél hidrogénezőbombában 3000-4000 psi (207-276 bar) H2 nyomáson hidrogéneztük. A redukció általában 20-30 óra alatt befejeződött, majd a katalizátort leszűrtük és kevés vízzel mostuk. A szűrlethez 85 ml tömény HCl-savat adtunk, és az oldatot lehűtöttük. Ha a redukció nem volt teljes, a nem reagált indolpropionsav ekkor levált, és szűréssel eltávolítottuk. A szűrletet ezután a szokásos Schotten-Baumann-eljárással benzoileztük 210 ml 12N nátrium-hidroxid és 180 ml benzoil-klorid felhasználásával. Az oldatot a benzoilezés során végig lúgosnak tartottuk, és a hőmérsékletet hűtéssel 40 °C alatt tartottuk. Amikor a benzoil-klorid teljesen reagált, az elegyet lehűtöttük és 300 ml tömény HCl-savval savasítottuk. A nyers terméket szűrtük és vízzel mostuk, majd 4 x 1 L adag forró vízzel extraháltuk a benzoesav eltávolítása érdekében. A forró, szirupszerű terméket (2) avizes kivonat dekantálása után néhány térfogat metanolból kristályosítottuk; hozam 103 g (70 %), MP: 151-153 °C.
1-Benzoil-5-keto-1,2,2a,3,4,5-hexahidrobenz-[cd]-indol (3)
1-Benzoil-3-(béta-karboxietil)-2,3-dihidroindol (2), 118 g (0,4 mol), 200 ml tiszta tionil-kloriddal kevertük. Az oldatot 30 percig állni hagytuk, majd 15-20 percig óvatosan melegítettük gőzfürdőn. A felesleges tionil-kloridot 30 °C alatt vákuumban teljesen bepároltuk, és a nyers sav-kloridot 200 mL szén-diszulfidban feloldottuk. A sav-klorid oldatát ezután vékony sugárban hozzáadtuk egy 5 L-es lombikban (HOOD-ban!!!) lévő 240 g alumínium-klorid 1750 mL szén-diszulfidban lévő, erőteljesen kevert szuszpenziójához. A komplex elvált, és a keverés nehézkessé vált. Az elegyet reflux alatt melegítettük és egy órán át kevertettük a reakció befejezéséhez, majd 500 g jég, 250 ml conc. HCl-sav és 500 ml víz hozzáadásával nagyon óvatosan bontottuk. A bomlás alatt a keverést fenntartottuk, a hűtést a széndiszulfid időszakos vákuumdesztillációjával befolyásoltuk, és a terméket 2 L benzollal extraháltuk. A kivonatot három részletben 500 mL 2N nátrium-hidroxiddal, majd vízzel alaposan mostuk. Magnézium-szulfáton megszárítottuk, majd vákuumban kis térfogatra bepároltuk. Több térfogatnyi éter lassú hozzáadásával a sárga keton (3 ) kikristályosodott. Szűrtük és éterrel mostuk; hozama 85,3 g (77 %), MP: 146-147 °C. Egy mintát átkristályosítottunk benzol-éterből történő elemzés céljából.
1-Benzoil-3-(béta-karboxietil)-2,3-dihidroindol (2), 118 g (0,4 mol), 200 ml tiszta tionil-kloriddal kevertük. Az oldatot 30 percig állni hagytuk, majd 15-20 percig óvatosan melegítettük gőzfürdőn. A felesleges tionil-kloridot 30 °C alatt vákuumban teljesen bepároltuk, és a nyers sav-kloridot 200 mL szén-diszulfidban feloldottuk. A sav-klorid oldatát ezután vékony sugárban hozzáadtuk egy 5 L-es lombikban (HOOD-ban!!!) lévő 240 g alumínium-klorid 1750 mL szén-diszulfidban lévő, erőteljesen kevert szuszpenziójához. A komplex elvált, és a keverés nehézkessé vált. Az elegyet reflux alatt melegítettük és egy órán át kevertettük a reakció befejezéséhez, majd 500 g jég, 250 ml conc. HCl-sav és 500 ml víz hozzáadásával nagyon óvatosan bontottuk. A bomlás alatt a keverést fenntartottuk, a hűtést a széndiszulfid időszakos vákuumdesztillációjával befolyásoltuk, és a terméket 2 L benzollal extraháltuk. A kivonatot három részletben 500 mL 2N nátrium-hidroxiddal, majd vízzel alaposan mostuk. Magnézium-szulfáton megszárítottuk, majd vákuumban kis térfogatra bepároltuk. Több térfogatnyi éter lassú hozzáadásával a sárga keton (3 ) kikristályosodott. Szűrtük és éterrel mostuk; hozama 85,3 g (77 %), MP: 146-147 °C. Egy mintát átkristályosítottunk benzol-éterből történő elemzés céljából.
1-Benzoyl-4-bromo-5-keto-1,2,2a,3,4,5-hexahydrobenz-[cd]-indole (4)
1-Benzoil-2,2a,3,4-tetrahidro-4-[metil-(2-metil-1,2-dioxolan-2-il-metil)-amino]-benz-[cd]-indol-5-(1H)-on (6)
Az 1-benzoil-4-brom-5-keto-1,2,2a,3,4,5-hexahidrobenz-[cd]-indol(4) 270 g (0,76 mol) és 307 g (2.35 mol) metilaminoaceton-etilén-ketál (5) 4500 ml száraz benzolban nitrogén alatt 21 órán át refluxáltuk 10 L RBF-ben, refluxkondenzátorral. Az elegyet lehűtöttük, és 151 g (93,5 %) metilaminoaceton-etilénketál-hidrobrómidot szűrtünk, MP: 158-159 °C.
A szűrletet többször mostuk jeges vízzel, majd 2,5 L hideg, híg HCl-savval extraháltuk, amely 150 ml koncentrált savat tartalmazott. A savas kivonatokhoz azonnal hozzáadtuk a jéghideg hígított nátrium-hidroxidot. A terméket 1 L kloroformmal extraháltuk, majd a kloroformos oldatot magnézium-szulfáton szárítottuk, szénnel kezeltük és vákuumban koncentráltuk. A visszamaradt ketál-keton (6 ) acetonból kristályosodott; MP: és keverék MP: 135-136 °C, hozam 220 g (71 %).
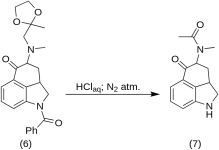
5-Keto-4-[N-metil-N-acetonylamino]-1,2,2a,3,4,5-hexahidrobenz-[cd]-indol (7)
20 g 1-benzoil-2,2a,3,4-tetrahidro-4-[metil-(2-metil-1,3-dioxolán-2-il-metil)-amino]-benz-[cd]-indol-5-(1H)-on (6 ) 250 ml tömény HCl-sav és 250 ml víz keverékében oldottuk, majd az oldatot 3-5 L RBF-ben öt napig nitrogén alatt, 37 °C-on tartottuk 3-5 L RBF-ben. Az elegyet lehűtöttük, szénnel kezeltük, szűrtük, és a szűrletet vákuumban kis térfogatra koncentráltuk. A maradékot felesleges nátrium-hidrogénkarbonáttal kezeltük; a terméket hideg kloroformmal extraháltuk, és az oldószert vákuumban, RT-n eltávolítottuk. A nyers diketont (7 ) porítottuk, kb. 75 ml 1:1 arányú benzol-éterrel felitattuk, majd szűrtük; hozama 9,8 g (77 %), MP: 105-107 °C. Azelemzéshez szükséges mintát benzol-éterből vagy etanolból átkristályosítottuk; MP: 109-110 °C; híg etanolból monohidrokloridot kaptunk; MP: 200 °C dec.
9-Keto-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (8)
25 g 5-Keto-4-[N-metil-N-acetonil]-amino-1,2,2a,3,4,5-hexahidrobenz-[cd]-indolt (7 ) 550 ml abszolút etanollal kevertünk. Az elegyet nitrogén alatt kevertettük és 2-5 L RBF-ben -15 °C-ra hűtöttük. Ezután 16,9 g nátrium-metoxidot adtunk hozzá, majd az elegyet -10 °C és -12 °C között tíz percig kevertettük. A reakcióelegyet -25 °C-ra hűtöttük, majd a terméket 6,5 hüvelykes buchner-tölcséren szűrtük, és kevés hideg etanollal és éterrel mostuk. A nyers keton (8 ) a lehető legkevesebb levegővel való érintkezés mellett (nátrium-metoxidot tartalmaz!) azonnal felitattuk kevés jeges vízzel, és újraszűrtük. Jeges vízzel, etanollal és éterrel mostuk; hozam 16,2 g (69 %), MP: 145-147 °C. Egy analitikus mintát híg etanolból átkristályosítottunk; MP: 155-157 °C; A dihidrokloridot vizes acetonból készítettük és átkristályosítottuk; MP: 270 °C dec.
4-Acetil-9-keto-7-metil-4,5,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (9)
9-Keto-7-metil-4,5,5,5a,6,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (8), 24 g, 80 ml hideg ecetsav-anhidridhez adtuk. Az elegyet 200 mL RBF-ben 25 °C-on tartottuk kb. 5 percig, majd alaposan lehűtöttük, és a terméket (9 ) leszűrtük és éterrel mostuk; hozam 20,5 g (76 %), mp: 167-170 °C. A szűrlet bepárlásával egy második termést kaptunk; ez a teljes hozamot 82%-ra növelte. Egy mintát aceton-etanolból átkristályosítottunk; MP: 169-170 °C; A hidrokloridot etanolban készítettük és vizes etanolból átkristályosítottuk; MP: 250 °C dec.
9-Keto-7-metil-4,5,5,5a,6,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (8), 24 g, 80 ml hideg ecetsav-anhidridhez adtuk. Az elegyet 200 mL RBF-ben 25 °C-on tartottuk kb. 5 percig, majd alaposan lehűtöttük, és a terméket (9 ) leszűrtük és éterrel mostuk; hozam 20,5 g (76 %), mp: 167-170 °C. A szűrlet bepárlásával egy második termést kaptunk; ez a teljes hozamot 82%-ra növelte. Egy mintát aceton-etanolból átkristályosítottunk; MP: 169-170 °C; A hidrokloridot etanolban készítettük és vizes etanolból átkristályosítottuk; MP: 250 °C dec.
4-Acetil-9-hidroxi-7-metil-4,5,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (10)
10 g 4-acetil-9-keto-7-metil-4,5,5,5a,6,6a,7,8,9-oktahidroxindolo-[4,3-fg]-kinolin (9 ) 150 ml metanol és 10 ml víz keverékéhez adtuk 500 ml RBF-ben. Hozzáadtunk 1,5 g nátrium-borohidridet, és a reakciót RT-n kis térfogatig hagytuk folyni, majd 15 mL conc. HCl-sav és 60 mL víz keverékét adtuk hozzá. A hűtéskor elvált hidrokloridot (10 ) leszűrtük és metanollal mostuk, 9,0 g (79 %). Egy mintát híg etanolból átkristályosítottunk; MP: 245-246 °C dec.
4-Acetil-9-klór-7-metil-4,5,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin-hidroklorid (11)
4-Acetil-9-hidroxi-7-metil-4,5,5,5a,6,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin-hidroklorid (10), 3. A 4-Acetil-9-hidroxi-7-metil-4,5,5a,6,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin-hidroklorid (10), 3.1 g-ot feloldottunk 75 ml folyékony kén-dioxidban, amely egy 500 ml-es acél autoklávban üvegbélésben volt. Tionil-kloridot, 1,2 mL-t adtunk hozzá, majd az edényt lezártuk és 6 órán át 25 °C-on tartottuk. Az autoklávot légtelenítettük, és a reakcióelegyet eltávolítottuk. A kén-dioxidot hagytuk elpárologni, miközben az oldat térfogatát száraz éter lassú hozzáadásával állandó értéken tartottuk. Az amorf klór-hidrokloridot (11 ) leszűrtük, éterrel mostuk és vákuumban szárítottuk, MP: 130-135 °C dec. hozam 3,5 g. A9-béta-epimer alkohol felhasználása ebben a reakcióban hasonló hozammal adta ugyanazt a kloridot.
4-Acetil-9-ciano-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (12)
Száraz, porított nátrium-cianidot, 40 g-ot adtunk 300 ml jéghideg folyékony hidrogén-cianidhoz. Az elegyet kevertettük és jégben lehűtöttük, majd 7,5 g nyers amorf 4-acetil-9-klór-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo[4,3f/g]-kinolin-hidrokloridot (11 ) adtunk hozzá. A keverést 500 ml RBF-ben 30 percig folytattuk, majd a hidrogén-cianidot csökkentett nyomáson, kb. 10 °C alatt gyorsan desztilláltuk. A maradékot kloroformmal és jeges vízzel kevertük, majd a kapott keveréket szűrtük. A szerves réteget elválasztottuk, és a vizes fázist kétszer kloroformmal extraháltuk. Az egyesített kivonatokat magnézium-szulfáton szárítottuk, színtelenítettük és az oldószert vákuumban desztilláltuk. A terméket (12 ) etil-acetátból kristályosítottuk; hozama 3,3 g (54%-os összmennyiség, az alkohol-hidrokloridra vonatkoztatva), m.p. 172-174 °C. Ugyanebből az oldószerből történő átkristályosítással a m.p. 181-182 °C-ra emelkedett.
Száraz, porított nátrium-cianidot, 40 g-ot adtunk 300 ml jéghideg folyékony hidrogén-cianidhoz. Az elegyet kevertettük és jégben lehűtöttük, majd 7,5 g nyers amorf 4-acetil-9-klór-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo[4,3f/g]-kinolin-hidrokloridot (11 ) adtunk hozzá. A keverést 500 ml RBF-ben 30 percig folytattuk, majd a hidrogén-cianidot csökkentett nyomáson, kb. 10 °C alatt gyorsan desztilláltuk. A maradékot kloroformmal és jeges vízzel kevertük, majd a kapott keveréket szűrtük. A szerves réteget elválasztottuk, és a vizes fázist kétszer kloroformmal extraháltuk. Az egyesített kivonatokat magnézium-szulfáton szárítottuk, színtelenítettük és az oldószert vákuumban desztilláltuk. A terméket (12 ) etil-acetátból kristályosítottuk; hozama 3,3 g (54%-os összmennyiség, az alkohol-hidrokloridra vonatkoztatva), m.p. 172-174 °C. Ugyanebből az oldószerből történő átkristályosítással a m.p. 181-182 °C-ra emelkedett.
9-Karbometoxi-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (13)
Az imént említett (12) terméket (1,0 g) 15 ml metanollal és 0,25 ml vízzel kevertük. Az elegyet lehűtöttük, és lassan 2 mL tömény kénsavat adtunk hozzá. Az oldatot üvegcsőbe zártuk nitrogén alatt, és 100 °C-on 23-24 órán keresztül 100 mL RBF-ben, refluxkondenzátorral 23-24 órán keresztül melegítettük. Az elegyet színtelenített szénnel kezeltük, majd vákuumban kb. 10 mL-re koncentráltuk. Kloroform (30 mL), jég és 10 g nátrium-hidrogénkarbonát keverékére öntöttük. A kloroformréteget elválasztottuk, és a vizes fázist 3 x 10 mL kloroformmal extraháltuk. Az egyesített kivonatokat magnézium-szulfáton szárítottuk, szárazra pároltuk, és a terméket (13 ) benzolból kristályosítottuk; hozama 0,51 g (53 %), MP: 159-160 °C. Etil-acetátból átkristályosítottuk; MP: 160-161 °C.
Az imént említett (12) terméket (1,0 g) 15 ml metanollal és 0,25 ml vízzel kevertük. Az elegyet lehűtöttük, és lassan 2 mL tömény kénsavat adtunk hozzá. Az oldatot üvegcsőbe zártuk nitrogén alatt, és 100 °C-on 23-24 órán keresztül 100 mL RBF-ben, refluxkondenzátorral 23-24 órán keresztül melegítettük. Az elegyet színtelenített szénnel kezeltük, majd vákuumban kb. 10 mL-re koncentráltuk. Kloroform (30 mL), jég és 10 g nátrium-hidrogénkarbonát keverékére öntöttük. A kloroformréteget elválasztottuk, és a vizes fázist 3 x 10 mL kloroformmal extraháltuk. Az egyesített kivonatokat magnézium-szulfáton szárítottuk, szárazra pároltuk, és a terméket (13 ) benzolból kristályosítottuk; hozama 0,51 g (53 %), MP: 159-160 °C. Etil-acetátból átkristályosítottuk; MP: 160-161 °C.
Szintetikus dl-lizergsav (14)
9-karbometoxi-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (13), 3,9 g és 78 ml 1,5%-os kálium-hidroxid-oldat keverékét 30 percig refluxáltuk nitrogén alatt. Hidratált nátrium-arzenátot, 8,5 g-ot és a korábban xilolszuszpenzióban forralással inaktivált Raney-nikkel (16 g, nedves) adtunk hozzá, majd az elegyet reflux alatt melegítettük és nitrogén atmoszférában 20 órán át kevertettük 200 mL RBF-ben, reflux kondenzátorral. Az oldatot szénnel kezeltük, és a nyers lizergsavat (14 ) pH 5,6-ra történő semlegesítéssel kicsaptuk. Szűrtük és vízzel mostuk; hozam 1,04 g, MP: 240-242 °C dec. Egy második termést, 0,16 g, MP: 233-235 °C dec. szintén kaptunk; teljes hozam 30%. A sav tisztítható volt híg ammónium-hidroxidban oldva, színtelenítő szénnel kezelve és szén-dioxiddal újra kicsapva, MP: 242-243 °C dec.; a természetes d-liszergsavból készült dl-liszergsavval való keverék szintén 242-243 °C dec. A vízmentes savat több órás 150 °C-os vákuumszárítással nyertük.
9-karbometoxi-7-metil-4,5,5a,6,6a,7,8,9-oktahidroindolo-[4,3-fg]-kinolin (13), 3,9 g és 78 ml 1,5%-os kálium-hidroxid-oldat keverékét 30 percig refluxáltuk nitrogén alatt. Hidratált nátrium-arzenátot, 8,5 g-ot és a korábban xilolszuszpenzióban forralással inaktivált Raney-nikkel (16 g, nedves) adtunk hozzá, majd az elegyet reflux alatt melegítettük és nitrogén atmoszférában 20 órán át kevertettük 200 mL RBF-ben, reflux kondenzátorral. Az oldatot szénnel kezeltük, és a nyers lizergsavat (14 ) pH 5,6-ra történő semlegesítéssel kicsaptuk. Szűrtük és vízzel mostuk; hozam 1,04 g, MP: 240-242 °C dec. Egy második termést, 0,16 g, MP: 233-235 °C dec. szintén kaptunk; teljes hozam 30%. A sav tisztítható volt híg ammónium-hidroxidban oldva, színtelenítő szénnel kezelve és szén-dioxiddal újra kicsapva, MP: 242-243 °C dec.; a természetes d-liszergsavból készült dl-liszergsavval való keverék szintén 242-243 °C dec. A vízmentes savat több órás 150 °C-os vákuumszárítással nyertük.
Attachments
Last edited: