G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,991
- Solutions
- 3
- Reaction score
- 3,380
- Points
- 113
- Deals
- 1
Introduction
Lors de la synthèse de la méphédrone (4-MMC) et d'autres substances psychoactives, différents solvants sont utilisés à différentes étapes (synthèse et purification). Ils restent sous la même forme qu'avant les synthèses. Cependant, ils sont mélangés à des saletés et leur utilisation sans un nettoyage important (régénération) dans les synthèses à venir est impossible. La part de ces solvants dans les déchets est d'environ 50 %. Presque tous ces solvants peuvent être restaurés et réutilisés. Il s'agit d'une part assez importante du coût du produit, et la régénération peut réduire les risques.
- Certains solvants sont contrôlés par les gouvernements (l'acétone, par exemple) et il est préférable de ne pas les acheter à nouveau. Ceux qui ne sont pas contrôlés ne valent pas non plus la peine d'être rachetés.
- Réduction des déchets. Chaque 5 kg de méphédrone génère jusqu'à ~ 75 kg de déchets (en fait plus avec l'eau), réduire ce chiffre de moitié apporte également un plus en termes de sécurité.
En général, si vous vous intéressez sérieusement à la synthèse de la méphédrone, vous devez garder ce sujet à l'esprit. Nous parlerons ici de la régénération des solvants que nous utilisons, à savoir.
1. L'alcool isopropylique (IPA)
2. Ledichlorométhane (DCM)
3. Acétone
4. Ortho-xylène (substitut moins inoffensif du benzène et du toluène)
6. Benzène
Il ne sera pas possible de régénérer 100 % des solvants. Mais réduire les achats de 10 fois (si 90% sont régénérés) est également une tâche très correcte et pratique.
1. IPA
La purification des produits à l'aide d'IPA génère une grande quantité de déchets d'IPA. L'IPA est également utilisé pour laver un produit solide. Par exemple, après la solidification, lorsque l'utilisation de l'acétone n'est pas très bonne car elle réagit avec l'acide restant, colorant le produit de toutes les couleurs de l'arc-en-ciel. Après la purification de la méphédrone, l'IPA se présente principalement sous la forme d'un mélange avec de l'eau (que l'IPA aide à expulser du mélange).
En premier lieu, je recommande de distiller l' IPA, dont le point d'ébullition est de 82,5 °C. Si vous n'avez pas besoin d'un IPA très pur, ou si vous êtes certain qu'il ne contient pas de pollution, vous pouvez vous contenter des actions suivantes sans distillation.
Ce mélange eau-IPA est régénéré très simplement : on y verse du chlorure de calcium (anhydre), que l'on trouve sans problème dans tous les magasins de produits chimiques, à raison de 1 kg de CaCl2 pour 10 litres de mélange et on mélange bien (on peut le faire en secouant le récipient). Fermez hermétiquement le récipient contenant l'IPA et mettez-le au congélateur (pour la nuit), car l'extraction de l'eau de l'IPA se fait mieux au froid. Après 6-8 heures, le mélange est retiré du congélateur, tandis que le chlorure de calcium "gèle" en une masse dense. L'IPA sec est filtré à partir du sédiment. Les 5 à 10 % restants de l'IPA sont troubles (contenant la suspension de CaCl2), la solution peut être drainée avec précaution ou filtrée sur un entonnoir à travers un filtre en papier ordinaire. Les impuretés présentes dans cet IPA (telles que les résidus de DCM ou l'acétone) n'affectent pas les performances de l'IPA lors des nettoyages ultérieurs. Étant donné que l'IPA est consommé plus que tous les autres solvants (jusqu'à 33 litres pour 5 kg de méphédrone), il s'agit de la récupération la plus efficace.
En premier lieu, je recommande de distiller l' IPA, dont le point d'ébullition est de 82,5 °C. Si vous n'avez pas besoin d'un IPA très pur, ou si vous êtes certain qu'il ne contient pas de pollution, vous pouvez vous contenter des actions suivantes sans distillation.
Ce mélange eau-IPA est régénéré très simplement : on y verse du chlorure de calcium (anhydre), que l'on trouve sans problème dans tous les magasins de produits chimiques, à raison de 1 kg de CaCl2 pour 10 litres de mélange et on mélange bien (on peut le faire en secouant le récipient). Fermez hermétiquement le récipient contenant l'IPA et mettez-le au congélateur (pour la nuit), car l'extraction de l'eau de l'IPA se fait mieux au froid. Après 6-8 heures, le mélange est retiré du congélateur, tandis que le chlorure de calcium "gèle" en une masse dense. L'IPA sec est filtré à partir du sédiment. Les 5 à 10 % restants de l'IPA sont troubles (contenant la suspension de CaCl2), la solution peut être drainée avec précaution ou filtrée sur un entonnoir à travers un filtre en papier ordinaire. Les impuretés présentes dans cet IPA (telles que les résidus de DCM ou l'acétone) n'affectent pas les performances de l'IPA lors des nettoyages ultérieurs. Étant donné que l'IPA est consommé plus que tous les autres solvants (jusqu'à 33 litres pour 5 kg de méphédrone), il s'agit de la récupération la plus efficace.
2. DCM
La récupération du DCM (CH2Cl2) est plus difficile en raison des mesures de sécurité strictes. En effet, lors de la distillation du DCM avec de l'eau, le DCM est partiellement oxydé par l'oxygène atmosphérique, formant un gaz assez toxique - le formaldéhyde. Si quelqu'un l'ignore, il s'agit du principal "facteur nuisible" de l'alcool méthylique, qui se décompose dans l'organisme en ce composé, responsable de tous les empoisonnements. Par conséquent, le travail de distillation du DCM doit être effectué strictement dans un système fermé, la sortie du condenseur doit se faire directement dans la hotte ou la sonde d'aspiration avec une bonne vitesse d'aspiration.
Le DCM contaminé est versé dans un ballon de distillation et porté à ébullition. Le DCM bout à 40 °C et son azétrope avec l'eau à 38 °C. Il bout violemment, avec des "explosions", donc ne versez pas plus de la moitié ou du tiers du volume du ballon de rb. Je vous conseille également d'utiliser des copeaux d'ébullition, tels que des tasses en porcelaine cassées, des carreaux brisés. Au fur et à mesure que le mélange s'évapore, la température du mélange augmente très rapidement, de nouvelles portions de DCM sale sont ajoutées, les pollutions sont concentrées, environ 1/10 du DCM reste avec cette saleté dans le ballon d'évaporation. Ensuite, il est égoutté, et le ballon, dans un masque à gaz ( !), est lavé avec quelques restes d'acétone ou/et d'IPA, des prunes sont utilisées. On obtient ainsi jusqu'à 80-90 % de DCM, qui est un solvant assez difficile à obtenir, et même lourd (1,3 kg par litre).
Le DСM secondaire obtenu est gris, parfois même jaunâtre, ce qui n'empêche pas de le réutiliser. Il contient de l'eau, ce qui n'est pas non plus gênant car tous les processus impliquant du DСM comprennent également des solutions aqueuses. Après la distillation, le DCM doit être lavé des restes d'IPA (ce qui se produit) et de formaldéhyde.
La procédure est la suivante : Le DCM est versé dans le ballon (réacteur), la même quantité d'eau distillée, le mélange est agité, la solution est divisée en couches, la couche de DCM est drainée. La même eau peut être utilisée pour laver 3-4 lots de DCM, les restes de formaldéhyde et d'IPA sont parfaitement solubles dans l'eau, et pendant la séparation restent dans la couche d'eau, qui est jetée après tous les lavages. Et le DCM, qui représente jusqu'à 1/3 du poids des réactifs difficiles à trouver, est prêt à repartir.
Si vous obtenez un mélange de DСM, d'IPA, d'eau et de pollutions résultant de l'acidification du DСM et de l'IPA, alors seul le DСM sortira correctement. Pour ce faire, le mélange est rempli d'eau, à raison d'environ 70 à 80 % du volume total du mélange. Il se sépare ensuite, laissant le DСM avec ses "propres" saletés (enfin, presque avec des traces d'IPA), et l'IPA, l'eau et les saletés solubles dans l'eau sont séparés. Le DСM est ensuite distillé comme indiqué ci-dessus et lavé 2 ou 3 fois avec de l'eau pour éliminer les restes d'IPA qui gêneront l'utilisation ultérieure du DCM. Il est possible d'extraire l'IPA d'une solution d'eau avec IPA (environ 30 % d'IPA) par plusieurs distillations successives (2 à 3 fois), ce qui permet d'enrichir constamment le pourcentage d'IPA. En même temps, une partie importante de l'IPA est perdue, même si vous décidez de vous embrouiller avec une telle distillation. Le DСM est un réactif beaucoup plus précieux, et il est logique de l'isoler même avec une procédure un peu plus compliquée. En outre, l'IPA avec l'eau peut être évacué dans les égouts, alors que le DСM est fortement déconseillé parce qu'en se séparant de l'eau dans les égouts, il s'accumule (en tant que liquide non miscible plus lourd) dans certaines cavités ; le DCM corrode le plastique et le caoutchouc, cette action peut conduire à des accidents dans les égouts, ce qui peut indiquer l'emplacement de votre laboratoire. En clair,il faut soit le régénérer, soit le verser dans des bidons et l'utiliser.
Le DCM contaminé est versé dans un ballon de distillation et porté à ébullition. Le DCM bout à 40 °C et son azétrope avec l'eau à 38 °C. Il bout violemment, avec des "explosions", donc ne versez pas plus de la moitié ou du tiers du volume du ballon de rb. Je vous conseille également d'utiliser des copeaux d'ébullition, tels que des tasses en porcelaine cassées, des carreaux brisés. Au fur et à mesure que le mélange s'évapore, la température du mélange augmente très rapidement, de nouvelles portions de DCM sale sont ajoutées, les pollutions sont concentrées, environ 1/10 du DCM reste avec cette saleté dans le ballon d'évaporation. Ensuite, il est égoutté, et le ballon, dans un masque à gaz ( !), est lavé avec quelques restes d'acétone ou/et d'IPA, des prunes sont utilisées. On obtient ainsi jusqu'à 80-90 % de DCM, qui est un solvant assez difficile à obtenir, et même lourd (1,3 kg par litre).
Le DСM secondaire obtenu est gris, parfois même jaunâtre, ce qui n'empêche pas de le réutiliser. Il contient de l'eau, ce qui n'est pas non plus gênant car tous les processus impliquant du DСM comprennent également des solutions aqueuses. Après la distillation, le DCM doit être lavé des restes d'IPA (ce qui se produit) et de formaldéhyde.
La procédure est la suivante : Le DCM est versé dans le ballon (réacteur), la même quantité d'eau distillée, le mélange est agité, la solution est divisée en couches, la couche de DCM est drainée. La même eau peut être utilisée pour laver 3-4 lots de DCM, les restes de formaldéhyde et d'IPA sont parfaitement solubles dans l'eau, et pendant la séparation restent dans la couche d'eau, qui est jetée après tous les lavages. Et le DCM, qui représente jusqu'à 1/3 du poids des réactifs difficiles à trouver, est prêt à repartir.
Si vous obtenez un mélange de DСM, d'IPA, d'eau et de pollutions résultant de l'acidification du DСM et de l'IPA, alors seul le DСM sortira correctement. Pour ce faire, le mélange est rempli d'eau, à raison d'environ 70 à 80 % du volume total du mélange. Il se sépare ensuite, laissant le DСM avec ses "propres" saletés (enfin, presque avec des traces d'IPA), et l'IPA, l'eau et les saletés solubles dans l'eau sont séparés. Le DСM est ensuite distillé comme indiqué ci-dessus et lavé 2 ou 3 fois avec de l'eau pour éliminer les restes d'IPA qui gêneront l'utilisation ultérieure du DCM. Il est possible d'extraire l'IPA d'une solution d'eau avec IPA (environ 30 % d'IPA) par plusieurs distillations successives (2 à 3 fois), ce qui permet d'enrichir constamment le pourcentage d'IPA. En même temps, une partie importante de l'IPA est perdue, même si vous décidez de vous embrouiller avec une telle distillation. Le DСM est un réactif beaucoup plus précieux, et il est logique de l'isoler même avec une procédure un peu plus compliquée. En outre, l'IPA avec l'eau peut être évacué dans les égouts, alors que le DСM est fortement déconseillé parce qu'en se séparant de l'eau dans les égouts, il s'accumule (en tant que liquide non miscible plus lourd) dans certaines cavités ; le DCM corrode le plastique et le caoutchouc, cette action peut conduire à des accidents dans les égouts, ce qui peut indiquer l'emplacement de votre laboratoire. En clair,il faut soit le régénérer, soit le verser dans des bidons et l'utiliser.
3. Acétone
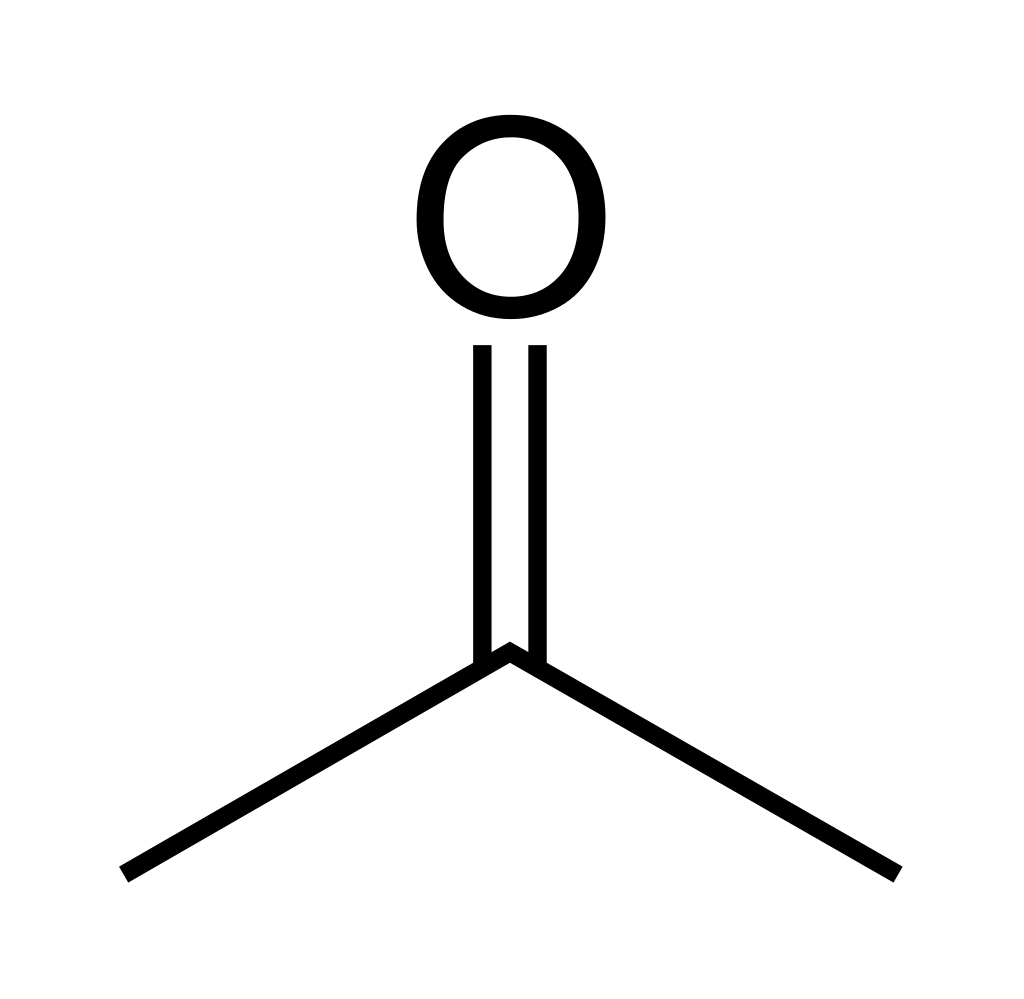
L'acétone est un solvant très capricieux pour la régénération. L'eau, qui est dissoute dans l'acétone, est éliminée très difficilement. C'est plus facile avec les pollutions organiques, l'acétone est purifiée par distillation sous forme de DCM. Si d'autres solvants sont dissous dans l'acétone, ils sont évaporés de la solution polluée sans eau. En outre, lorsque les portions suivantes d'acétone sale sont ajoutées, la température du mélange augmente, et à une température supérieure à 75-80 °C, l'évaporation doit être arrêtée, laissant un peu d'acétone avec le résidu sale. Il n'est pas nécessaire de sécher et de rincer l'acétone distillée.
Le problème est que cette méthode ne permet de régénérer l'acétone que 2 à 3 fois (selon l'expérience). L'acétone est utilisée comme solvant de lavage pour la méphédrone humide avec des restes d'IPA ou de DCM, par exemple. Ces solvants sont évaporés en même temps que l'acétone - leurs points d'ébullition sont proches - et ils s'évaporent avec l'eau (contrairement à l'acétone), qui ne peut pas être éliminée de ce mélange par du chlorure de calcium ou un autre agent sec. Après 2 ou 3 distillations, cet acétone-IPA est éliminé pour le lavage de la verrerie. Il est possible de prolonger la durée de vie de l'acétone secondaire en séchant la méphédrone avant de la laver avec de l'acétone. Cette procédure n'est pas optimale parce qu'elle prend beaucoup de temps. La méphédrone sèche assez longtemps après le nettoyage à l'IPA, surtout si le produit n'est pas très propre.
De petites quantités d'IPA n'empêchent pas l'acétone de laver un produit, surtout sous forme de glace. L'eau peut être éliminée par distillation sur du pentoxyde de phosphore P2O5 ; sécher l'acétone avec de la potasse anhydre (environ 5% du poids de l'acétone) est chauffé pendant plusieurs heures à reflux, verser dans un autre flacon et distiller sur un agent de séchage frais ; le point d'ébullition de l'acétone est de 56,2 °C. Le point d'ébullition de l'acétone est de 56,2 °C. Lesodium métallique et les alcalis ne conviennent pas au séchage de l'acétone.
Le problème est que cette méthode ne permet de régénérer l'acétone que 2 à 3 fois (selon l'expérience). L'acétone est utilisée comme solvant de lavage pour la méphédrone humide avec des restes d'IPA ou de DCM, par exemple. Ces solvants sont évaporés en même temps que l'acétone - leurs points d'ébullition sont proches - et ils s'évaporent avec l'eau (contrairement à l'acétone), qui ne peut pas être éliminée de ce mélange par du chlorure de calcium ou un autre agent sec. Après 2 ou 3 distillations, cet acétone-IPA est éliminé pour le lavage de la verrerie. Il est possible de prolonger la durée de vie de l'acétone secondaire en séchant la méphédrone avant de la laver avec de l'acétone. Cette procédure n'est pas optimale parce qu'elle prend beaucoup de temps. La méphédrone sèche assez longtemps après le nettoyage à l'IPA, surtout si le produit n'est pas très propre.
De petites quantités d'IPA n'empêchent pas l'acétone de laver un produit, surtout sous forme de glace. L'eau peut être éliminée par distillation sur du pentoxyde de phosphore P2O5 ; sécher l'acétone avec de la potasse anhydre (environ 5% du poids de l'acétone) est chauffé pendant plusieurs heures à reflux, verser dans un autre flacon et distiller sur un agent de séchage frais ; le point d'ébullition de l'acétone est de 56,2 °C. Le point d'ébullition de l'acétone est de 56,2 °C. Lesodium métallique et les alcalis ne conviennent pas au séchage de l'acétone.
4. Ortho-Xylène
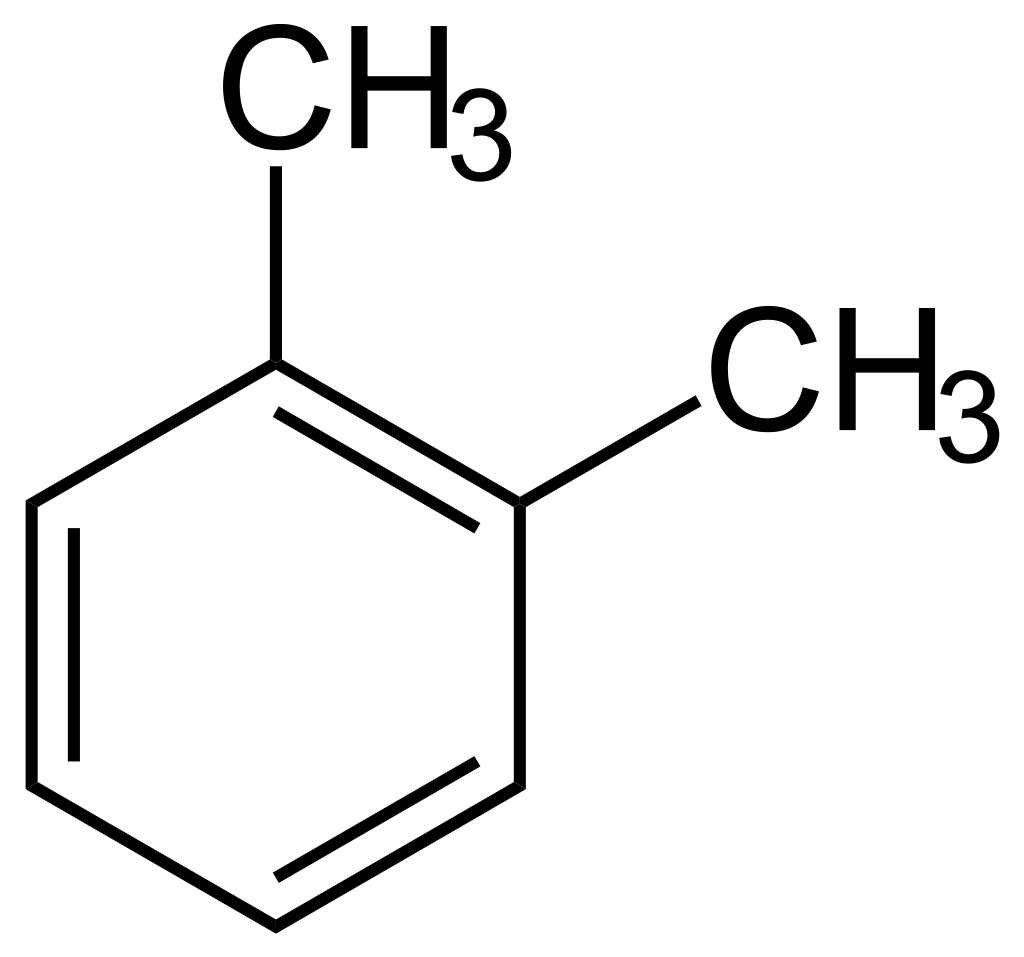
L'ortho-xylène est un solvant injustement "oublié". Il possède de nombreuses propriétés intéressantes. Il n'est ni toxique, ni cancérigène, ni aussi volatil (pb 144 °C) que le benzène ou le toluène. Les valeurs de temps et de température de synthèse sont similaires à celles du solvant benzène (déjà vérifiées). O-xylène, presque non miscible à l'eau (0,014 %). Le mélange azéotropique d'o-xylène et d'eau bout à 92 °C et contient 64,25 % d'o-xylène et 35,75 % d'eau. La régénération du xylène se présente donc comme suit.
2/3 de xylène et 1/3 d'eau distillée sont versés dans le ballon à fond rond [remplir la moitié du volume du ballon]. Le mélange bout, comme il se doit pour un solvant à point d'ébullition élevé, lentement et progressivement, l'eau de la couche inférieure produit des jets de vapeur qui traversent la couche supérieure de xylène. Il se forme alors un chapeau de mousse qui peut aspirer des saletés dans le condenseur à reflux. Il convient de verser un demi-volume au fond du ballon et d'ajouter des copeaux d'ébullition pour éviter la formation de mousse. Deux couches se forment simultanément dans le ballon de réception, la couche inférieure est constituée d'eau (versée), le xylène est en outre lavé à l'eau à des fins de purification, car certains polluants pénètrent dans le ballon de réception (apparemment en raison du point d'ébullition élevé de l'azéotrope). Lexylène n'est pratiquement pas miscible avec l'eau, il n'est donc pas nécessaire de sécher le produit régénéré.
5. Éther diéthylique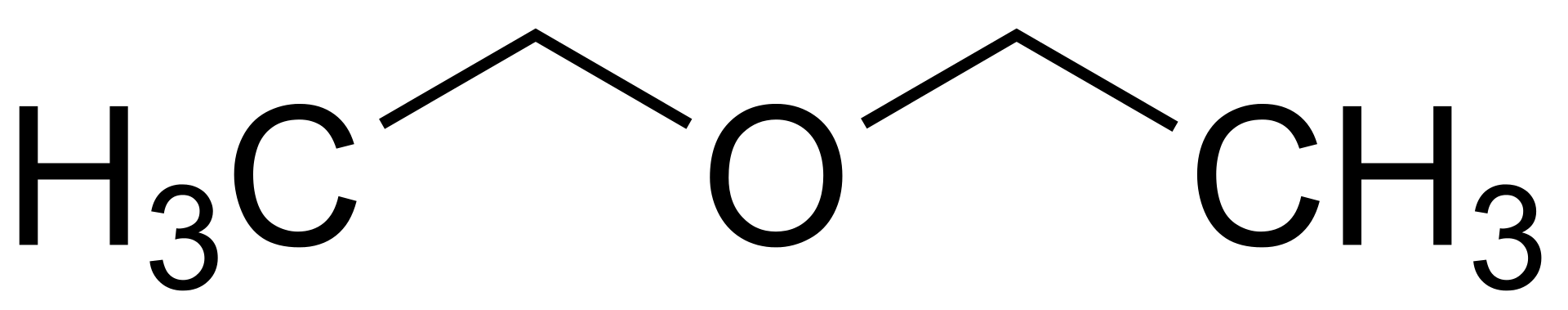
Extrêmement inflammable ; les vapeurs forment des mélanges explosifs avec l'air. Les vapeurs sont environ 2,6 fois plus lourdes que l'air et peuvent se répandre sur la surface de la table de travail. Il faut donc veiller à ce qu'à proximité (jusqu'à 1 m) du lieu de travail avec l'éther, tous les brûleurs à gaz soient éteints et que les poêles électriques à spirale ouverte soient déconnectés du réseau. Lors du stockage de l'éther diéthylique sous l'action de la lumière et de l'oxygène atmosphérique, des composés peroxydiques explosifs et de l'acétaldéhyde se forment dans l'éther diéthylique. Les composés peroxydes sont à l'origine d'explosions extrêmement violentes, notamment lors de la distillation à sec de l'éther. De nombreuses réactions ont été proposées pour la détection du peroxyde dans l'éther diéthylique. L'éther est lavé avec une solution de NaOH à 5 % et de l'eau, puis séché pendant 24 heures sur du CaCl2 anhydre (150-200 g de CaCl2 pour 1 litre d'éther). Le CaCl2 est ensuite filtré sur un grand papier filtre et l'éther est recueilli dans une bouteille en verre foncé. Le flacon est fermé hermétiquement par un bouchon de liège dans lequel est inséré un tube de chlorure de calcium rempli de CaCl2, coudé à un angle aigu. Ensuite, après avoir ouvert le ballon, on introduit brièvement du fil de sodium dans l'éther, à raison de 5 g pour 1 litre d'éther.
Après 24 heures, lorsqu'il n'y a plus d'émission de bulles d'hydrogène, on ajoute à nouveau 3 g de fil de sodium pour 1 litre d'éther, et après 12 heures, l'éther est versé dans un ballon de distillation et distillé sur du fil de sodium. Le récipient doit être protégé par un tube de chlorure de calcium avec du CaCl2. Le distillat (point d'ébullition 34,6 °C) est recueilli dans une bouteille en verre foncé qui, après avoir ajouté 1 g de fil de sodium pour 1 litre d'éther, est fermée par un bouchon de liège avec un tube de chlorure de calcium et conservée dans un endroit froid et sombre. Si la surface du fil a beaucoup changé et que des bulles d'hydrogène sont à nouveau libérées lorsque le fil est ajouté, l'éther doit être filtré dans un autre flacon et une autre portion de fil de sodium doit être ajoutée.
Un moyen pratique et très efficace de purifier l'éther diéthylique des peroxydes et en même temps de l'humidité consiste à faire passer l'éther dans une colonne avec de l'Al2O3 actif. Des colonnes d'une hauteur de 60 à 80 cm et d'un diamètre de 2 à 4 cm, remplies de 82 g d'Al2O3, suffisent à purifier 700 ml d'éther contenant une quantité significative de composés peroxydés. Les déchets d'Al2O3 peuvent être facilement régénérés si une solution aqueuse acidifiée à 50 % de FeSO4. 7H2O est passée dans la colonne, lavée à l'eau, séchée et activée thermiquement à 400-450 °C.
L'éther absolu est un liquide très hygroscopique. Ledegré d'absorption d'humidité par l'éther au cours de son stockage peut être déterminé par le bleuissement de la poudre blanche anhydre de CuSO4 lorsqu'elle est introduite dans l'éther (un hydrate coloré CuSO4.5H2O se forme).
Après 24 heures, lorsqu'il n'y a plus d'émission de bulles d'hydrogène, on ajoute à nouveau 3 g de fil de sodium pour 1 litre d'éther, et après 12 heures, l'éther est versé dans un ballon de distillation et distillé sur du fil de sodium. Le récipient doit être protégé par un tube de chlorure de calcium avec du CaCl2. Le distillat (point d'ébullition 34,6 °C) est recueilli dans une bouteille en verre foncé qui, après avoir ajouté 1 g de fil de sodium pour 1 litre d'éther, est fermée par un bouchon de liège avec un tube de chlorure de calcium et conservée dans un endroit froid et sombre. Si la surface du fil a beaucoup changé et que des bulles d'hydrogène sont à nouveau libérées lorsque le fil est ajouté, l'éther doit être filtré dans un autre flacon et une autre portion de fil de sodium doit être ajoutée.
Un moyen pratique et très efficace de purifier l'éther diéthylique des peroxydes et en même temps de l'humidité consiste à faire passer l'éther dans une colonne avec de l'Al2O3 actif. Des colonnes d'une hauteur de 60 à 80 cm et d'un diamètre de 2 à 4 cm, remplies de 82 g d'Al2O3, suffisent à purifier 700 ml d'éther contenant une quantité significative de composés peroxydés. Les déchets d'Al2O3 peuvent être facilement régénérés si une solution aqueuse acidifiée à 50 % de FeSO4. 7H2O est passée dans la colonne, lavée à l'eau, séchée et activée thermiquement à 400-450 °C.
L'éther absolu est un liquide très hygroscopique. Ledegré d'absorption d'humidité par l'éther au cours de son stockage peut être déterminé par le bleuissement de la poudre blanche anhydre de CuSO4 lorsqu'elle est introduite dans l'éther (un hydrate coloré CuSO4.5H2O se forme).
6. Benzène
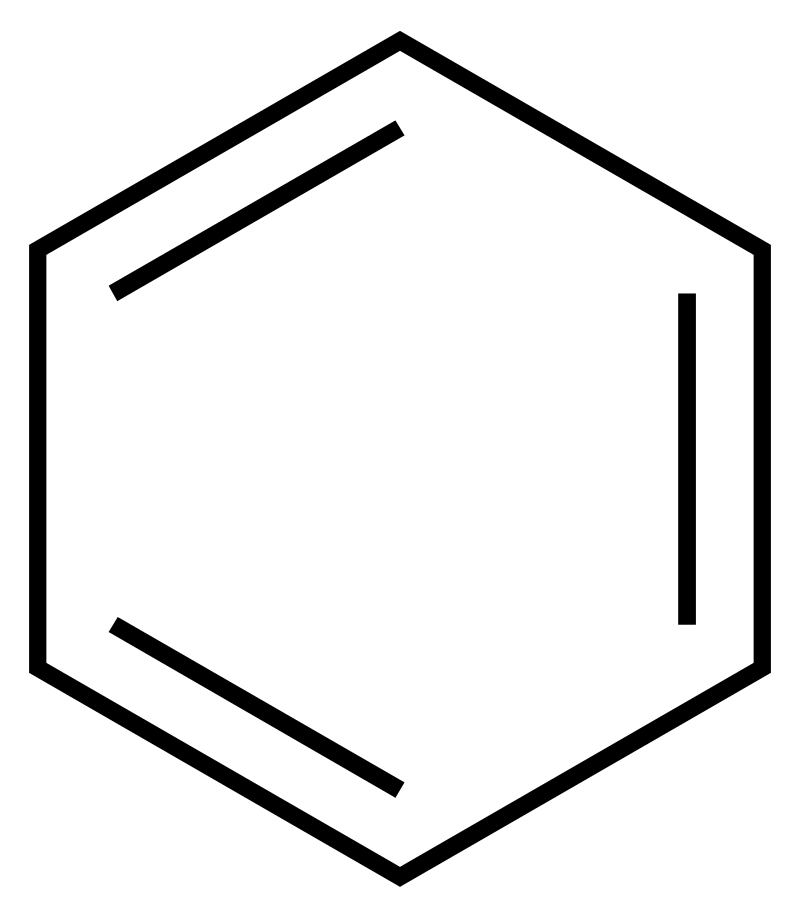
Le benzène et ses homologues, le toluène et les xylènes, sont largement utilisés comme solvants et milieux de séchage azéotropiques. Le benzène doit être manipulé avec un équipement de sécurité spécial en raison de son inflammabilité et de sa toxicité, ainsi que de la formation de mélanges explosifs avec l'air. Les vapeurs de benzène en cas d'exposition répétée perturbent le fonctionnement normal des organes hématopoïétiques ; à l'état liquide, le benzène est fortement absorbé par la peau et l'irrite. Le benzène forme un mélange azéotropique avec l'eau (8,83 % en poids, pb 69,25 °C). Par conséquent, avant la distillation, le benzène humide est porté à ébullition avec un appareil Dean-Stark et l'eau est presque entièrement distillée. Un séchage supplémentaire du benzène distillé est généralement effectué avec du CaCl2 calciné (pendant 2 à 3 jours) et du fil de sodium. Pendant la distillation, il faut veiller à ce que le benzène distillé ne cristallise pas dans un condenseur (Tm 5,5 °C).
Le benzène technique contient jusqu'à 0,05 % en poids de thiophène, qui ne peut être séparé du benzène ni par distillation fractionnée ni par cristallisation (congélation). Le thiophène dans le benzène est détecté comme suit : une solution de 10 mg d'isatine dans 10 ml de H2SO4 conc. est agitée avec 3 ml de benzène. En présence de thiophène, la couche d'acide sulfurique devient bleu-vert. Le benzène est purifié du thiophène par extraction répétée avec du H2SO4 concentré. Pour 1 litre de benzène, il faut 80 ml d'acide. La purification est effectuée jusqu'à ce que l'acide prenne une couleur jaune pâle. Après séparation de la couche d'acide, le benzène est lavé avec de l'eau, puis avec une solution de Na2CO3 à 10 % et à nouveau avec de l'eau, après quoi le benzène est distillé. Une méthode plus efficace et plus simple pour éliminer le thiophène du benzène consiste à faire bouillir 1 litre de benzène avec 100 g de nickel de Raney dans un ballon à reflux pendant 15 à 30 minutes. Une autre façon de purifier le benzène du thiophène consiste à le cristalliser de façon fractionnée à partir de l'alcool éthylique. Une solution saturée de benzène dans l'alcool est refroidie à environ -15 °C, le benzène solide est rapidement filtré et distillé.
Le benzène technique contient jusqu'à 0,05 % en poids de thiophène, qui ne peut être séparé du benzène ni par distillation fractionnée ni par cristallisation (congélation). Le thiophène dans le benzène est détecté comme suit : une solution de 10 mg d'isatine dans 10 ml de H2SO4 conc. est agitée avec 3 ml de benzène. En présence de thiophène, la couche d'acide sulfurique devient bleu-vert. Le benzène est purifié du thiophène par extraction répétée avec du H2SO4 concentré. Pour 1 litre de benzène, il faut 80 ml d'acide. La purification est effectuée jusqu'à ce que l'acide prenne une couleur jaune pâle. Après séparation de la couche d'acide, le benzène est lavé avec de l'eau, puis avec une solution de Na2CO3 à 10 % et à nouveau avec de l'eau, après quoi le benzène est distillé. Une méthode plus efficace et plus simple pour éliminer le thiophène du benzène consiste à faire bouillir 1 litre de benzène avec 100 g de nickel de Raney dans un ballon à reflux pendant 15 à 30 minutes. Une autre façon de purifier le benzène du thiophène consiste à le cristalliser de façon fractionnée à partir de l'alcool éthylique. Une solution saturée de benzène dans l'alcool est refroidie à environ -15 °C, le benzène solide est rapidement filtré et distillé.
Benzène à partir de benzoate de sodium
Conclusion
La récupération de chaque solvant individuel est économiquement avantageuse. La séparation des mélanges de différents solvants par fractions est beaucoup plus compliquée. Pour une régénération réussie, il est préférable de choisir des méthodes de synthèse pour utiliser les solvants qui ne les mélangent pas entre eux. Actuellement, le processus qui se termine par une acidification à l'acide chlorhydrique avec la sélection et le lavage de la fraction aqueuse semble être le plus judicieux. Le nettoyage de la première solution de produit utilise du DCM, puis il faut utiliser l'ébullition avec de l'IPA, et enfin laver le produit final avec de l'acétone. En conclusion, le nettoyage avec trois solvants différents qui ne se mélangent pas pendant l'utilisation (surtout si le produit est séché après le nettoyage dans l'IPA) garantit une bonne pureté du produit et la possibilité de récupérer une partie importante des solvants.
Last edited by a moderator: