G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,991
- Solutions
- 3
- Reaction score
- 3,379
- Points
- 113
- Deals
- 1
Johdanto.
Vain noin 80 % orgaanisen laboratorion reaktioista sisältää vaiheen nimeltä refluksointi. Reaktioliuottimen avulla pidät materiaalit liuenneina ja vakiolämpötilassa kiehuttamalla liuotinta, tiivistämällä sitä ja palauttamalla sen takaisin kolviin. Refluksimenetelmää käytetään laajalti myös lääkeaineiden synteesissä, kuten amfetamiinin ja metamfetamiinin ja muiden fenyylietyyliamiinien, LSD:n, joidenkin synteettisten kannabinoidien, CBD:n isomerisaation, MDMA:n ja monien muiden tapausten valmistuksessa. Tämä tekniikka on melko yksinkertainen, mutta sinun ei pidä aliarvioida sen vaaraa ja ryhtyä kaikkiin varotoimiin.
Yleiskatsaus Refluxiin.
Refluksiasetus (kuva 1) mahdollistaa nesteen kiehumisen ja tiivistymisen, jolloin tiivistetty neste palaa takaisin alkuperäiseen pulloon. Refluksiasetus vastaa tislausta, ja suurin ero on lauhduttimen pystysuora sijoitus. Neste pysyy liuottimen (tai liuoksen) kiehumispisteessä aktiivisen refluksin aikana.
Refluksilaitteisto mahdollistaa liuoksen helpon kuumentamisen, mutta ilman liuotinhäviötä, joka aiheutuisi kuumentamisesta avoimessa astiassa. Refluksilaitteistossa liuotinhöyryt jäävät lauhduttimeen, ja reagoivien aineiden pitoisuus pysyy vakiona koko prosessin ajan. Liuoksen refluksoinnin päätarkoitus on lämmittää liuosta hallitusti vakiolämpötilassa. Kuvitellaan esimerkiksi, että liuosta halutaan lämmittää 60 ℃:n lämpötilaan tunnin ajan kemiallisen reaktion toteuttamiseksi. Lämpimän vesihauteen pitäminen 60 ℃:n lämpötilassa olisi vaikeaa ilman erikoislaitteita, ja se vaatisi säännöllistä seurantaa. Jos liuottimena olisi metanoli, liuos voitaisiin kuitenkin lämmittää takaisinvirtaukseen, ja se säilyttäisi lämpötilansa ilman säännöllistä ylläpitoa metanolin kiehumispisteessä (65 ℃). On totta, että 65 ℃ ei ole 60 ℃, ja jos tietty lämpötila olisi ratkaiseva reaktion kannalta, tarvittaisiin erityisiä lämmityslaitteita. Usein reaktiolämpötilaksi valitaan kuitenkin liuottimen kiehumispiste sen käytännöllisyyden vuoksi.
Vaiheittaiset menettelyt.
1. Kaada refluksoitava liuos pyöreäpohjaiseen kolviin ja kiinnitä se rengastelineeseen tai ristikkoon jatkopuristimella ja pienellä kumitiivisteellä (kuva 2 a ja video). Pullo saa olla enintään puolitäynnä. Kuvissa ei ole kumitiivisteitä tuntemattomasta syystä. Jos käytät korkean lämpötilan keittämistä (>150 ℃) tai liekkilämmitystä, niitä ei voi käyttää.
2. Lisää sekoitustanko tai muutama keittokivi kolhujen estämiseksi. Kiehumakiviä ei pidä käyttää, kun refluksoidaan väkeviä rikki- tai fosforihappoliuoksia, koska ne värjäävät liuoksen. Kun esimerkiksi sekoituspalkkia käytetään kuoppien estämiseen väkevän rikkihapon kanssa, liuos jää värittömäksi (kuva 2 b). Kun sama reaktio tehdään kiehumakivellä, liuos tummuu kuumentamisen aikana (kuva 2 c) ja muuttaa lopulta koko liuoksen syvän violetinruskeaksi (kuva 2 d).
2. Lisää sekoitustanko tai muutama keittokivi kolhujen estämiseksi. Kiehumakiviä ei pidä käyttää, kun refluksoidaan väkeviä rikki- tai fosforihappoliuoksia, koska ne värjäävät liuoksen. Kun esimerkiksi sekoituspalkkia käytetään kuoppien estämiseen väkevän rikkihapon kanssa, liuos jää värittömäksi (kuva 2 b). Kun sama reaktio tehdään kiehumakivellä, liuos tummuu kuumentamisen aikana (kuva 2 c) ja muuttaa lopulta koko liuoksen syvän violetinruskeaksi (kuva 2 d).
3. Aseta kumiletkut lauhduttimeen (kostuta päät ensin, jotta ne liukuvat) ja kiinnitä sitten lauhdutin pystysuoraan pyöreäpohjaiseen kolviin. Jos käytät korkeaa lauhdutinta, kiinnitä lauhdutin rengastelineeseen tai ristikkoon (kuva 3 a). Varmista, että lauhdutin istuu tiiviisti kolviin. Turvallisuushuomautus: Jos osia ei ole liitetty kunnolla ja palavia höyryjä pääsee ulos, ne voivat syttyä lämmönlähteestä. Älä yhdistä pyöreäpohjaista kolvia ja lauhdutinta muoviliittimellä, kuten kuvassa 3 с on esitetty. Muoviliittimet voivat joskus pettää (erityisesti silloin, kun niitä kuumennetaan), eikä kolvia voida tällä tavalla luotettavasti irrottaa lämmönlähteestä refluksin päätyttyä.
Huomautus: Mitä korkeampi liuottimen (liuottimen seoksen) kiehumispiste on, sitä lyhyempää refluksilauhdutinta tarvitaan. Jos taas liuotin kiehuu alhaisissa lämpötiloissa (eetteri), käytä pisintä Liebigin refluksilauhdutinta.
4. Kytke lauhduttimen alemman varren letku vesihanaan ja anna ylemmän varren letkun valua lavuaariin (kuva 3 b). On tärkeää, että vesi menee lauhduttimen alaosasta sisään ja yläosasta ulos (jotta vesi virtaa painovoimaa vastaan), tai muuten lauhdutin on tehoton, koska se ei täyty kokonaan.
Huomautus: Mitä korkeampi liuottimen (liuottimen seoksen) kiehumispiste on, sitä lyhyempää refluksilauhdutinta tarvitaan. Jos taas liuotin kiehuu alhaisissa lämpötiloissa (eetteri), käytä pisintä Liebigin refluksilauhdutinta.
4. Kytke lauhduttimen alemman varren letku vesihanaan ja anna ylemmän varren letkun valua lavuaariin (kuva 3 b). On tärkeää, että vesi menee lauhduttimen alaosasta sisään ja yläosasta ulos (jotta vesi virtaa painovoimaa vastaan), tai muuten lauhdutin on tehoton, koska se ei täyty kokonaan.
5. Jos useita liuoksia refluksoidaan samanaikaisesti (esim. jos monet oppilaat tekevät refluksointia vierekkäin), kunkin refluksointiasetelman letkut voidaan kytkeä sarjaan (kuva 4). Tämän toteuttamiseksi "Setup A:n" ylempi varsi, joka normaalisti valuu lavuaariin, liitetään sen sijaan "Setup B:n" alempaan varteen. Laitteiden kytkeminen sarjaan minimoi vedenkulutuksen, koska yhdestä lauhduttimesta poistuva vesi menee seuraavaan lauhduttimeen. Useita refluksilaitteita voidaan kytkeä sarjaan, ja veden virtausta on seurattava sen varmistamiseksi, että kaikki laitteistot jäähdytetään riittävästi.
.

6. Aloita tasaisen vesivirran kierrättäminen letkujen läpi (ei niin voimakasta, että letku heilahtaa ympäriinsä korkeasta vedenpaineesta). Tarkista vielä kerran, että lasitavaran osat sopivat varmasti yhteen, ja aseta sitten lämmönlähde pullon alle. Kytke sekoituslevy päälle, jos käytät sekoituspalkkia.
a) Jos käytät lämmitysvaippaa, pidä se paikallaan säädettävällä alustalla (esim. lankaverkolla/rengaspuristimella). Jätä muutama sentti vaipan alle, jotta kun reaktio on valmis, vaippa voidaan laskea alas ja kolvi jäähdyttää. Jos lämmitysvaippa ei sovi täydellisesti pyöreäpohjaisen pullon kokoon, ympäröi pullo hiekalla paremman kosketuksen aikaansaamiseksi (kuva 5 a).
b) Jos käytetään hiekkakylpyä, kolvi haudataan hiekkaan niin, että hiekka on vähintään yhtä korkealla kuin kolvissa oleva nestepinta (kuva 5 b).
c) Jos asetelma jätetään lopulta pitkäksi aikaa ilman valvontaa (esim. yön yli), kiristä kuparilanka lauhduttimen letkujen kiinnikkeiden päälle, jotta vedenpaineen muutokset eivät aiheuta letkujen irtoamista.
7. Jos lämmönlähde on esilämmitetty (valinnainen), liuoksen pitäisi alkaa kiehua viiden minuutin kuluessa. Jos näin ei tapahdu, lisää lämmitysnopeutta. Sopiva lämmitysnopeus saavutetaan, kun liuos kiehuu voimakkaasti ja "refluksirengas" näkyy noin kolmanneksen matkasta lauhduttimessa. Refluksirengas on yläraja, jossa kuumat höyryt tiivistyvät aktiivisesti. Joissakin liuoksissa (esim. vesiliuos) refluksirengas on selvä, ja lauhduttimessa on helposti näkyviä pisaroita (kuva 6 a+b). Muissa liuoksissa (esim. monissa orgaanisissa liuottimissa) refluksirengas on hienovaraisempi, mutta se voidaan nähdä tarkalla tarkkailulla (kuva 6 c). Lauhduttimessa voi näkyä hienovaraista liikettä, kun nestettä tippuu lauhduttimen sivuille, tai taustakohteet voivat näkyä vääristyneinä, koska valo taittuu lauhdutusnesteen läpi (kuvassa 6 d rengastelineen napa on vääristynyt).
8. Jos noudatetaan menettelyä, jossa refluksoidaan tietyn ajan (esim. "refluksoidaan tunnin ajan"), ajanjakson on alettava, kun liuos ei vain kiehu vaan refluksoi aktiivisesti lauhduttimen pohjakolmanneksessa.
9. Lämpöä on vähennettävä, jos refluksirengas nousee menemään lauhduttimen puoliväliin tai ylemmäs, tai muuten höyryt voivat karata kolvista.
10. Kun refluksi on päättynyt, sammuta lämmönlähde ja poista kolvi lämmöstä joko nostamalla refluksilaite ylös tai laskemalla lämmönlähde alas (kuva 7 a).
9. Lämpöä on vähennettävä, jos refluksirengas nousee menemään lauhduttimen puoliväliin tai ylemmäs, tai muuten höyryt voivat karata kolvista.
10. Kun refluksi on päättynyt, sammuta lämmönlähde ja poista kolvi lämmöstä joko nostamalla refluksilaite ylös tai laskemalla lämmönlähde alas (kuva 7 a).
Älä sulje lauhduttimen läpi virtaavaa vettä, ennen kuin liuos on vain kosketuslämpöistä. Muutaman minuutin ilmajäähdytyksen jälkeen pyöreäpohjainen pullo voidaan upottaa vesihanaan jäähdytysprosessin nopeuttamiseksi (kuva 7 b).
Kuiva refluksi.
Jos sinun on pidettävä ilmakehän vesihöyry poissa reaktiostasi, sinun on käytettävä kuivausputkea ja tuloilmasovitinta refluksiasetelmassa (kuva 8). Voit käyttää näitä, jos sinun on pidettävä vesihöyry poissa mistä tahansa järjestelmästä, ei vain refluksiasetuksesta.
.
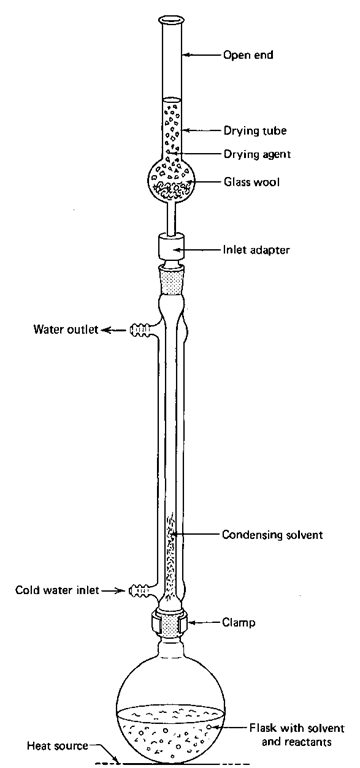
1. Puhdista ja kuivaa kuivausputki tarvittaessa. Sinun ei tarvitse tehdä perusteellista puhdistusta, ellet epäile, että vedetön kuivausaine ei ole enää vedetön. Jos aine on paakkuuntunut putken sisällä, se on todennäköisesti kuollut. Putki kannattaa puhdistaa ja ladata uudelleen toimenpiteen alussa. Muista käyttää vedetöntä kalsiumkloridia tai -sulfaattia. Sen pitäisi pysyä kunnossa muutaman käyttökerran. Jos olet onnekas, valkoisen Drieriten joukkoon saattaa sekoittua indikoivaa Drieriteä, joka on erityisesti valmistettua vedetöntä kalsiumsulfaattia. Jos väri on sininen, kuivausaine on hyvä; jos se on punainen, kuivausaine ei ole enää kuiva, ja siitä on syytä päästä eroon (katso kuivausaineet kohdassa "Tyhjiökuivaimet").
2. Laita sisään löysä tulppa lasivillaa tai puuvillaa, jotta kuivausaine ei pääse putoamaan reaktiopulloon.
3. Kokoa laite kuvan mukaisesti siten, että kuivausputki ja sovitin ovat lauhduttimen päällä.
4. Tässä vaiheessa reagenssit voidaan lisätä kolviin ja lämmittää laitteella. Yleensä laitteistoa lämmitetään tyhjänä, jotta vesi saadaan ajettua pois laitteen seinämiltä.
5. Kuumennetaan yleensä tyhjänä olevaa apparaattia höyrykylvyssä ja annetaan koko asetelmalle neljänneskierros silloin tällöin, jotta se kuumenee tasaisesti. Polttimen käyttö on mahdollista, jos palovaaraa ei ole ja jos lämmitys tehdään huolellisesti. Raskaat hiotut lasiliitokset halkeavat, jos niitä kuumennetaan liikaa.
6. Anna laitteen jäähtyä huoneenlämpöiseksi. Jäähtyessään ilma imetään kuivausputken läpi ennen kuin se osuu laitteeseen. Kuivausaine sitoo ilmassa olevan kosteuden.
7. Lisää nopeasti kuivat reagenssit tai liuottimet reaktiopulloon ja kokoa järjestelmä uudelleen.
8. Suorita reaktio tavalliseen tapaan tavallisena refluksina.
2. Laita sisään löysä tulppa lasivillaa tai puuvillaa, jotta kuivausaine ei pääse putoamaan reaktiopulloon.
3. Kokoa laite kuvan mukaisesti siten, että kuivausputki ja sovitin ovat lauhduttimen päällä.
4. Tässä vaiheessa reagenssit voidaan lisätä kolviin ja lämmittää laitteella. Yleensä laitteistoa lämmitetään tyhjänä, jotta vesi saadaan ajettua pois laitteen seinämiltä.
5. Kuumennetaan yleensä tyhjänä olevaa apparaattia höyrykylvyssä ja annetaan koko asetelmalle neljänneskierros silloin tällöin, jotta se kuumenee tasaisesti. Polttimen käyttö on mahdollista, jos palovaaraa ei ole ja jos lämmitys tehdään huolellisesti. Raskaat hiotut lasiliitokset halkeavat, jos niitä kuumennetaan liikaa.
6. Anna laitteen jäähtyä huoneenlämpöiseksi. Jäähtyessään ilma imetään kuivausputken läpi ennen kuin se osuu laitteeseen. Kuivausaine sitoo ilmassa olevan kosteuden.
7. Lisää nopeasti kuivat reagenssit tai liuottimet reaktiopulloon ja kokoa järjestelmä uudelleen.
8. Suorita reaktio tavalliseen tapaan tavallisena refluksina.
Lisäys ja refluksi.
Aina silloin tällöin joudut lisäämään yhdistettä asetelmaan reaktion ollessa käynnissä, yleensä refluksin ohella. No, et riko systeemiä auki, päästä myrkyllisiä höyryjä ulos ja tee itseäsi sairaaksi lisätessäsi uusia reagensseja. Käytetään lisäyssuppiloa. Nyt puhuimme lisäyssuppiloista takaisin erotussuppiloiden (laboratorion lasitavarat) kanssa, kun harkitsimme varsi, ja se on saattanut olla hämmentävää.
Suppilon käyttö.
Katso kuvaa 9 a. Se on todellinen erotussuppilo. Tänne laitetaan nesteitä, ravistetaan ja uutetaan niitä. Mutta voisitko käyttää tätä suppiloa materiaalin lisäämiseen asetelmaan? Ei. Päässä ei ole hiottua lasiliitosta, ja vain lasiliitokset sopivat lasiliitoksiin. Kuvassa 9 c on paineen tasaava lisäyssuppilo. Muistatko, kun sinua varoitettiin poistamasta erotussuppilon tulppaa, jotta suppiloon ei muodostuisi tyhjiötä, kun tyhjennät sitä? Joka tapauksessa sivusuppilo tasaa paineen pulloon lisättävän nesteen molemmilla puolilla, joten neste virtaa vapaasti ilman tyhjiön muodostumista ja ilman, että sinun tarvitsee poistaa tulppaa. Tämä laite on erittäin hieno, erittäin kallis, erittäin rajoitettu ja erittäin harvinainen. Ja jos yrität uuttoa tällaisella, kaikki neste valuu putkesta lattialle, kun ravistat suppiloa. Niinpä päädyttiin kompromissiin (kuva 9 b). Koska uuttoja tehdään luultavasti enemmän kuin lisäyksiä, olipa refluksin kanssa tai ilman, paineentasausputki poistettiin, mutta lasiliitos pysyi paikoillaan. Uuttoja; ei ongelmia. Varren luonteella ei ole merkitystä. Mutta lisäysten aikana sinun on otettava vastuu siitä, ettei ikävää alipaineistumista tapahdu. Voit poistaa tulpan silloin tällöin tai laittaa tulpan tilalle kuivausputken ja tuloilmasovittimen. Jälkimmäinen pitää kosteuden poissa ja estää tyhjiön muodostumisen suppilon sisälle.
Kuinka asetukset tehdään
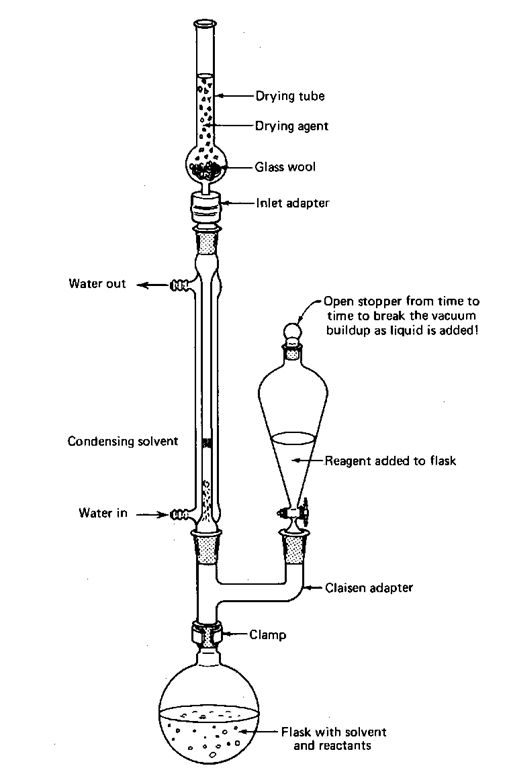
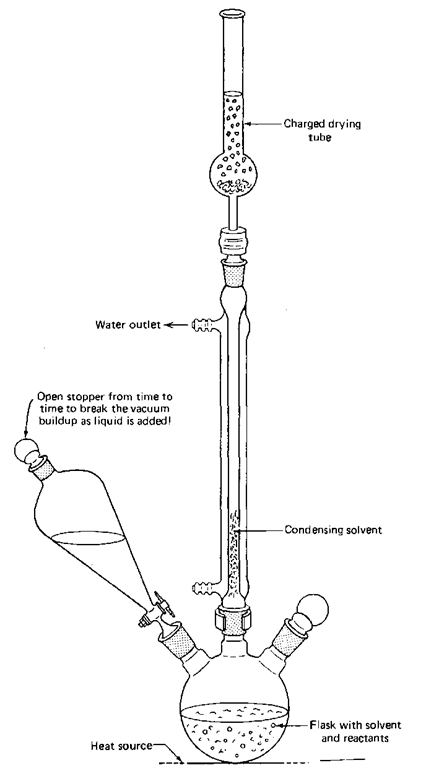
Additio ja refluksi voidaan järjestää ainakin kahdella tavalla joko kolmikaulapullon tai Claisenin sovittimen avulla. Ajattelin näyttää nämä molemmat asetelmat kuivausputkien kanssa. Ne estävät ilmassa olevan kosteuden pääsyn reaktioosi. Jos et tarvitse niitä, tee se ilman niitä.
Suppilon käyttö.
Katso kuvaa 9 a. Se on todellinen erotussuppilo. Tänne laitetaan nesteitä, ravistetaan ja uutetaan niitä. Mutta voisitko käyttää tätä suppiloa materiaalin lisäämiseen asetelmaan? Ei. Päässä ei ole hiottua lasiliitosta, ja vain lasiliitokset sopivat lasiliitoksiin. Kuvassa 9 c on paineen tasaava lisäyssuppilo. Muistatko, kun sinua varoitettiin poistamasta erotussuppilon tulppaa, jotta suppiloon ei muodostuisi tyhjiötä, kun tyhjennät sitä? Joka tapauksessa sivusuppilo tasaa paineen pulloon lisättävän nesteen molemmilla puolilla, joten neste virtaa vapaasti ilman tyhjiön muodostumista ja ilman, että sinun tarvitsee poistaa tulppaa. Tämä laite on erittäin hieno, erittäin kallis, erittäin rajoitettu ja erittäin harvinainen. Ja jos yrität uuttoa tällaisella, kaikki neste valuu putkesta lattialle, kun ravistat suppiloa. Niinpä päädyttiin kompromissiin (kuva 9 b). Koska uuttoja tehdään luultavasti enemmän kuin lisäyksiä, olipa refluksin kanssa tai ilman, paineentasausputki poistettiin, mutta lasiliitos pysyi paikoillaan. Uuttoja; ei ongelmia. Varren luonteella ei ole merkitystä. Mutta lisäysten aikana sinun on otettava vastuu siitä, ettei ikävää alipaineistumista tapahdu. Voit poistaa tulpan silloin tällöin tai laittaa tulpan tilalle kuivausputken ja tuloilmasovittimen. Jälkimmäinen pitää kosteuden poissa ja estää tyhjiön muodostumisen suppilon sisälle.
Kuinka asetukset tehdään
Additio ja refluksi voidaan järjestää ainakin kahdella tavalla joko kolmikaulapullon tai Claisenin sovittimen avulla. Ajattelin näyttää nämä molemmat asetelmat kuivausputkien kanssa. Ne estävät ilmassa olevan kosteuden pääsyn reaktioosi. Jos et tarvitse niitä, tee se ilman niitä.
.
Kiehuvat kivet (kiehuvat lastut).
Kiehumakivet (tai kiehumalastut) ovat pieniä mustan huokoisen kiven (usein piikarbidin) kappaleita, jotka lisätään liuottimeen tai liuokseen. Ne sisältävät ilmaa, joka kuplii ulos, kun nestettä kuumennetaan, ja niillä on suuri pinta-ala, joka voi toimia nukleaatiopaikkoina liuotinkuplien muodostumiselle. Ne on lisättävä viileään nesteeseen, ei sellaiseen, joka on lähellä kiehumispistettään, tai seurauksena voi olla voimakas kuplien purkautuminen. Kun neste saatetaan kiehuvaksi kiehuvilla kivillä, kuplat ovat yleensä peräisin pääasiassa kivistä (kuva 11 b). Kiehumakiviä ei voi käyttää uudelleen, sillä yhden käyttökerran jälkeen niiden raot täyttyvät liuottimella, eivätkä ne enää pysty muodostamaan kuplia.
Kiehumakiviä ei pitäisi käyttää kuumennettaessa väkeviä rikki- tai fosforihappoliuoksia, koska ne voivat hajottaa ja saastuttaa liuoksen. Esimerkiksi kuvassa 12 on esitetty Fischerin esteröintireaktio, jossa käytetään väkevää rikkihappoa. Kun sekoituspalkkia käytetään kuhmun estämiseksi, liuos pysyy värittömänä (kuva 12 a). Kun sama reaktio suoritetaan käyttämällä kiehumakiveä, liuos tummuu kuumentamisen aikana (kuva 12 b) ja muuttaa lopulta koko liuoksen syvän violetinruskeaksi (kuva 12 c). Sen lisäksi, että tumma väri saastuttaa liuosta, se vaikeuttaa materiaalin käsittelyä erotussuppilolla: kuvassa 12 d on kaksi kerrosta, vaikka sitä on hyvin vaikea nähdä.
Lämmitysmenetelmät ja syttyvyys.
- Joissakin yhteyksissä on ratkaisevaa, mitä lämmönlähdettä käytetään, kun taas toisissa yhteyksissä useat voivat toimia yhtä hyvin. Käytettävän lämmönlähteen valinta riippuu useista tekijöistä.
- Saatavuus (onko laitoksellasi laitteita?).
- Lämmitysnopeus (halutaanko lämmittää vähitellen vai nopeasti).
- Lämmityksen joustavuus (pitääkö lämpöä heilutella laitteen ympärillä?).
- tarvittava loppulämpötila (matalalla kiehuvat nesteet vaativat erilaisen lähestymistavan kuin korkealla kiehuvat nesteet).
- Sisällön syttyvyys
Koska turvallisuus on tärkeä tekijä laboratoriovalintoja tehtäessä, on tärkeää ottaa huomioon lämmitettävän nesteen syttyvyys. Lähes kaikkia orgaanisia nesteitä pidetään "syttyvinä", mikä tarkoittaa, että ne voivat syttyä tuleen ja jatkaa palamista (tärkeä poikkeus on, että halogenoidut liuottimet ovat yleensä palamattomia). Tämä ei kuitenkaan tarkoita, että kaikki orgaaniset nesteet syttyvät välittömästi, jos ne asetetaan lämmönlähteen lähelle. Monet nesteet vaativat syttymislähteen (kipinän, tulitikun tai liekin), jotta niiden höyryt syttyvät palamaan, ja tätä ominaisuutta kuvataan usein nesteen leimahduspisteellä. Leimahduspiste on lämpötila, jossa höyryt voivat syttyä sytytyslähteen avulla. Esimerkiksi 70-prosenttisen etanolin leimahduspiste on 16,6 ℃, mikä tarkoittaa, että se voi syttyä palamaan huoneenlämmössä tulitikun avulla. Bunsen-poltin on erinomainen sytytyslähde (ja se voi saavuttaa noin 1500 ℃:n lämpötilan), joten polttimet ovat vakava palovaara orgaanisten nesteiden kanssa ja lämmönlähde, jota tulisi usein välttää.
Toinen tärkeä ominaisuus syttyvyydestä keskusteltaessa on nesteen itsesyttymislämpötila: lämpötila, jossa aine syttyy spontaanisti normaalipaineessa ja ilman sytytyslähdettä. Tämä ominaisuus on erityisen tärkeä, koska se ei edellytä liekkiä (jota usein vältetään orgaanisessa laboratoriossa), vaan ainoastaan kuumaa aluetta. Kuumalevyn pinta, joka on käännetty "korkealle", voi saavuttaa jopa 350 ℃:n lämpötilan. Turvallisuushuomautus: koska dietyylieetterin, pentaanin, heksaanin ja vähän kiehuvan petrolieetterin itsesyttymislämpötilat ovat alle tämän arvon (kuva 14), olisi vaarallista keittää näitä liuottimia kuumalevyllä, koska höyryt voisivat valua ulos astiasta ja syttyä kosketuksesta kuumalevyn pintaan. Yleisesti ottaen on noudatettava varovaisuutta, kun keittolevyä käytetään minkä tahansa haihtuvan, syttyvän nesteen lämmittämiseen avoimessa astiassa, sillä höyryt voivat päästä keittolevyn keraamisen päällysteen yli ja koskettaa sen alla olevaa lämmityselementtiä, joka voi olla kuumempi kuin 350oC. Tästä syystä keittolevyt eivät ole optimaalinen valinta, kun kuumennetaan avoimia astioita, joissa on haihtuvia orgaanisia nesteitä, vaikka joissakin tapauksissa niitä voidaan käyttää varovasti, kun ne on asetettu "matalalle" ja niitä käytetään hyvin ilmastoidussa huurrehuoneessa.
Toinen tärkeä ominaisuus syttyvyydestä keskusteltaessa on nesteen itsesyttymislämpötila: lämpötila, jossa aine syttyy spontaanisti normaalipaineessa ja ilman sytytyslähdettä. Tämä ominaisuus on erityisen tärkeä, koska se ei edellytä liekkiä (jota usein vältetään orgaanisessa laboratoriossa), vaan ainoastaan kuumaa aluetta. Kuumalevyn pinta, joka on käännetty "korkealle", voi saavuttaa jopa 350 ℃:n lämpötilan. Turvallisuushuomautus: koska dietyylieetterin, pentaanin, heksaanin ja vähän kiehuvan petrolieetterin itsesyttymislämpötilat ovat alle tämän arvon (kuva 14), olisi vaarallista keittää näitä liuottimia kuumalevyllä, koska höyryt voisivat valua ulos astiasta ja syttyä kosketuksesta kuumalevyn pintaan. Yleisesti ottaen on noudatettava varovaisuutta, kun keittolevyä käytetään minkä tahansa haihtuvan, syttyvän nesteen lämmittämiseen avoimessa astiassa, sillä höyryt voivat päästä keittolevyn keraamisen päällysteen yli ja koskettaa sen alla olevaa lämmityselementtiä, joka voi olla kuumempi kuin 350oC. Tästä syystä keittolevyt eivät ole optimaalinen valinta, kun kuumennetaan avoimia astioita, joissa on haihtuvia orgaanisia nesteitä, vaikka joissakin tapauksissa niitä voidaan käyttää varovasti, kun ne on asetettu "matalalle" ja niitä käytetään hyvin ilmastoidussa huurrehuoneessa.
.
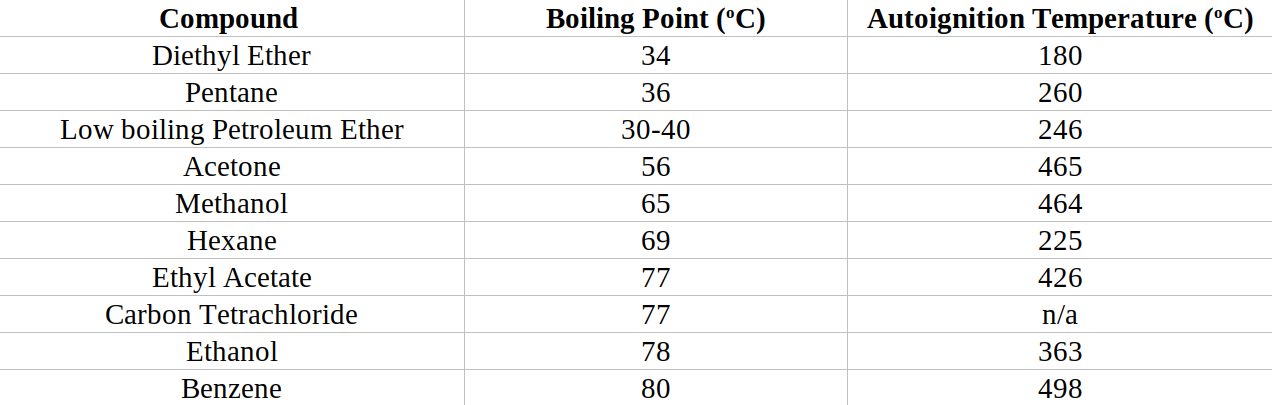
Koska palaminen on reaktio höyryfaasissa, nesteillä, joiden kiehumispisteet ovat alhaiset (< 40 ℃), on yleensä alhaiset leimahduspisteet ja itsesyttymislämpötilat, koska niiden höyrynpaineet ovat huomattavat (kuva 12). Kaikkiin matalalla kiehuviin nesteisiin on suhtauduttava varovaisemmin kuin nesteisiin, joiden kiehumispiste on kohtalainen (> 60 ℃).
Last edited by a moderator:


