Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 240
- Reaction score
- 270
- Points
- 63
El deseo compulsivo de comer, comer y volver a comer después de consumir cannabis, aunque el estómago no esté de acuerdo, es a la vez una maldición y una salvación. Todo depende del propósito con el que se consuma esta planta. Y el mecanismo recién descubierto de la acción de los cannabinoides en el cerebro resultó ser paradójico: el apetito indomable es causado por la estimulación de las neuronas hipotalámicas que normalmente forman la sensación de saciedad. Aquí también estaban implicados los "invasores bacterianos": las mitocondrias.
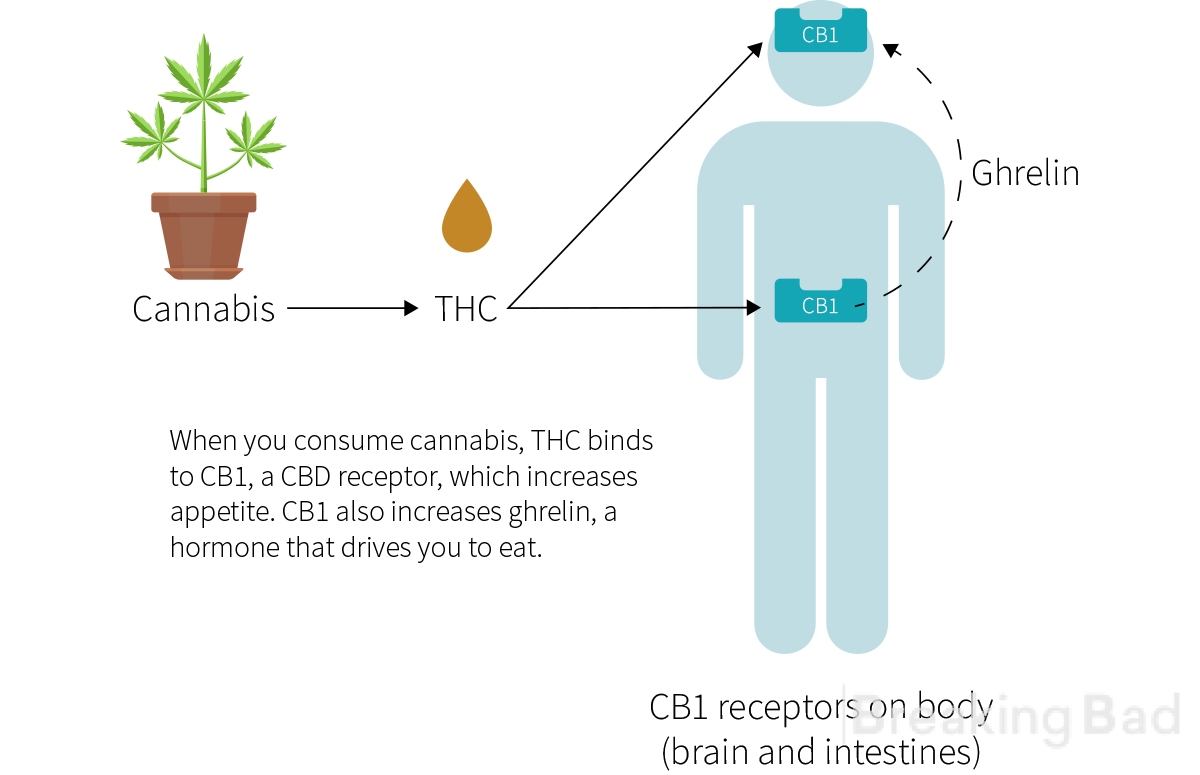
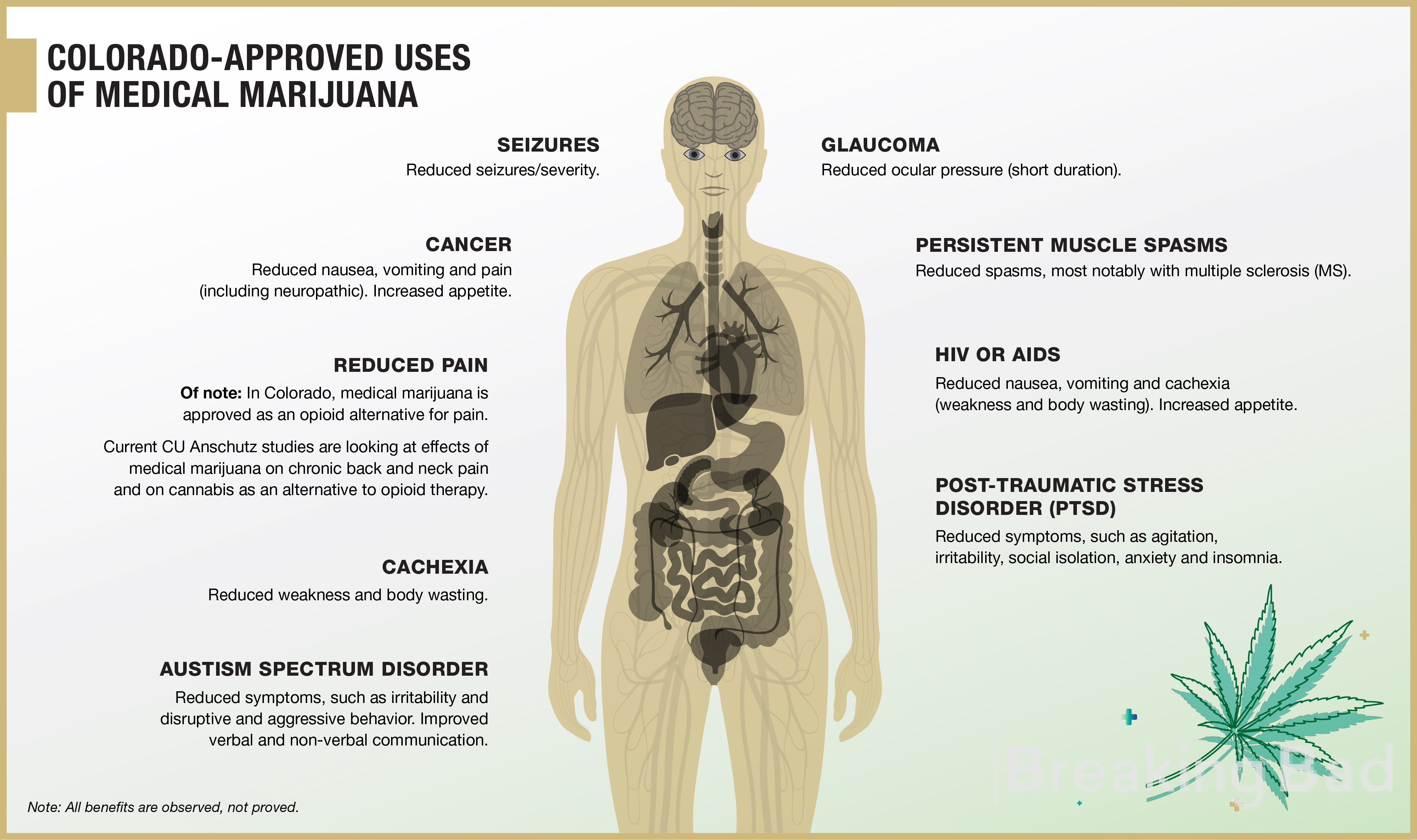
Este efecto del cannabis, popularmente descrito como "the munchies", es bien conocido e incluso se utiliza en medicina para aumentar el apetito de los pacientes que sufren una pérdida de peso debida a una anorexia dolorosa o a un tratamiento contra el cáncer especialmente tóxico. Las sustancias psicoactivas del cannabis, los cannabinoides, provocan este efecto. El más activo y estudiado es el terpenoide delta-9-tetrahidrocannabinol, o THC. Es este cannabinoide -sintéticamente bajo el nombre genérico de dronabinol- el que está aprobado para uso médico en Estados Unidos, Canadá y algunos países europeos. Dado que sus ventajas sobre otros antieméticos y analgésicos son cuestionables, el dronabinol se prescribe solo en casos de intolerancia a la terapia estándar.
En 2015, investigadores de la Universidad de Yale (EE UU) dirigidos por Tamas Horvath descubrieron lo paradójico de estos mecanismos: el apetito se despierta por la activación de circuitos cerebrales, cuya función normal es crear la sensación de saciedad, pero no de hambre incontrolable en absoluto. Sin embargo, la paradoja resultó ser sólo externa: un estudio realizado en una línea especial de ratones modificados genéticamente arrojó luz sobre el "hackeo" del sistema de sensación de saciedad. Seexplicaba por un complejo modo de funcionamiento de un grupo especial de neuronas hipotalámicas productoras de proopiomelanocortina, un precursor de varias hormonas, entre ellas la hormona adrenocorticotrópica, las hormonas estimulantes de los melanocitos y el opioide endógeno β-endorfina.
En 2015, investigadores de la Universidad de Yale (EE UU) dirigidos por Tamas Horvath descubrieron lo paradójico de estos mecanismos: el apetito se despierta por la activación de circuitos cerebrales, cuya función normal es crear la sensación de saciedad, pero no de hambre incontrolable en absoluto. Sin embargo, la paradoja resultó ser sólo externa: un estudio realizado en una línea especial de ratones modificados genéticamente arrojó luz sobre el "hackeo" del sistema de sensación de saciedad. Seexplicaba por un complejo modo de funcionamiento de un grupo especial de neuronas hipotalámicas productoras de proopiomelanocortina, un precursor de varias hormonas, entre ellas la hormona adrenocorticotrópica, las hormonas estimulantes de los melanocitos y el opioide endógeno β-endorfina.
El eslabón central en la regulación del apetito
La regulación central del apetito corre a cargo de las vías de señalización hipotalámicas, predominantemente del núcleo arqueado. El hipotálamo, debido a la ausencia local de la barrera hematoencefálica, integra las señales hormonales procedentes del aparato digestivo, el tejido adiposo y el sistema de recompensa cerebral, y en función de ellas genera "órdenes" que debilitan o aumentan el metabolismo, la motilidad intestinal y el apetito. Las células del núcleo arqueado transmiten señales a las neuronas de orden II de otras partes del hipotálamo, especialmente del núcleo paraventricular, donde se producen las hormonas que regulan la actividad del sistema nervioso simpático y la función de las glándulas tiroides y suprarrenales.
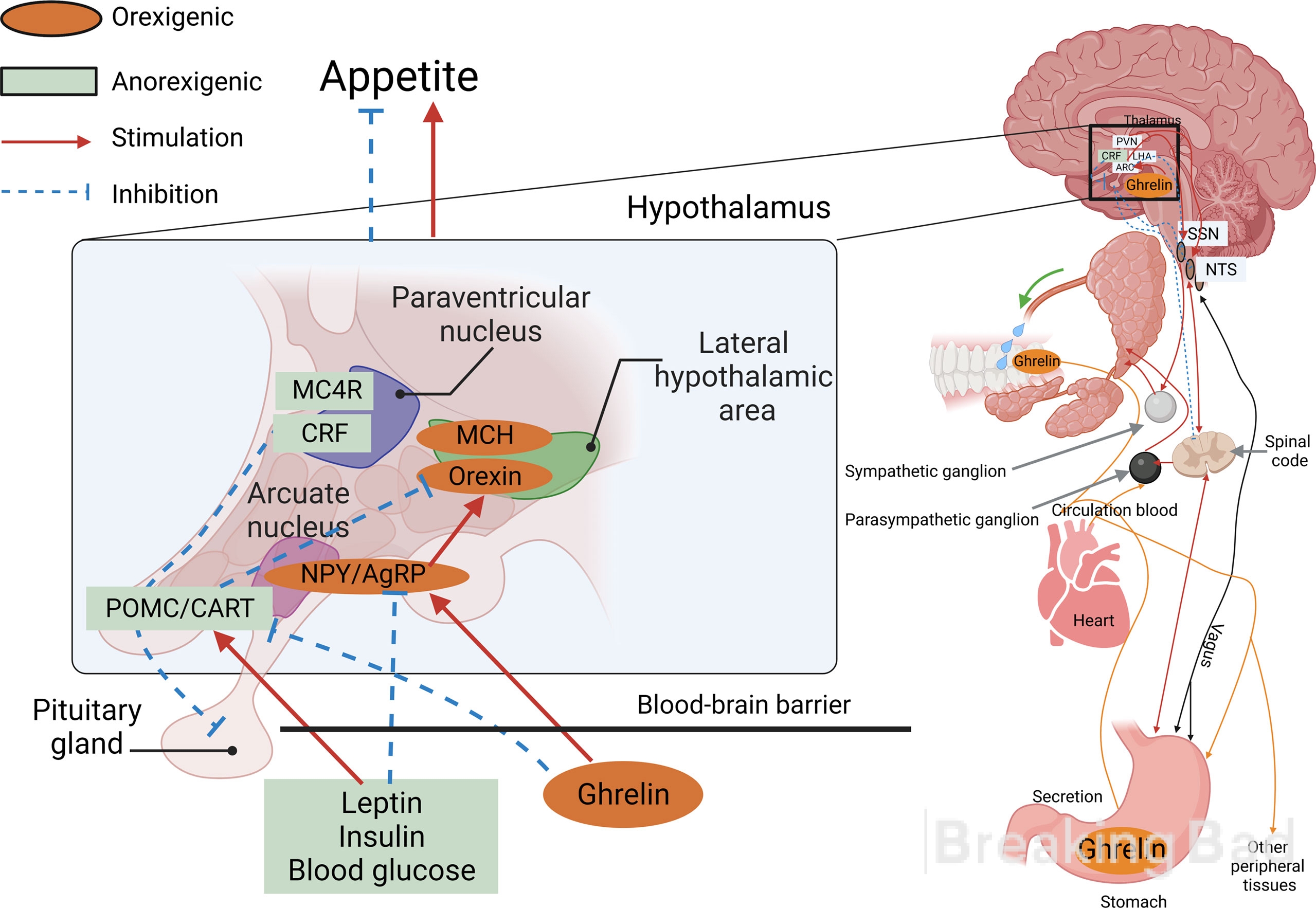
Dentro del núcleo en forma de arco del hipotálamo hay dos poblaciones de neuronas que actúan en direcciones diferentes y mantienen así el equilibrio energético del organismo (la imagen muestra el mecanismo molecular del mantenimiento de dicho equilibrio y de la regulación del apetito).
La imagen muestra el mecanismo molecular del mantenimiento de dicho equilibrio y de la regulación del apetito. Dentro del núcleo en forma de arco del hipotálamo hay dos poblaciones de neuronas que actúan en direcciones diferentes y mantienen así el equilibrio energético del cuerpo.
La regulación central del apetito corre a cargo de las vías de señalización hipotalámicas, predominantemente del núcleo arqueado. El hipotálamo, debido a la ausencia local de la barrera hematoencefálica, integra las señales hormonales procedentes del aparato digestivo, el tejido adiposo y el sistema de recompensa cerebral, y en función de ellas genera "órdenes" que debilitan o aumentan el metabolismo, la motilidad intestinal y el apetito. Las células del núcleo arqueado transmiten señales a las neuronas de orden II de otras partes del hipotálamo, especialmente del núcleo paraventricular, donde se producen las hormonas que regulan la actividad del sistema nervioso simpático y la función de las glándulas tiroides y suprarrenales.
Dentro del núcleo en forma de arco del hipotálamo hay dos poblaciones de neuronas que actúan en direcciones diferentes y mantienen así el equilibrio energético del organismo (la imagen muestra el mecanismo molecular del mantenimiento de dicho equilibrio y de la regulación del apetito).
La imagen muestra el mecanismo molecular del mantenimiento de dicho equilibrio y de la regulación del apetito. Dentro del núcleo en forma de arco del hipotálamo hay dos poblaciones de neuronas que actúan en direcciones diferentes y mantienen así el equilibrio energético del cuerpo.
- Las neuronasque producen péptidos orexigénicos que estimulan el apetito y disminuyen la tasa metabólica y el gasto energético son la proteína agouti-like y el neuropéptido Y (el péptido predominante del SNC).
- Las neuronas que producen neuropéptidos anorexígenos supresores del apetito son la proopiomelanocortina y el transcrito regulado por cocaína y anfetamina. Aún se sabe poco sobre el transcrito regulado por cocaína y anfetamina. Parece ser un psicoestimulante endógeno, con un efecto similar al de la anfetamina y la cocaína, y un objetivo potencial para la terapia de la adicción. Las mutaciones del gen CARTPT se han relacionado con la propensión al alcoholismo. Se cree que el CARTPT desempeña un papel clave en la modulación de la actividad de la vía mesolímbica dopaminérgica del sistema de recompensa cerebral. Seha demostrado que este péptido reduce el apetito y la tasa de acumulación de grasa, y una disminución de su actividad en el hipotálamo de los animales (en la depresión, por ejemplo) conduce a la glotonería y la obesidad.
Enlace periférico en la regulación del apetito
Se cree que los principales moduladores periféricos del comportamiento alimentario son las hormonas insulina, leptina y grelina, que tienen una influencia dirigida de forma diferente sobre la actividad de las neuronas hipotalámicas.
Leptina - es segregada por las células del tejido adiposo cuando se ingieren alimentos, en proporción a la cantidad de grasa en el cuerpo, y reduce el apetito.
Insulina - es segregada por las células β de los islotes de Langerhans del páncreas después de una comida. La acción periférica de la insulina es anabólica y anticatabólica: aumenta la síntesis de grasas y proteínas, aumenta la entrada de glucosa en las células (disminuyendo su nivel en sangre), estimula la formación de glucógeno a partir de la glucosa e inhibe la degradación del glucógeno y las grasas. El efecto central de la insulina, por el contrario, es catabólico - reduce el apetito, desplazando el balance energético hacia el lado del "gasto".
Tanto la leptina como la insulina interactúan con ambas poblaciones neuronales: inhiben las células NP-y/APB ourexigénicas y activan las células POMC/CART condicionalmente anorexigénicas (ver figura con diagrama molecular). La leptina, además, reduce la salida del mediador inhibitorio GABA de los axones en contacto con las neuronas POMC. Todo esto conduce generalmente a un efecto anorexígeno - supresión del apetito.
Las células GI sintetizan una serie de hormonas anorexígenas y sólo un péptido estimulante del apetito, la grelina (hormona del hambre). Es producida por las paredes del estómago y del intestino delgado durante la inanición y en el cerebro interactúa con los receptores de la hormona del crecimiento (GHSR1a) y estimula su secreción, por lo que fue bautizada: inductora de la liberación de la hormona del crecimiento (ghrelina). En el núcleo arqueado del hipotálamo, la ghrelina excita las neuronas NP-y/APB, empujando a la gente a comer, y también media en el placer del alcohol y de la comida deliciosa.
Puntos de aplicación de los cannabinoides en este esquema
Como hemos descubierto, la consecuencia de la estimulación de las neuronas POMC es una disminución del apetito, y la de las neuronas APB es un aumento del apetito. Por lo tanto, sería lógico explicar el fenómeno de "the munchies" tras el consumo de marihuana por la inhibición de la primera población celular y/o la activación de la segunda. Sin embargo, un estudio reciente realizado por el grupo de Tamas Horvath descubrió que, en realidad, el cannabis actúa exactamente al revés: el hambre en personas bien alimentadas es provocada por la activación de las neuronas POMC, mientras que las células APB permanecen "silenciosas".
Basándose en las pruebas recopiladas, los autores del trabajo propusieron un esquema de excitación de las neuronas POMC por los cannabinoides, que incluye dos vías.
Se cree que los principales moduladores periféricos del comportamiento alimentario son las hormonas insulina, leptina y grelina, que tienen una influencia dirigida de forma diferente sobre la actividad de las neuronas hipotalámicas.
Leptina - es segregada por las células del tejido adiposo cuando se ingieren alimentos, en proporción a la cantidad de grasa en el cuerpo, y reduce el apetito.
Insulina - es segregada por las células β de los islotes de Langerhans del páncreas después de una comida. La acción periférica de la insulina es anabólica y anticatabólica: aumenta la síntesis de grasas y proteínas, aumenta la entrada de glucosa en las células (disminuyendo su nivel en sangre), estimula la formación de glucógeno a partir de la glucosa e inhibe la degradación del glucógeno y las grasas. El efecto central de la insulina, por el contrario, es catabólico - reduce el apetito, desplazando el balance energético hacia el lado del "gasto".
Tanto la leptina como la insulina interactúan con ambas poblaciones neuronales: inhiben las células NP-y/APB ourexigénicas y activan las células POMC/CART condicionalmente anorexigénicas (ver figura con diagrama molecular). La leptina, además, reduce la salida del mediador inhibitorio GABA de los axones en contacto con las neuronas POMC. Todo esto conduce generalmente a un efecto anorexígeno - supresión del apetito.
Las células GI sintetizan una serie de hormonas anorexígenas y sólo un péptido estimulante del apetito, la grelina (hormona del hambre). Es producida por las paredes del estómago y del intestino delgado durante la inanición y en el cerebro interactúa con los receptores de la hormona del crecimiento (GHSR1a) y estimula su secreción, por lo que fue bautizada: inductora de la liberación de la hormona del crecimiento (ghrelina). En el núcleo arqueado del hipotálamo, la ghrelina excita las neuronas NP-y/APB, empujando a la gente a comer, y también media en el placer del alcohol y de la comida deliciosa.
Puntos de aplicación de los cannabinoides en este esquema
Como hemos descubierto, la consecuencia de la estimulación de las neuronas POMC es una disminución del apetito, y la de las neuronas APB es un aumento del apetito. Por lo tanto, sería lógico explicar el fenómeno de "the munchies" tras el consumo de marihuana por la inhibición de la primera población celular y/o la activación de la segunda. Sin embargo, un estudio reciente realizado por el grupo de Tamas Horvath descubrió que, en realidad, el cannabis actúa exactamente al revés: el hambre en personas bien alimentadas es provocada por la activación de las neuronas POMC, mientras que las células APB permanecen "silenciosas".
Basándose en las pruebas recopiladas, los autores del trabajo propusieron un esquema de excitación de las neuronas POMC por los cannabinoides, que incluye dos vías.
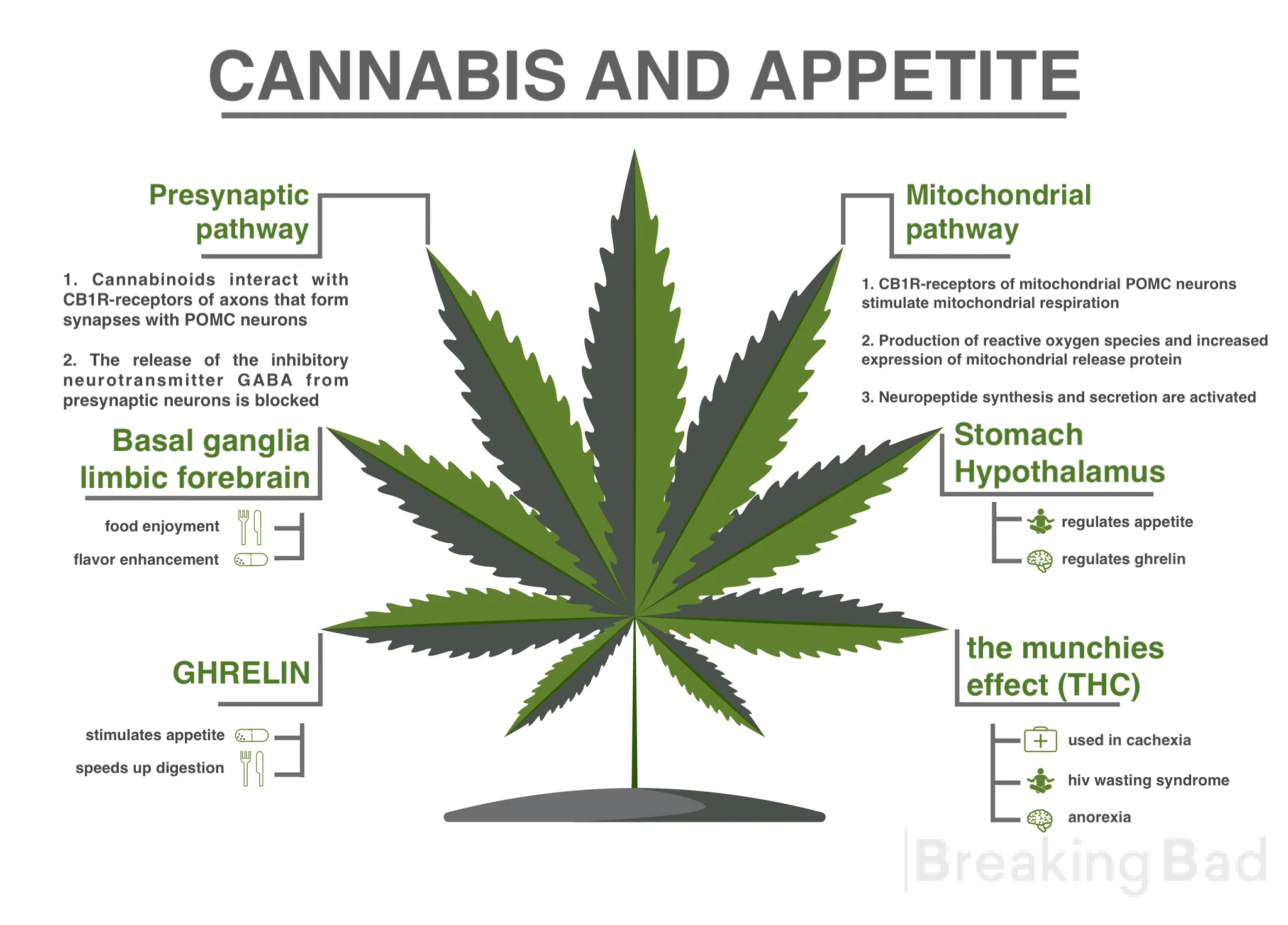
- Vía presináptica: Cuando los cannabinoides interactúan con los receptores CB1R de los axones que forman sinapsis con las neuronas POMC, se bloquea la liberación del neurotransmisor inhibidor GABA de las neuronas presinápticas (por ejemplo, las células APB). Comoresultado, las neuronas POMC pueden excitarse.
- Vía mitocondrial (nueva y básica): cuando los cannabinoides interactúan con los receptores CB1R de las neuronas POMC mitocondriales, se estimula la respiración mitocondrial, se producen especies reactivas de oxígeno (ROS) y aumenta la expresión de la proteína desacoplante mitocondrial 2 (RB2, UCP2). Esta proteína es la que interviene en la regulación de la producción de AFC y del comportamiento alimentario.
¿Pero por qué, en este caso, las células secretan β-endorfina? El hecho es que la α-MSH de acción opuesta y la β-endorfina son codificadas por el mismo gen Pomc, ya que son formadas por conversiones post-traduccionales del mismo péptido POMC. Los niveles de expresión génica de las dos convertasas que llevan a cabo esta formación no difieren cuando los cannabinoides se unen a los receptores CB1R.
Aparentemente, la α-MSH y la β-endorfina también se producen en cantidades iguales en este caso, pero son secretadas selectivamente por las neuronas POMC. Tamas Horvath y sus colegas mostraron que cerca del 35% de los brotes neuronales POMC que forman sinapsis con neuronas del núcleo paraventricular contienen vesículas secretoras con α-MSH o β-endorfina. Es decir, estos péptidos se producen sincrónicamente y en cantidades iguales, pero se almacenan por separado, y lo más importante, son secretados por las neuronas POMC bajo el control de diferentes señales. La RB2 bajo la influencia de los cannabinoides "cambia la flecha" de la vía de secreción de α-MSH, que reduce el apetito, a la vía de secreción de β-endorfina, que provoca un apetito irresistible (y posiblemente obesidad).
Todavía no se sabe si el efecto descrito de la PB2 es exclusivo de la población de neuronas POMC, porque anteriormente se ha demostrado que esta proteína también es producida por muchas otras células del sistema nervioso. Tampoco se sabe si las neuronas de otras regiones del cerebro responden a los cannabinoides exactamente de la misma manera. El equipo de Yale se centró específicamente en la alimentación incontrolada mediada por CB1R de animales saciados, que es exactamente lo que hacen los amantes de los cannabinoides. Es posible que las neuronas hipotalámicas POMC también estén implicadas en el desarrollo de otros síntomas asociados al consumo de marihuana.
Conclusión
Así, paradójicamente, las neuronas que normalmente inducen una sensación de saciedad se convierten en la fuerza impulsora del consumo de alimentos bajo la influencia del THC. El cannabis activa el bulbo olfatorio del cerebro (el departamento responsable de reconocer los olores), lo que hace que la comida huela mejor y más fuerte. El THC también actúa sobre los receptores de una zona del cerebro llamada núcleo adyacente, lo que aumenta la liberación del neurotransmisor dopamina. La liberación de dopamina aumenta la sensación de placer al comer colocado. El cerebro libera dopamina de forma natural cuando comemos alimentos placenteros, pero cuando el THC está presente, tu cuerpo obtiene una liberación adicional de dopamina de lo que comes.
El THC también interactúa con los receptores CB1 en el hipotálamo para liberar una hormona llamada grelina, una hormona que estimula el apetito y acelera la digestión. ElTHC no sólo estimula esta hormona, sino que la grelina también es responsable de crear la sensación de hambre, que desempeña un papel en el metabolismo de los carbohidratos, razón por la que los científicos plantean la hipótesis de que el THC te hace sentir hambre y desear sustancias ricas en carbohidratos.
Aparentemente, la α-MSH y la β-endorfina también se producen en cantidades iguales en este caso, pero son secretadas selectivamente por las neuronas POMC. Tamas Horvath y sus colegas mostraron que cerca del 35% de los brotes neuronales POMC que forman sinapsis con neuronas del núcleo paraventricular contienen vesículas secretoras con α-MSH o β-endorfina. Es decir, estos péptidos se producen sincrónicamente y en cantidades iguales, pero se almacenan por separado, y lo más importante, son secretados por las neuronas POMC bajo el control de diferentes señales. La RB2 bajo la influencia de los cannabinoides "cambia la flecha" de la vía de secreción de α-MSH, que reduce el apetito, a la vía de secreción de β-endorfina, que provoca un apetito irresistible (y posiblemente obesidad).
Todavía no se sabe si el efecto descrito de la PB2 es exclusivo de la población de neuronas POMC, porque anteriormente se ha demostrado que esta proteína también es producida por muchas otras células del sistema nervioso. Tampoco se sabe si las neuronas de otras regiones del cerebro responden a los cannabinoides exactamente de la misma manera. El equipo de Yale se centró específicamente en la alimentación incontrolada mediada por CB1R de animales saciados, que es exactamente lo que hacen los amantes de los cannabinoides. Es posible que las neuronas hipotalámicas POMC también estén implicadas en el desarrollo de otros síntomas asociados al consumo de marihuana.
Conclusión
Así, paradójicamente, las neuronas que normalmente inducen una sensación de saciedad se convierten en la fuerza impulsora del consumo de alimentos bajo la influencia del THC. El cannabis activa el bulbo olfatorio del cerebro (el departamento responsable de reconocer los olores), lo que hace que la comida huela mejor y más fuerte. El THC también actúa sobre los receptores de una zona del cerebro llamada núcleo adyacente, lo que aumenta la liberación del neurotransmisor dopamina. La liberación de dopamina aumenta la sensación de placer al comer colocado. El cerebro libera dopamina de forma natural cuando comemos alimentos placenteros, pero cuando el THC está presente, tu cuerpo obtiene una liberación adicional de dopamina de lo que comes.
El THC también interactúa con los receptores CB1 en el hipotálamo para liberar una hormona llamada grelina, una hormona que estimula el apetito y acelera la digestión. ElTHC no sólo estimula esta hormona, sino que la grelina también es responsable de crear la sensación de hambre, que desempeña un papel en el metabolismo de los carbohidratos, razón por la que los científicos plantean la hipótesis de que el THC te hace sentir hambre y desear sustancias ricas en carbohidratos.
