Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 240
- Reaction score
- 270
- Points
- 63
El desarrollo de la adicción a las sustancias psicoactivas sintéticas es un problema social relevante en la mayoría de los países del mundo, que en la actualidad ha adquirido importancia nacional. Esta cuestión requiere atención mundial, en primer lugar, debido al rápido crecimiento del número de personas implicadas en el consumo de sustancias psicoactivas y, en segundo lugar, debido a las consecuencias del comportamiento antisocial de estas personas: comisión de delitos, desarrollo de diversas enfermedades causadas por el abuso de sustancias psicoactivas.
Una de estas sustancias psicoactivas es la mezcla de hierbas para fumar - "spice". Está disponible en el mercado en forma de hierbas con una sustancia química aplicada, y ha ganado rápidamente popularidad entre los jóvenes.
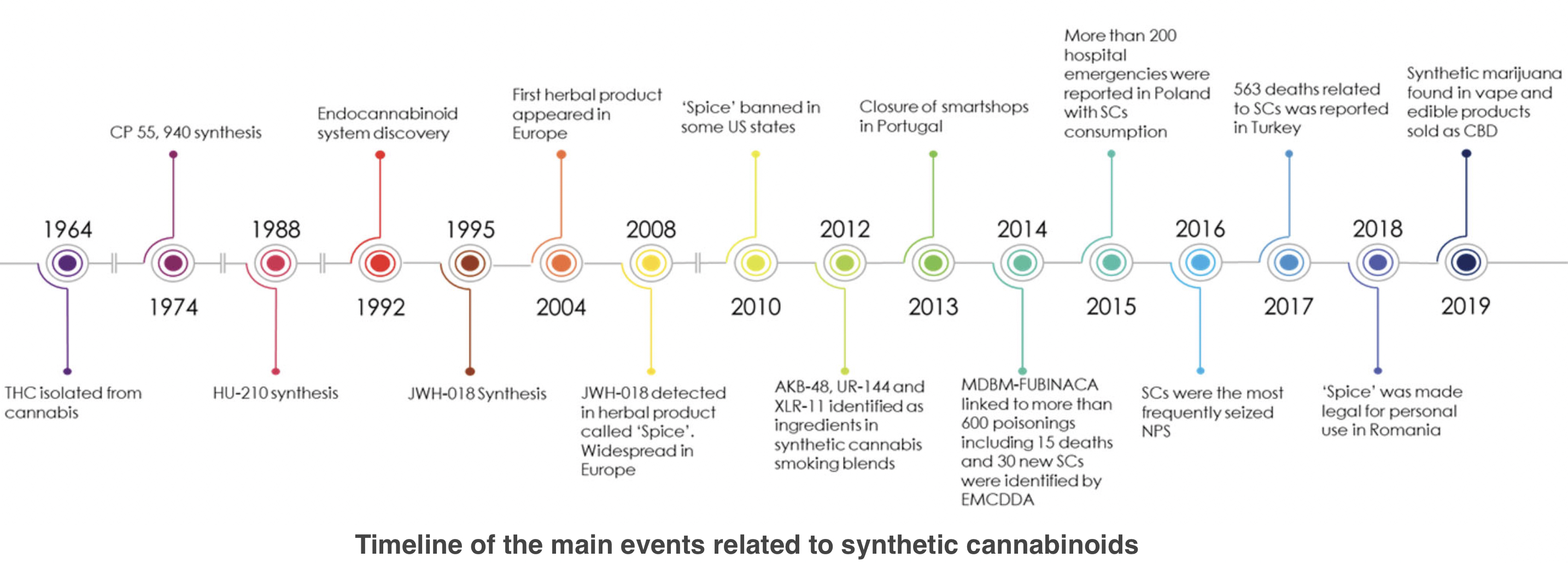
Clasificación de las sustancias que forman parte de las mezclas para fumar:
1. 1. Cannabinoides clásicos -ocannabinol, otros compuestos químicos presentes en el cannabis y análogos sintéticos estructuralmente relacionados, por ejemplo, AM-411, AM-906, HU-210, O-1184;
2. 2. Cannabinoides no clásicos: ciclohexilfenoles o 3-arilciclohexanoles, por ejemplo, CP-55.244, CP-55.940, CP-47.497 (y homólogos de C6-9);
3. 3. Cannabinoides híbridos: combinaciones de características estructurales de cannabinoides clásicos y no clásicos, por ejemplo, AM-4030;
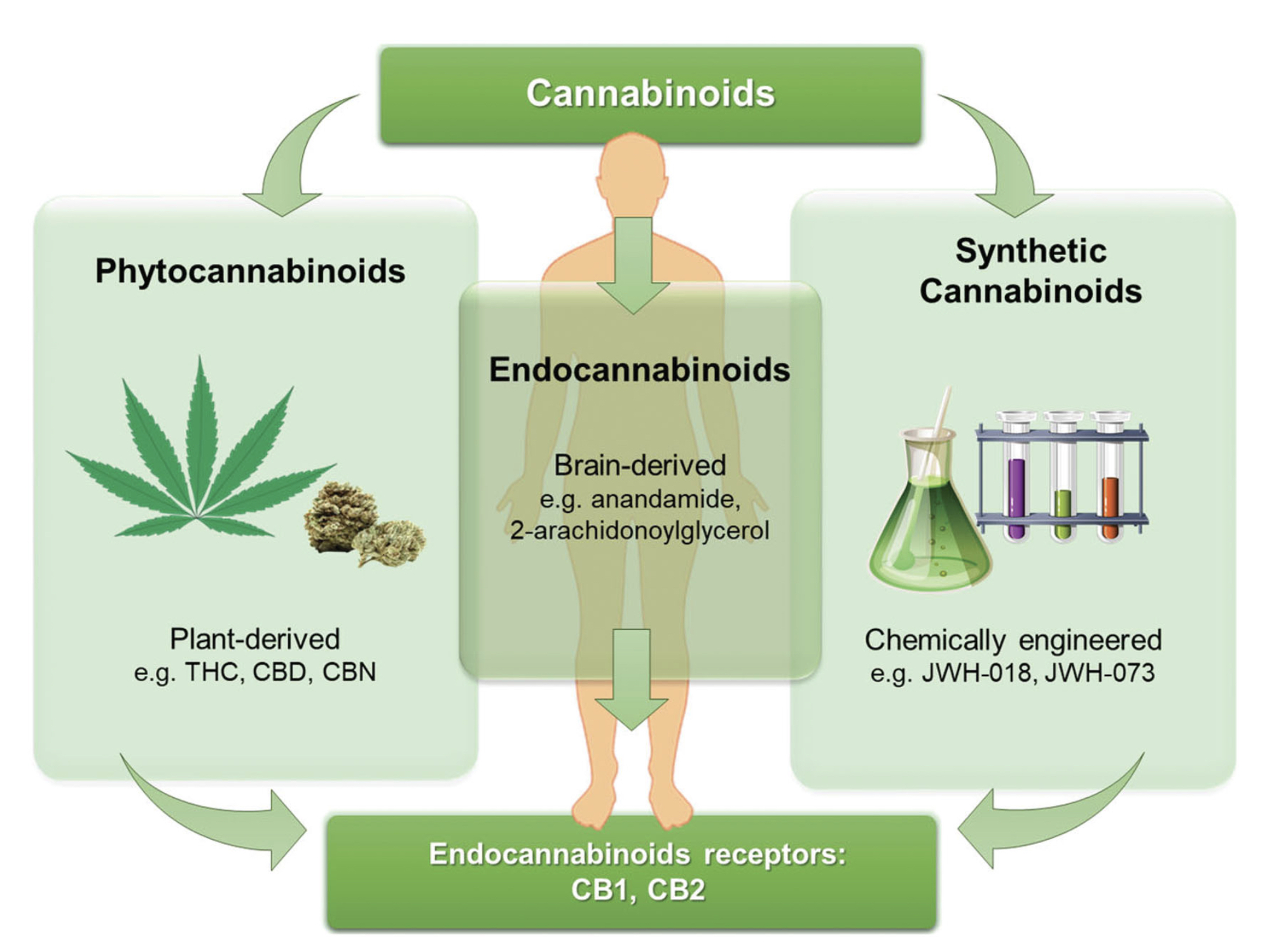
4. Eicosanoides - endocannabinoides como la anandamida (AEA) y sus análogos sintéticos, por ejemplo, la metanandamida (AM-356);
5. Otros. Incluyen otros tipos estructurales - diarilpirazoles (por ejemplo, Rimonabant), naftoilpirroles (por ejemplo, JWH-307), naftilmetilindenos (por ejemplo, JWH-176) e indazolcarboxamidas (por ejemplo, APINACA).
6. Aminoalquilindoles, que pueden dividirse a su vez en los siguientes grupos
* fenilacetilindoles (JWH-250, JWH-251);
* benzoilindoles (pravadolina, AM-694, RSC-4);
* naftilmetilindoles (JWH-184);
* ciclopropoyl-idoles (UR-144, XLR-11);
* adamantoilindoles (AB-001, AM-1248);
* carboxamidas de indol (APICA, STS-135);
* naftoilindoles (por ejemplo, JWH-015, JWH-018, JWH-073, JWH-081, JWH-122, JWH-200, JWH-210, JWH-398);
Muchos derivados y análogos de las clases de compuestos mencionadas anteriormente pueden sintetizarse mediante la unión de halógenos, alquilos, alcoxilos u otros sustituyentes a uno de los sistemas cíclicos aromáticos.
El efecto de los cannabinoides clásicos.
Hasta la fecha, se conocen docenas de derivados del tetrahidrocannabinol que superan significativamente tanto al D8-THC como al D9-THC en términos de actividad biológica. Entre ellos se encuentran JWH-051, JWH-057, WH-102, JPG-103, así como D9-THC-3-dimetilheptilo, cannabinol-3-dimetilheptilo, 1-hidroxi-cannabinol-3-dimetilheptilo, 11-COOH-cannabinol-3-dimetilheptilo. Se detectó una alta afinidad por los receptores CB1 y una pronunciada actividad biológica en los derivados del D8-THC con varios radicales en la posición 3. Todos estos agentes tienen la estructura del tetrahidrocannabinol. Las propiedades del HU-210 se describen con más detalle a continuación.
Se sabe que el proceso de excitación del receptor cannabinoide implica su interacción con una proteína de unión a nucleótidos de guanina (proteína G). Sin dicha interacción, es imposible la posterior modulación de los sistemas transductores implicados en la neurotransmisión endocannabinoide (adenilato ciclasa, proteína quinasa activada por mitógenos, canales de calcio y potasio).
La capacidad de los agonistas cannabinoides para iniciar la interacción del receptor con la proteína G suele estimarse mediante el aumento de la unión de 35S-guanosina-5'-(-tio) - trifosfato (35S-GTPS). Se descubrió que el HU-210 potenciaba la unión del 35S-GTPS a los receptores CB1 humanos expresados en varios sistemas celulares, superando significativamente al D9-tetrahidrocannabinol y a otros agonistas CB1 en este indicador. Por ejemplo, con respecto a los receptores del primer subtipo expresados en células HEK-239, la capacidad de HU-210 para potenciar la unión de 35S-GTPS superó el indicador para CP-55940 en 11-17 veces, y para WIN-55212-2 - en 79 veces. Los receptores CB1 humanos se expresaron en el mismo sistema celular - en células HEK-239. El efecto del HU-210 fue 24 veces superior al del CP-55940 y 872 veces superior al del WIN-55212-2. En las preparaciones de las membranas sinápticas del cerebro de ratón, C57BL/6 HU-210 estimuló la unión de 35S-GTPS más activamente en comparación con D9-tetrahidrocannabinol. Superó al D9-THC en 28 veces, al CP-55940- en 2 veces, al WIN-55212-2 -en 59 veces, al JWH-073- en 12 veces. Hay que tener en cuenta que los compuestos CP-55940 y WIN-55212-2 se caracterizan por una elevada actividad biológica frente a los sistemas cannabinoides y se utilizan ampliamente en la investigación científica como eficaces agonistas del receptor CB1.
La inhibición cannabinoide de la actividad de la adenilato ciclasa estimulada por la forskolina se considera un importante equivalente neuroquímico de sus efectos farmacológicos. El HU-210 fue superior en este indicador a los cannabinoides CP-55940, anandamida, WIN-55212-2 y D9-THC, lo que también indica un alto potencial biológico del agente. Así, el IC50 del D9-tetrahidrocannabinol hacia la adenilato ciclasa (expresada en células CHO) fue de 16,51,2 nM, mientras que para la HU-210 fue de 0,1970,012 nM.
Como se deduce de lo anterior, los cannabinoides clásicos de la lista 1 HU-210 tienen una afinidad pronunciada por los receptores CB1, superando al D9-THC en este indicador. Esto sugiere que la sustancia psicoactiva considerada tiene una actividad biológica pronunciada y un potencial adictivo significativo, ya que para los agonistas cannabinoides, como para los agonistas de otros receptores, se observa una correlación directa entre la afinidad del receptor y la gravedad de los efectos biológicos. En experimentos con ratones, el HU-210 superó al D9-tetrahidrocannabinol en su capacidad de inhibir la SDA en 2900 veces, en su acción hipotérmica - en 900 veces, en su actividad antinociceptiva - en 240 veces.
El alto potencial adictivo del HU-210 se reveló en los primeros años tras su síntesis. En la prueba de discriminación con ratas macho Sprague-Dowley y palomas, la actividad adictiva del HU-210 superó el mismo indicador para el D9-THC en 66 y 80 veces, respectivamente. En estudios que utilizaron el método de aprendizaje para distinguir (discriminar) sustancias, el potencial adictivo del HU-210 fue muchas veces superior al de los agonistas CB1 de alta afinidad CP-55940 y BAY 38-7271, y diez veces superior en comparación con el D9-tetrahidrocannabinol.
El efecto de los cannabinoides no clásicos.
En la historia del estudio de las propiedades del CP-47497 se distinguen dos etapas. Inicialmente, se determinó la alta eficacia biológica de este fármaco, incluido un pronunciado potencial adictivo. Se cree que la actividad farmacológica del agente es aproximadamente 10 veces superior a la del D9-tetrahidrocannabinol. Más tarde, a medida que se introducían nuevos ligandos de los receptores CB1 y CB2, empezó a aparecer información sobre la gran afinidad de los receptores cannabinoides del primer subtipo por el CP-47497 y sus homólogos. Como se muestra, la mayor afinidad se detectó en el CP-47497 y en el CP-47497-C8.
En el estudio se evaluaron por primera vez los equivalentes conductuales a las exposiciones a CP-47497. El potencial antinociceptivo del agente en roedores (se utilizaron métodos de apretar la base de la cola, prueba de deslizamiento de la cola, etc.) fue comparable al de la morfina y superó al D9-tetrahidrocannabinol en varias veces. El agente CP-47497 resultó ser mucho más eficaz cuando se probó la inhibición de la actividad motora espontánea en roedores, el debilitamiento de la actividad convulsiva (choque electroconvulsivo), la acción hipotérmica y la inducción de ataxia en perros en comparación con el D9-THC. El potencial adictivo (según los resultados del método de discriminación en ratas) también fue muy superior al indicador del D9-tetrahidrocannabinol.
El CP-55940, un homólogo que tiene n-butanol en lugar de propanol en la posición 4 del anillo de ciclohexano, muestra una elevada actividad biológica. La afinidad de este compuesto es muchas veces superior al indicador correspondiente del CP-47497 (Ki = 1,12 ± 0,17 nM), y la actividad analgésica (evaluada mediante la prueba de retorcimiento en ratones) fue más de 4 veces superior en comparación con un efecto similar del CP-47497. El efecto antinociceptivo de otro homólogo que tiene propilciclohexano en la posición 4 es más de 6 veces superior al del CP-47497, y el Ki fue de 1,30 ± 0,57 nM. Cuando se alteró la estructura de la molécula CP-55940 con la sustitución del anillo de ciclohexano por cicloheptano, aumentó la afinidad por los receptores CB1 (Ki = 0,17 ± 0,04 nM) y la actividad analgésica (en 16 veces).
Aminoalquilindoles, indolilnaftilmetanos, indenos, pirroles y otros cannabinoides.
La primera síntesis del ancestro de los aminoalquilindoles WIN-55212-2 se llevó a cabo en 1991. Entonces, se estableció la elevada actividad biológica del WIN-55212-2 (en estudios con radioligandos y en experimentos con órganos aislados), y también se demostró su potencial adictivo (un método de entrenamiento de la discriminación). El WIN-55212-2 ha encontrado una amplia aplicación como sonda farmacológica de los receptores cannabinoides. También se utiliza con éxito como radioligando (3H-WIN-55212-2).
La actividad agonista de los aminoalquilindoles puede estimarse por el aumento de la unión específica de 35S-Gtp a las membranas del cerebro de roedores. Se demostró que el JWH-073 aumentaba la unión del análogo del GTP a las membranas sinápticas del cerebro de ratón en un 59% con respecto al nivel basal, con una EC50 = 34 nM. Para el D9-THC, los valores correspondientes fueron del 40% y 81 nM, respectivamente. La eficacia agonística de otros agentes fue significativamente mayor: para HU- 210, la ganancia máxima fue del 110% a ЕС50= 2,9 nM; los mismos indicadores para CP-55940 - 120% y 6,1 nM; para CP-55244 -120% y 0,12 nM. Al utilizar membranas cerebelosas de ratón como material biológico, la actividad de unión de JWH-073 a 35S-GTPgS fue menor: el aumento máximo alcanzó el 53%, ЕС50 = 490 nM. Los valores correspondientes para CP-55940 fueron 134% y 20 nM; para D9-THC - 54% y 260 nM.
Los efectos de los grupos de "nuevos cannabinoides" sobre la actividad de la adenilato ciclasa pueden demostrarse con un ejemplo de JWH-018. En el estudio, el efecto cannabinoide sobre la capacidad de inhibir la actividad de la adenilato ciclasa estimulada por la forskolina (valores en nM; los receptores CB1 humanos y la adenilato ciclasa se coexpresan en células CHO) fue el siguiente: CP-55940 = 5,5 ± 2,9; WIN-55212-2 = 38,9 ± 8,2; JWH-018 = 14,7 ± 3,9.
Entre las sustancias de los grupos considerados, hay agentes con una gran afinidad por los receptores cannabinoides. Por ejemplo, el compuesto JWH-048 era 4 veces superior al D9-ТHK en afinidad por los receptores CB1, y en su capacidad de cambiar los indicadores vegetativos y de comportamiento (inhibición de la SDA, efecto antinociceptivo, efecto hipotérmico) no era inferior al alcaloide del cannabis. También se encontró una alta afinidad por los receptores CB1 en JWH-164, JWH-180, JWH-181, JWH-182, JWH-210, JWH-212, JWH-213, JWH-234, JWH-240, JWH-242, JWH-258 y JWH-262. Sus constantes de inhibición de la unión específica del ligando CB1 3H-CP-55940 con las membranas sinápticas del cerebro de roedor fueron de 6,6 ± 0,7 nM; 26 ± 2 nM; 1.3±0,1 nM; 0,65 ± 0,03 nM; 0,46 ± 0,03 nM; 33,0 ± 0,9 nM; 1,5 ± 0,2 nM; 8,4 ± 1,8 nM; 14 ± 1 nM; 42 ± 9 nM; 4,6 ± 0,6 nM y 28 ± 3 nM, respectivamente.
Un indicador similar para el D9-tetrahidrocannabinol fue de 41 ± 2 nM. El aminoalquilindol JWH-398 (1-pentil-3-(4-cloro-1-naftol)indol se aisló de mezclas de fumadores. La afinidad por los receptores CB1 de este agente es alta (Ki = 2,3 nM).
Los 1-pentil-3-fenilacetilindoles (no contienen radical naftaleno) presentaron una afinidad superior por los receptores CB1 que el D9-tetrahidrocannabinol: JWH-203-5,1 veces; JWH - 204-3,2 veces; JWH - 249-4,9 veces; JWH - 250-3,7 veces; JWH - 251-1,4 veces; JWH - 252-1,8 veces; JWH - 302-2,4 veces; JWH - 305-2,7 veces; JWH - 306-1,6 veces; JWH - 311-1,8 veces.
BAY 38-7271, un compuesto sintetizado en el laboratorio de la empresa alemana Bayer AG, tiene una gran afinidad por los receptores del primer subtipo. Los valores de la constante de disociación 3H-BAY 38-7271 en experimentos con radioligandos con membranas sinápticas de cerebros de rata y humanos, así como con receptores CB1 humanos clonados, oscilaron entre 1,84 y 2,91 nM. En una serie paralela de experimentos, se obtuvieron valores similares para un ligando generalmente reconocido 3H-CP-55940. BAY 38-7271 en términos de eficacia agonística (evaluada por el grado de aumento de la unión 35S-Gtp a las membranas sinápticas de la corteza cerebral humana y del cerebro completo de rata), fue muchas veces superior al D9-tetrahidrocannabinol. La actividad biológica de BAY 38-7271 (capacidad de provocar hipotermia en ratas tras inyección intraperitoneal o intravenosa) se define como inferior en comparación con el mismo indicador para HU-210, pero era comparable a la de CP-55940 y WIN-55212-2. En condiciones experimentales similares, fue significativamente inferior en comparación con BAY 38-7271 en términos de actividad hipotérmica. El potencial adictivo de BAY 38-7271 se evaluó en ratas utilizando el método de distinción (discriminación) de sustancias, fue inferior en comparación con indicadores similares para HU-210 y CP-55940, pero fue diez veces superior al parámetro correspondiente para D9-tetrahidrocannabinol. Todos los equivalentes conductuales enumerados de los cannabinoides fueron prevenidos por los antagonistas de los receptores CB1 rimonabant (SR-141716A). Esto indica que los efectos adictivos se realizan a través de los receptores del primer subtipo.
Aspectos clínicos del efecto sobre el organismo
Los receptores CB1 pertenecen a la familia de receptores unidos a proteínas G y están ampliamente distribuidos en áreas del cerebro cuyas funciones están asociadas al control de la actividad motora, las funciones cognitivas, las reacciones emocionales, el comportamiento motivado y la homeostasis. En cuanto al efecto psicoactivo, los ligandos de los receptores cannabinoides del primer subtipo son los más importantes. Su activación está representada por euforia, sedación, disminución de la actividad motora espontánea (AME), efectos antinociceptivos, hipotermia, catalepsia. La combinación de estos equivalentes conductuales y fisiológicos constituye la base del potencial adictivo de los cannabinoides. Si hablamos del impacto sobre el estado mental de una persona, también podemos añadir un efecto alucinógeno a esta lista.
Los receptores CB2 se localizan principalmente en las células inmunitarias, tanto dentro como fuera del sistema nervioso central. El funcionamiento de estos receptores implica la modulación de la emisión de citoquinas y la migración de las células inmunitarias. En el cerebro, los receptores CB2 están presentes en la microglía, los vasos sanguíneos y algunas neuronas.
Las sustancias psicoactivas, que forman parte de la composición de la "especia", tienen un fuerte efecto en la mayoría de los sistemas corporales. El daño cerebral es el más pronunciado. Fumar la composición provoca un espasmo agudo de los vasos cerebrales - esto ocurre de forma refleja para reducir el paso de sustancias tóxicas al tejido cerebral. La vasoconstricción conduce a la hipoxia, la reducción de la viabilidad de las células cerebrales y su muerte.
Además, las mezclas de humo tienen una gran influencia en el sistema nervioso central. El efecto de los ingredientes del humo sobre el sistema nervioso central provoca adicción a fumar "picante". Como resultado, pueden manifestarse diversas reacciones: un estado de euforia, histeria no provocada o estallidos de risa, trastornos de coordinación y orientación, alucinaciones visuales y auditivas, una pérdida absoluta de la capacidad de controlar el propio comportamiento. Todas estas reacciones del sistema nervioso central ya amenazan la vida humana cuando se manifiestan. Hay un gran número de casos en los que personas, estando bajo la influencia de drogas consistentes en estas mezclas, saltaron desde el último piso de un rascacielos o nadaron en agua helada.
Con el consumo regular de "spice" se producen trastornos irreversibles del sistema nervioso central. Puede haber trastornos persistentes de la atención, debilitamiento de la memoria y disminución de la inteligencia, tendencia a la depresión y al suicidio. Entre otras cosas, los fumadores de "spice" tienen un riesgo muy alto de quedar discapacitados debido a lesiones graves del sistema nervioso central.
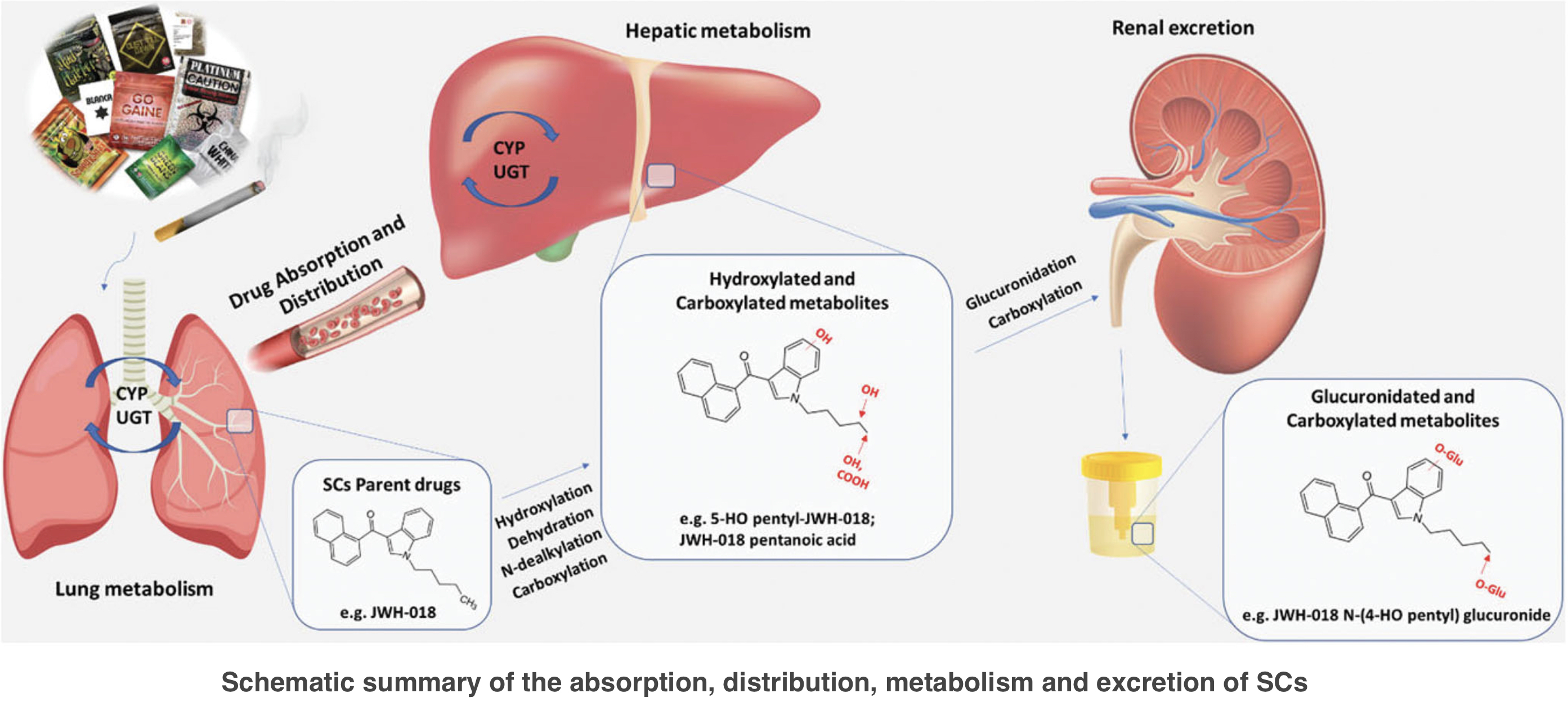
Si el humo contiene sustancias tóxicas, pueden producirse reacciones tóxicas: náuseas y vómitos, taquicardia e hipertensión, espasmos y convulsiones, desmayos y coma. La dificultad para eliminar las consecuencias de fumar mezclas de especias radica en que, en muchos casos, los compuestos narcóticos no se detectan en la sangre de los pacientes durante los análisis, lo que complica considerablemente el diagnóstico y el tratamiento adecuado. El uso sistemático de tales mezclas para fumar provoca una adaptación física y mental. Como resultado, el síndrome de abstinencia provoca síntomas como dolores corporales, náuseas, fiebre. Fumar una mezcla también provoca un trastorno mental. La memoria, la actividad mental y la atención se ven amenazadas. Según otras observaciones clínicas, el consumo prolongado de "spice" tiene un impacto negativo en el hígado y en los sistemas sexual y cardiovascular. Fumar "spice" también afecta a la erección, ralentiza la motilidad de los espermatozoides y altera el ciclo menstrual en las mujeres. El uso prolongado de cannabinoides sintéticos como parte de mezclas para fumar puede provocar el desarrollo de cáncer y trastornos mentales.
El hígado también sufre mucho. Sus células están expuestas a los efectos nocivos de los componentes tóxicos de la especia, especialmente peligrosos en caso de sobredosis, lo que no es raro. Algunas de las sustancias nocivas son neutralizadas por las células hepáticas, y un gran número de ellas mueren en el proceso; y el resto de las sustancias son transportadas por la sangre a través del cuerpo. El efecto sobre el sistema excretor se refleja en gran medida en el daño renal. Cuando los restos de sustancias tóxicas se excretan por la orina, se daña el parénquima renal y se forma una esclerosis (sustitución por tejido conjuntivo). Las sustancias activas de las mezclas de tabaco entran en el organismo a través de los pulmones junto con el humo cuando se inhala. La mayor parte de las sustancias atraviesa las paredes de los capilares pulmonares, entra en el torrente sanguíneo casi libremente y se propaga por todo el cuerpo.
Así, al controlar la composición de las mezclas para fumar, se observó que todos los tipos de cannabiтoides sintéticos tienen efectos diferentes en los receptores del cuerpo, por lo que es imposible decir cuándo se produce una sobredosis. Las sustancias psicoactivas, que forman parte del " spice ", afectan a los receptores cannabinoides - CB1 y CB2, pertenecientes al sistema de señalización endocannabinoide. Además, dependiendo de la composición de la mezcla, el efecto es diferente. Por ejemplo, el compuesto O2-propan-9β-oxi-11-norhexahidrocannabinol, que tiene una alta afinidad por los receptores cannabinoides del primer subtipo y presenta actividad agonística en experimentos in vitro, resultó mínimamente activo en experimentos con ratones (evaluación de efectos sedantes, antinociceptivos, cataleptogénicos e hipotérmicos). El cannabinoide 3-(1', 1' - dimetiletil)-D8-THC pertenece a los ligandos de alta afinidad de los receptores CB1 (supera 3 veces en afinidad al D9-THC), pero no tiene actividad biológica. Con el consumo regular de "spice", todo el organismo se resiente. Las funciones hepáticas se alteran, las funciones del sistema nervioso central se deprimen, los órganos de los sistemas excretor y respiratorio también sufren.
Una de estas sustancias psicoactivas es la mezcla de hierbas para fumar - "spice". Está disponible en el mercado en forma de hierbas con una sustancia química aplicada, y ha ganado rápidamente popularidad entre los jóvenes.
Clasificación de las sustancias que forman parte de las mezclas para fumar:
1. 1. Cannabinoides clásicos -ocannabinol, otros compuestos químicos presentes en el cannabis y análogos sintéticos estructuralmente relacionados, por ejemplo, AM-411, AM-906, HU-210, O-1184;
2. 2. Cannabinoides no clásicos: ciclohexilfenoles o 3-arilciclohexanoles, por ejemplo, CP-55.244, CP-55.940, CP-47.497 (y homólogos de C6-9);
3. 3. Cannabinoides híbridos: combinaciones de características estructurales de cannabinoides clásicos y no clásicos, por ejemplo, AM-4030;
4. Eicosanoides - endocannabinoides como la anandamida (AEA) y sus análogos sintéticos, por ejemplo, la metanandamida (AM-356);
5. Otros. Incluyen otros tipos estructurales - diarilpirazoles (por ejemplo, Rimonabant), naftoilpirroles (por ejemplo, JWH-307), naftilmetilindenos (por ejemplo, JWH-176) e indazolcarboxamidas (por ejemplo, APINACA).
6. Aminoalquilindoles, que pueden dividirse a su vez en los siguientes grupos
* fenilacetilindoles (JWH-250, JWH-251);
* benzoilindoles (pravadolina, AM-694, RSC-4);
* naftilmetilindoles (JWH-184);
* ciclopropoyl-idoles (UR-144, XLR-11);
* adamantoilindoles (AB-001, AM-1248);
* carboxamidas de indol (APICA, STS-135);
* naftoilindoles (por ejemplo, JWH-015, JWH-018, JWH-073, JWH-081, JWH-122, JWH-200, JWH-210, JWH-398);
Muchos derivados y análogos de las clases de compuestos mencionadas anteriormente pueden sintetizarse mediante la unión de halógenos, alquilos, alcoxilos u otros sustituyentes a uno de los sistemas cíclicos aromáticos.
El efecto de los cannabinoides clásicos.
Hasta la fecha, se conocen docenas de derivados del tetrahidrocannabinol que superan significativamente tanto al D8-THC como al D9-THC en términos de actividad biológica. Entre ellos se encuentran JWH-051, JWH-057, WH-102, JPG-103, así como D9-THC-3-dimetilheptilo, cannabinol-3-dimetilheptilo, 1-hidroxi-cannabinol-3-dimetilheptilo, 11-COOH-cannabinol-3-dimetilheptilo. Se detectó una alta afinidad por los receptores CB1 y una pronunciada actividad biológica en los derivados del D8-THC con varios radicales en la posición 3. Todos estos agentes tienen la estructura del tetrahidrocannabinol. Las propiedades del HU-210 se describen con más detalle a continuación.
Se sabe que el proceso de excitación del receptor cannabinoide implica su interacción con una proteína de unión a nucleótidos de guanina (proteína G). Sin dicha interacción, es imposible la posterior modulación de los sistemas transductores implicados en la neurotransmisión endocannabinoide (adenilato ciclasa, proteína quinasa activada por mitógenos, canales de calcio y potasio).
La capacidad de los agonistas cannabinoides para iniciar la interacción del receptor con la proteína G suele estimarse mediante el aumento de la unión de 35S-guanosina-5'-(-tio) - trifosfato (35S-GTPS). Se descubrió que el HU-210 potenciaba la unión del 35S-GTPS a los receptores CB1 humanos expresados en varios sistemas celulares, superando significativamente al D9-tetrahidrocannabinol y a otros agonistas CB1 en este indicador. Por ejemplo, con respecto a los receptores del primer subtipo expresados en células HEK-239, la capacidad de HU-210 para potenciar la unión de 35S-GTPS superó el indicador para CP-55940 en 11-17 veces, y para WIN-55212-2 - en 79 veces. Los receptores CB1 humanos se expresaron en el mismo sistema celular - en células HEK-239. El efecto del HU-210 fue 24 veces superior al del CP-55940 y 872 veces superior al del WIN-55212-2. En las preparaciones de las membranas sinápticas del cerebro de ratón, C57BL/6 HU-210 estimuló la unión de 35S-GTPS más activamente en comparación con D9-tetrahidrocannabinol. Superó al D9-THC en 28 veces, al CP-55940- en 2 veces, al WIN-55212-2 -en 59 veces, al JWH-073- en 12 veces. Hay que tener en cuenta que los compuestos CP-55940 y WIN-55212-2 se caracterizan por una elevada actividad biológica frente a los sistemas cannabinoides y se utilizan ampliamente en la investigación científica como eficaces agonistas del receptor CB1.
La inhibición cannabinoide de la actividad de la adenilato ciclasa estimulada por la forskolina se considera un importante equivalente neuroquímico de sus efectos farmacológicos. El HU-210 fue superior en este indicador a los cannabinoides CP-55940, anandamida, WIN-55212-2 y D9-THC, lo que también indica un alto potencial biológico del agente. Así, el IC50 del D9-tetrahidrocannabinol hacia la adenilato ciclasa (expresada en células CHO) fue de 16,51,2 nM, mientras que para la HU-210 fue de 0,1970,012 nM.
Como se deduce de lo anterior, los cannabinoides clásicos de la lista 1 HU-210 tienen una afinidad pronunciada por los receptores CB1, superando al D9-THC en este indicador. Esto sugiere que la sustancia psicoactiva considerada tiene una actividad biológica pronunciada y un potencial adictivo significativo, ya que para los agonistas cannabinoides, como para los agonistas de otros receptores, se observa una correlación directa entre la afinidad del receptor y la gravedad de los efectos biológicos. En experimentos con ratones, el HU-210 superó al D9-tetrahidrocannabinol en su capacidad de inhibir la SDA en 2900 veces, en su acción hipotérmica - en 900 veces, en su actividad antinociceptiva - en 240 veces.
El alto potencial adictivo del HU-210 se reveló en los primeros años tras su síntesis. En la prueba de discriminación con ratas macho Sprague-Dowley y palomas, la actividad adictiva del HU-210 superó el mismo indicador para el D9-THC en 66 y 80 veces, respectivamente. En estudios que utilizaron el método de aprendizaje para distinguir (discriminar) sustancias, el potencial adictivo del HU-210 fue muchas veces superior al de los agonistas CB1 de alta afinidad CP-55940 y BAY 38-7271, y diez veces superior en comparación con el D9-tetrahidrocannabinol.
El efecto de los cannabinoides no clásicos.
En la historia del estudio de las propiedades del CP-47497 se distinguen dos etapas. Inicialmente, se determinó la alta eficacia biológica de este fármaco, incluido un pronunciado potencial adictivo. Se cree que la actividad farmacológica del agente es aproximadamente 10 veces superior a la del D9-tetrahidrocannabinol. Más tarde, a medida que se introducían nuevos ligandos de los receptores CB1 y CB2, empezó a aparecer información sobre la gran afinidad de los receptores cannabinoides del primer subtipo por el CP-47497 y sus homólogos. Como se muestra, la mayor afinidad se detectó en el CP-47497 y en el CP-47497-C8.
En el estudio se evaluaron por primera vez los equivalentes conductuales a las exposiciones a CP-47497. El potencial antinociceptivo del agente en roedores (se utilizaron métodos de apretar la base de la cola, prueba de deslizamiento de la cola, etc.) fue comparable al de la morfina y superó al D9-tetrahidrocannabinol en varias veces. El agente CP-47497 resultó ser mucho más eficaz cuando se probó la inhibición de la actividad motora espontánea en roedores, el debilitamiento de la actividad convulsiva (choque electroconvulsivo), la acción hipotérmica y la inducción de ataxia en perros en comparación con el D9-THC. El potencial adictivo (según los resultados del método de discriminación en ratas) también fue muy superior al indicador del D9-tetrahidrocannabinol.
El CP-55940, un homólogo que tiene n-butanol en lugar de propanol en la posición 4 del anillo de ciclohexano, muestra una elevada actividad biológica. La afinidad de este compuesto es muchas veces superior al indicador correspondiente del CP-47497 (Ki = 1,12 ± 0,17 nM), y la actividad analgésica (evaluada mediante la prueba de retorcimiento en ratones) fue más de 4 veces superior en comparación con un efecto similar del CP-47497. El efecto antinociceptivo de otro homólogo que tiene propilciclohexano en la posición 4 es más de 6 veces superior al del CP-47497, y el Ki fue de 1,30 ± 0,57 nM. Cuando se alteró la estructura de la molécula CP-55940 con la sustitución del anillo de ciclohexano por cicloheptano, aumentó la afinidad por los receptores CB1 (Ki = 0,17 ± 0,04 nM) y la actividad analgésica (en 16 veces).
Aminoalquilindoles, indolilnaftilmetanos, indenos, pirroles y otros cannabinoides.
La primera síntesis del ancestro de los aminoalquilindoles WIN-55212-2 se llevó a cabo en 1991. Entonces, se estableció la elevada actividad biológica del WIN-55212-2 (en estudios con radioligandos y en experimentos con órganos aislados), y también se demostró su potencial adictivo (un método de entrenamiento de la discriminación). El WIN-55212-2 ha encontrado una amplia aplicación como sonda farmacológica de los receptores cannabinoides. También se utiliza con éxito como radioligando (3H-WIN-55212-2).
La actividad agonista de los aminoalquilindoles puede estimarse por el aumento de la unión específica de 35S-Gtp a las membranas del cerebro de roedores. Se demostró que el JWH-073 aumentaba la unión del análogo del GTP a las membranas sinápticas del cerebro de ratón en un 59% con respecto al nivel basal, con una EC50 = 34 nM. Para el D9-THC, los valores correspondientes fueron del 40% y 81 nM, respectivamente. La eficacia agonística de otros agentes fue significativamente mayor: para HU- 210, la ganancia máxima fue del 110% a ЕС50= 2,9 nM; los mismos indicadores para CP-55940 - 120% y 6,1 nM; para CP-55244 -120% y 0,12 nM. Al utilizar membranas cerebelosas de ratón como material biológico, la actividad de unión de JWH-073 a 35S-GTPgS fue menor: el aumento máximo alcanzó el 53%, ЕС50 = 490 nM. Los valores correspondientes para CP-55940 fueron 134% y 20 nM; para D9-THC - 54% y 260 nM.
Los efectos de los grupos de "nuevos cannabinoides" sobre la actividad de la adenilato ciclasa pueden demostrarse con un ejemplo de JWH-018. En el estudio, el efecto cannabinoide sobre la capacidad de inhibir la actividad de la adenilato ciclasa estimulada por la forskolina (valores en nM; los receptores CB1 humanos y la adenilato ciclasa se coexpresan en células CHO) fue el siguiente: CP-55940 = 5,5 ± 2,9; WIN-55212-2 = 38,9 ± 8,2; JWH-018 = 14,7 ± 3,9.
Entre las sustancias de los grupos considerados, hay agentes con una gran afinidad por los receptores cannabinoides. Por ejemplo, el compuesto JWH-048 era 4 veces superior al D9-ТHK en afinidad por los receptores CB1, y en su capacidad de cambiar los indicadores vegetativos y de comportamiento (inhibición de la SDA, efecto antinociceptivo, efecto hipotérmico) no era inferior al alcaloide del cannabis. También se encontró una alta afinidad por los receptores CB1 en JWH-164, JWH-180, JWH-181, JWH-182, JWH-210, JWH-212, JWH-213, JWH-234, JWH-240, JWH-242, JWH-258 y JWH-262. Sus constantes de inhibición de la unión específica del ligando CB1 3H-CP-55940 con las membranas sinápticas del cerebro de roedor fueron de 6,6 ± 0,7 nM; 26 ± 2 nM; 1.3±0,1 nM; 0,65 ± 0,03 nM; 0,46 ± 0,03 nM; 33,0 ± 0,9 nM; 1,5 ± 0,2 nM; 8,4 ± 1,8 nM; 14 ± 1 nM; 42 ± 9 nM; 4,6 ± 0,6 nM y 28 ± 3 nM, respectivamente.
Un indicador similar para el D9-tetrahidrocannabinol fue de 41 ± 2 nM. El aminoalquilindol JWH-398 (1-pentil-3-(4-cloro-1-naftol)indol se aisló de mezclas de fumadores. La afinidad por los receptores CB1 de este agente es alta (Ki = 2,3 nM).
Los 1-pentil-3-fenilacetilindoles (no contienen radical naftaleno) presentaron una afinidad superior por los receptores CB1 que el D9-tetrahidrocannabinol: JWH-203-5,1 veces; JWH - 204-3,2 veces; JWH - 249-4,9 veces; JWH - 250-3,7 veces; JWH - 251-1,4 veces; JWH - 252-1,8 veces; JWH - 302-2,4 veces; JWH - 305-2,7 veces; JWH - 306-1,6 veces; JWH - 311-1,8 veces.
BAY 38-7271, un compuesto sintetizado en el laboratorio de la empresa alemana Bayer AG, tiene una gran afinidad por los receptores del primer subtipo. Los valores de la constante de disociación 3H-BAY 38-7271 en experimentos con radioligandos con membranas sinápticas de cerebros de rata y humanos, así como con receptores CB1 humanos clonados, oscilaron entre 1,84 y 2,91 nM. En una serie paralela de experimentos, se obtuvieron valores similares para un ligando generalmente reconocido 3H-CP-55940. BAY 38-7271 en términos de eficacia agonística (evaluada por el grado de aumento de la unión 35S-Gtp a las membranas sinápticas de la corteza cerebral humana y del cerebro completo de rata), fue muchas veces superior al D9-tetrahidrocannabinol. La actividad biológica de BAY 38-7271 (capacidad de provocar hipotermia en ratas tras inyección intraperitoneal o intravenosa) se define como inferior en comparación con el mismo indicador para HU-210, pero era comparable a la de CP-55940 y WIN-55212-2. En condiciones experimentales similares, fue significativamente inferior en comparación con BAY 38-7271 en términos de actividad hipotérmica. El potencial adictivo de BAY 38-7271 se evaluó en ratas utilizando el método de distinción (discriminación) de sustancias, fue inferior en comparación con indicadores similares para HU-210 y CP-55940, pero fue diez veces superior al parámetro correspondiente para D9-tetrahidrocannabinol. Todos los equivalentes conductuales enumerados de los cannabinoides fueron prevenidos por los antagonistas de los receptores CB1 rimonabant (SR-141716A). Esto indica que los efectos adictivos se realizan a través de los receptores del primer subtipo.
Aspectos clínicos del efecto sobre el organismo
Los receptores CB1 pertenecen a la familia de receptores unidos a proteínas G y están ampliamente distribuidos en áreas del cerebro cuyas funciones están asociadas al control de la actividad motora, las funciones cognitivas, las reacciones emocionales, el comportamiento motivado y la homeostasis. En cuanto al efecto psicoactivo, los ligandos de los receptores cannabinoides del primer subtipo son los más importantes. Su activación está representada por euforia, sedación, disminución de la actividad motora espontánea (AME), efectos antinociceptivos, hipotermia, catalepsia. La combinación de estos equivalentes conductuales y fisiológicos constituye la base del potencial adictivo de los cannabinoides. Si hablamos del impacto sobre el estado mental de una persona, también podemos añadir un efecto alucinógeno a esta lista.
Los receptores CB2 se localizan principalmente en las células inmunitarias, tanto dentro como fuera del sistema nervioso central. El funcionamiento de estos receptores implica la modulación de la emisión de citoquinas y la migración de las células inmunitarias. En el cerebro, los receptores CB2 están presentes en la microglía, los vasos sanguíneos y algunas neuronas.
Las sustancias psicoactivas, que forman parte de la composición de la "especia", tienen un fuerte efecto en la mayoría de los sistemas corporales. El daño cerebral es el más pronunciado. Fumar la composición provoca un espasmo agudo de los vasos cerebrales - esto ocurre de forma refleja para reducir el paso de sustancias tóxicas al tejido cerebral. La vasoconstricción conduce a la hipoxia, la reducción de la viabilidad de las células cerebrales y su muerte.
Además, las mezclas de humo tienen una gran influencia en el sistema nervioso central. El efecto de los ingredientes del humo sobre el sistema nervioso central provoca adicción a fumar "picante". Como resultado, pueden manifestarse diversas reacciones: un estado de euforia, histeria no provocada o estallidos de risa, trastornos de coordinación y orientación, alucinaciones visuales y auditivas, una pérdida absoluta de la capacidad de controlar el propio comportamiento. Todas estas reacciones del sistema nervioso central ya amenazan la vida humana cuando se manifiestan. Hay un gran número de casos en los que personas, estando bajo la influencia de drogas consistentes en estas mezclas, saltaron desde el último piso de un rascacielos o nadaron en agua helada.
Con el consumo regular de "spice" se producen trastornos irreversibles del sistema nervioso central. Puede haber trastornos persistentes de la atención, debilitamiento de la memoria y disminución de la inteligencia, tendencia a la depresión y al suicidio. Entre otras cosas, los fumadores de "spice" tienen un riesgo muy alto de quedar discapacitados debido a lesiones graves del sistema nervioso central.
Si el humo contiene sustancias tóxicas, pueden producirse reacciones tóxicas: náuseas y vómitos, taquicardia e hipertensión, espasmos y convulsiones, desmayos y coma. La dificultad para eliminar las consecuencias de fumar mezclas de especias radica en que, en muchos casos, los compuestos narcóticos no se detectan en la sangre de los pacientes durante los análisis, lo que complica considerablemente el diagnóstico y el tratamiento adecuado. El uso sistemático de tales mezclas para fumar provoca una adaptación física y mental. Como resultado, el síndrome de abstinencia provoca síntomas como dolores corporales, náuseas, fiebre. Fumar una mezcla también provoca un trastorno mental. La memoria, la actividad mental y la atención se ven amenazadas. Según otras observaciones clínicas, el consumo prolongado de "spice" tiene un impacto negativo en el hígado y en los sistemas sexual y cardiovascular. Fumar "spice" también afecta a la erección, ralentiza la motilidad de los espermatozoides y altera el ciclo menstrual en las mujeres. El uso prolongado de cannabinoides sintéticos como parte de mezclas para fumar puede provocar el desarrollo de cáncer y trastornos mentales.
El hígado también sufre mucho. Sus células están expuestas a los efectos nocivos de los componentes tóxicos de la especia, especialmente peligrosos en caso de sobredosis, lo que no es raro. Algunas de las sustancias nocivas son neutralizadas por las células hepáticas, y un gran número de ellas mueren en el proceso; y el resto de las sustancias son transportadas por la sangre a través del cuerpo. El efecto sobre el sistema excretor se refleja en gran medida en el daño renal. Cuando los restos de sustancias tóxicas se excretan por la orina, se daña el parénquima renal y se forma una esclerosis (sustitución por tejido conjuntivo). Las sustancias activas de las mezclas de tabaco entran en el organismo a través de los pulmones junto con el humo cuando se inhala. La mayor parte de las sustancias atraviesa las paredes de los capilares pulmonares, entra en el torrente sanguíneo casi libremente y se propaga por todo el cuerpo.
Así, al controlar la composición de las mezclas para fumar, se observó que todos los tipos de cannabiтoides sintéticos tienen efectos diferentes en los receptores del cuerpo, por lo que es imposible decir cuándo se produce una sobredosis. Las sustancias psicoactivas, que forman parte del " spice ", afectan a los receptores cannabinoides - CB1 y CB2, pertenecientes al sistema de señalización endocannabinoide. Además, dependiendo de la composición de la mezcla, el efecto es diferente. Por ejemplo, el compuesto O2-propan-9β-oxi-11-norhexahidrocannabinol, que tiene una alta afinidad por los receptores cannabinoides del primer subtipo y presenta actividad agonística en experimentos in vitro, resultó mínimamente activo en experimentos con ratones (evaluación de efectos sedantes, antinociceptivos, cataleptogénicos e hipotérmicos). El cannabinoide 3-(1', 1' - dimetiletil)-D8-THC pertenece a los ligandos de alta afinidad de los receptores CB1 (supera 3 veces en afinidad al D9-THC), pero no tiene actividad biológica. Con el consumo regular de "spice", todo el organismo se resiente. Las funciones hepáticas se alteran, las funciones del sistema nervioso central se deprimen, los órganos de los sistemas excretor y respiratorio también sufren.
Last edited by a moderator:
