G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,965
- Solutions
- 3
- Reaction score
- 3,340
- Points
- 113
- Deals
- 1
Introduktion.
 Hvordan fungerer tyndlagskromatografi?
Hvordan fungerer tyndlagskromatografi?
 Forberedelse.
Forberedelse.
Fremstilling af kromatogrammet.
Tag en plast- eller glaskrukke, hæld 10-15 ml vand, 4-5 dråber jodalkoholopløsning. Rør rundt i 7-10 minutter. Dræn vandet. Jod udfældes i vandet på glassets sider. Sæt glasset i en beholder.
Retentionsfaktor
Når en separation er fuldført, ses de enkelte forbindelser som pletter, der er adskilt vertikalt. Hver plet har en retentionsfaktor (Rf), som er lig med den afstand, der migreres i forhold til den samlede afstand, der dækkes af opløsningsmidlet. Rf-formlen er Rf= afstand tilbagelagt af prøven/afstand tilbagelagt af opløsningsmidlet.
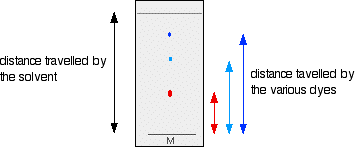 Rf-værdien kan bruges til at identificere forbindelser, fordi den er unik for hver enkelt forbindelse. Når man sammenligner to forskellige forbindelser under de samme betingelser, er forbindelsen med den største Rf-værdi mindre polær, fordi den ikke klæber til den stationære fase så længe som den polære forbindelse, der ville have en lavere Rf-værdi. Rf-værdier og reproducerbarhed kan påvirkes af en række forskellige faktorer såsom lagtykkelse, fugt på TLC-pladen, karrets mætning, temperatur, dybden af den mobile fase, TLC-pladens beskaffenhed, prøvestørrelse og opløsningsmiddelparametre. Disse effekter medfører normalt en stigning i Rf-værdierne. Men i tilfælde af lagtykkelse vil Rf-værdien falde, fordi den mobile fase bevæger sig langsommere op ad pladen.
Rf-værdien kan bruges til at identificere forbindelser, fordi den er unik for hver enkelt forbindelse. Når man sammenligner to forskellige forbindelser under de samme betingelser, er forbindelsen med den største Rf-værdi mindre polær, fordi den ikke klæber til den stationære fase så længe som den polære forbindelse, der ville have en lavere Rf-værdi. Rf-værdier og reproducerbarhed kan påvirkes af en række forskellige faktorer såsom lagtykkelse, fugt på TLC-pladen, karrets mætning, temperatur, dybden af den mobile fase, TLC-pladens beskaffenhed, prøvestørrelse og opløsningsmiddelparametre. Disse effekter medfører normalt en stigning i Rf-værdierne. Men i tilfælde af lagtykkelse vil Rf-værdien falde, fordi den mobile fase bevæger sig langsommere op ad pladen.
Diskussion af resultater
Metamfetamin - 0,55
Mefedron - 0,65
Konklusion.
Kromatografi bruges til at adskille blandinger af stoffer i deres bestanddele. Alle former for kromatografi fungerer efter samme princip. I denne artikel vil jeg forklare denne metode ved at definere Rf for amfetamin, metamfetamin og mefedron.
Kromatografiplader har en stationær fase (et fast stof eller en væske på et fast stof) og en mobil fase (en væske eller en gas). Den mobile fase flyder gennem den stationære fase og fører blandingens komponenter med sig. Forskellige komponenter bevæger sig med forskellig hastighed. Vi ser på årsagerne til dette længere nede på siden. Tyndlagskromatografi udføres præcis, som det hedder - ved hjælp af et tyndt, ensartet lag silicagel eller aluminiumoxid, der er belagt med et stykke glas, metal eller stiv plast. Silicagelen (eller aluminiumoxidet) er den stationære fase. Den stationære fase til tyndlagskromatografi indeholder også ofte et stof, som fluorescerer i UV-lys eller jodkammer - af grunde, som du vil se senere. Den mobile fase er et passende flydende opløsningsmiddel eller en blanding af opløsningsmidler.
Kromatografiplader har en stationær fase (et fast stof eller en væske på et fast stof) og en mobil fase (en væske eller en gas). Den mobile fase flyder gennem den stationære fase og fører blandingens komponenter med sig. Forskellige komponenter bevæger sig med forskellig hastighed. Vi ser på årsagerne til dette længere nede på siden. Tyndlagskromatografi udføres præcis, som det hedder - ved hjælp af et tyndt, ensartet lag silicagel eller aluminiumoxid, der er belagt med et stykke glas, metal eller stiv plast. Silicagelen (eller aluminiumoxidet) er den stationære fase. Den stationære fase til tyndlagskromatografi indeholder også ofte et stof, som fluorescerer i UV-lys eller jodkammer - af grunde, som du vil se senere. Den mobile fase er et passende flydende opløsningsmiddel eller en blanding af opløsningsmidler.
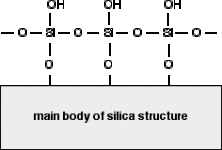
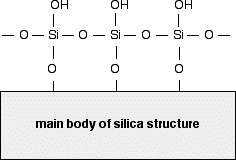
Silicagel er en form for siliciumdioxid (silica). Siliciumatomerne er forbundet via oxygenatomer i en gigantisk kovalent struktur. Men på overfladen af silicagelen er siliciumatomerne bundet til -OH-grupper. Så på overfladen af silicagelen har du Si-O-H-bindinger i stedet for Si-O-Si-bindinger. Diagrammet viser en lille del af silicaoverfladen. Silicagelens overflade er meget polær og kan på grund af -OH-grupperne danne hydrogenbindinger med egnede forbindelser omkring den samt Van-der-Waals-dispersionskræfter og dipol-dipol-attraktioner.
Det skal du bruge:
1. Sprøjte til 5 ml х 4
2. Urinprøveglas af plast х 4
3. Store plastikbeholdere til mad (eller et stort bægerglas og en plastikbeholder) х 2
4. TLC-plade med silicagelag 5x10 cm (du kan klippe en stor plade med en saks)
5. Opløsningsmidler ethylacetat, methanol, hexan (kan erstattes af carbontetrachlorid), vandig ammoniakopløsning 10% eller højere, jodalkoholopløsning
6. Blød blyant, lineal og tang
Glem ikke handsker og åndedrætsværn, og udfør eksperimentet i et ventileret rum.
1. Sprøjte til 5 ml х 4
2. Urinprøveglas af plast х 4
3. Store plastikbeholdere til mad (eller et stort bægerglas og en plastikbeholder) х 2
4. TLC-plade med silicagelag 5x10 cm (du kan klippe en stor plade med en saks)
5. Opløsningsmidler ethylacetat, methanol, hexan (kan erstattes af carbontetrachlorid), vandig ammoniakopløsning 10% eller højere, jodalkoholopløsning
6. Blød blyant, lineal og tang
Glem ikke handsker og åndedrætsværn, og udfør eksperimentet i et ventileret rum.
Fremstilling af kromatogrammet.
1. Du skal forberede en flydende opløsning ethylacetat:methanol:ammoniakopløsning 85:10:5. For 10 ml skal du tage 8,5 ml ethylacetat, 1 ml methanol og 0,5 ml ammoniakopløsning og blande det.
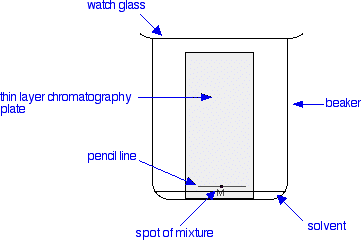
 2. Rengør pladen med silicagel med denne opløsning. Sæt pladen ned i opløsningen, den skal være 3-4 mm dyb i et stort bægerglas (som på billede 1). Du kan bruge en pincet til at manipulere med. Vigtigt: Gør ikke pladen våd med vand, for så bliver den ødelagt. Du skal holde pladen i opløsningen, indtil forsiden af opløsningsmidlet når op til den øverste kant af pladen.
2. Rengør pladen med silicagel med denne opløsning. Sæt pladen ned i opløsningen, den skal være 3-4 mm dyb i et stort bægerglas (som på billede 1). Du kan bruge en pincet til at manipulere med. Vigtigt: Gør ikke pladen våd med vand, for så bliver den ødelagt. Du skal holde pladen i opløsningen, indtil forsiden af opløsningsmidlet når op til den øverste kant af pladen.
Billede
3. Vi starter med et simpelt tilfælde. Der er fire stoffer: amfetamin (A), metamfetamin (L), koffein (K) og mephedron (M).
Til dette eksperiment skal du have en fri base af stoffer. Kom 10-15 mg af prøven (et par klumper) i et glas (plast), ren to dråber vandig ammoniakopløsning. Hæld derefter 3-4 dråber hexan eller carbontetrachlorid i glasset, og ryst det i et minut. Den frie base af dit lægemiddel fortyndes i det organiske lag.
med fri base

4. Nu skal du placere den på kromatografipladen, som blev forberedt tidligt. Tag en nål fra en sprøjte, og klip den af med en tang, som i eksemplet. Du skal have en flad kant.




 Tag en ren og tørret plade, og tegn en blyantlinje ca. 5-6 mm op fra den nederste kant. Enhver mærkning på pladen, som viser dråbens oprindelige placering, skal også være med blyant. Hvis noget af dette blev gjort med blæk, ville farvestoffer fra blækket også flytte sig, når kromatogrammet udviklede sig. Marker fire prikker med lige stor afstand mellem dem. Stik enden af den afklippede nål ned i det organiske lag af den første narkotiske opløsning. Rør ved pladen med spidsen af nålen, og lav en lille plet på 3-4 mm i diameter, vent, til den er tør, og gentag proceduren 10 gange. Gentag trin 2, 3 for andre stoffer.
Tag en ren og tørret plade, og tegn en blyantlinje ca. 5-6 mm op fra den nederste kant. Enhver mærkning på pladen, som viser dråbens oprindelige placering, skal også være med blyant. Hvis noget af dette blev gjort med blæk, ville farvestoffer fra blækket også flytte sig, når kromatogrammet udviklede sig. Marker fire prikker med lige stor afstand mellem dem. Stik enden af den afklippede nål ned i det organiske lag af den første narkotiske opløsning. Rør ved pladen med spidsen af nålen, og lav en lille plet på 3-4 mm i diameter, vent, til den er tør, og gentag proceduren 10 gange. Gentag trin 2, 3 for andre stoffer.
Almindelig fejl: Lav ikke en stor fedtplet, fordi dit stof kan overlejre andre stoffer under forsøget.
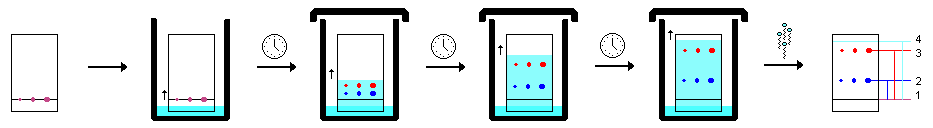
5. Når pletterne af frie baser er tørre, stilles pladen i et lavt lag opløsningsmiddel i et tildækket bægerglas. Det er vigtigt, at niveauet af opløsningsmiddel er under linjen med pletten på. Vent, indtil opløsningsmidlets frontlinje når 4-5 mm før den øverste kant af pladen, og træk den ud. Tegn derefter en blyantlinje på opløsningsmidlets forreste linje. Tør den med luft.

 6. Kromatogrammet placeres i en lukket beholder (f.eks. et andet bægerglas dækket med et urglas eller store plastikbeholdere) sammen med nogle få jodkrystaller. Joddampen i beholderen reagerer med pletter på kromatogrammet. De stoffer, du er interesseret i, kan dukke op som farvede pletter. Spor dem med en blyant, og tegn prikker i midten af hver plet.
6. Kromatogrammet placeres i en lukket beholder (f.eks. et andet bægerglas dækket med et urglas eller store plastikbeholdere) sammen med nogle få jodkrystaller. Joddampen i beholderen reagerer med pletter på kromatogrammet. De stoffer, du er interesseret i, kan dukke op som farvede pletter. Spor dem med en blyant, og tegn prikker i midten af hver plet.
 Du kan også bruge en UV-lampe med 254 og 365 nm bølgelængde.
Du kan også bruge en UV-lampe med 254 og 365 nm bølgelængde.

Sådan klargør du jodkammeret.Almindelig fejl: Lav ikke en stor fedtplet, fordi dit stof kan overlejre andre stoffer under forsøget.
5. Når pletterne af frie baser er tørre, stilles pladen i et lavt lag opløsningsmiddel i et tildækket bægerglas. Det er vigtigt, at niveauet af opløsningsmiddel er under linjen med pletten på. Vent, indtil opløsningsmidlets frontlinje når 4-5 mm før den øverste kant af pladen, og træk den ud. Tegn derefter en blyantlinje på opløsningsmidlets forreste linje. Tør den med luft.
Tag en plast- eller glaskrukke, hæld 10-15 ml vand, 4-5 dråber jodalkoholopløsning. Rør rundt i 7-10 minutter. Dræn vandet. Jod udfældes i vandet på glassets sider. Sæt glasset i en beholder.
Retentionsfaktor
Når en separation er fuldført, ses de enkelte forbindelser som pletter, der er adskilt vertikalt. Hver plet har en retentionsfaktor (Rf), som er lig med den afstand, der migreres i forhold til den samlede afstand, der dækkes af opløsningsmidlet. Rf-formlen er Rf= afstand tilbagelagt af prøven/afstand tilbagelagt af opløsningsmidlet.
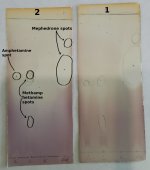
I forsøget fik jeg tre pletter i stedet for de forventede fire. Gentagelse af forsøget viser, at koffein ikke kan elueres med en opløsning af ethylacetat:methanol:ammoniak 85:10:5. Eksperimentelt godkendt, at denne opløsning er egnet til eluering af stoffer som amfetamin, metamfetamin og mephedron.
 Rf af undersøgte stoffer.
Rf af undersøgte stoffer.
Amfetamin - 0,53Metamfetamin - 0,55
Mefedron - 0,65
Forklaring.
Jeg har fået to plader med resultater. To målte afstande mellem startpunktet og midten af den omkransede plet. Amfetaminpletten gik 42 i den første plade og 49 mm i den anden plade fra startlinjen, opløsningsmiddelfrontlinjen gik henholdsvis 85 og 86 mm. Rf1=42/85=0.49, Rf2=49/86=0.52. Derefter beregnede jeg det aritmetiske gennemsnit til 0,53. Samme beregninger blev foretaget for andre stoffer.
Jeg har fået to plader med resultater. To målte afstande mellem startpunktet og midten af den omkransede plet. Amfetaminpletten gik 42 i den første plade og 49 mm i den anden plade fra startlinjen, opløsningsmiddelfrontlinjen gik henholdsvis 85 og 86 mm. Rf1=42/85=0.49, Rf2=49/86=0.52. Derefter beregnede jeg det aritmetiske gennemsnit til 0,53. Samme beregninger blev foretaget for andre stoffer.
Konklusion.
Som forsøget viser, kan du måle Rf for dit stof og sammenligne med et kendt stof i samme plade. Lav en plet af din stoffri base og 1-4 pletter af andre stoffer for at kontrollere Rf. Hvis pletterne er i samme afstand fra startlinjen, er det sandsynligvis det samme stof. Og hvis du får flere pletter fra dit stof, har du sandsynligvis en blanding af stoffer. Nogle stoffer har flere pletter, fordi de er en blanding af stof og biprodukter fra syntese. Du kan dog sammenligne dem med andre stoffer ved hjælp af tyndtlagskromatografi.
Attachments
Last edited by a moderator: